Analysis in clinical features of acute pontine infarction patients with imaging manifestation as "pontine hemisection sign"
-
摘要:目的 探讨影像学表现为“脑桥半切征”的急性脑桥梗死患者的临床特征、病因及预后。方法 收集影像学表现为“脑桥半切征”的11例急性脑桥梗死患者的临床资料,结合文献回顾性分析其临床表现、影像学特征、病因以及预后。结果 11例急性脑桥梗死患者核磁共振成像(MRI)形态学均表现为“脑桥半切征”。患者均为急性起病,平均年龄(72.64±8.26)岁,危险因素以高血压病、糖尿病及高脂血症为主。11例患者临床症状均表现为病灶对侧肢体瘫痪和构音障碍,伴有对侧偏身感觉减退5例,中枢性面瘫8例,中枢性舌瘫7例,眩晕或头晕5例,眼震4例以及共济失调3例。11例患者出院时美国国立卫生研究院卒中量表(NIHSS)评分为(4.91±2.54)分。所有患者MRI检查均显示病灶累及脑桥腹前内侧区,其中3例合并累及前外侧区。3例患者磁共振血管造影(MRA)检查发现存在椎基底动脉重度狭窄或闭塞。结论 “脑桥半切征”是急性脑桥梗死的一种特殊影像学征象,典型临床表现为突发起病的对侧肢体瘫痪、构音障碍及中枢性面瘫,可伴有眩晕和眼震等症状,其主要病因机制为基底动脉分支病变和大动脉闭塞性疾病,多数患者临床预后较好。Abstract:Objective To investigate the clinical features, etiology and outcomes of acute pontine infarction patients with imaging manifestation as "pontine hemisection sign".Methods Clinical materials of 11 acute pontine infarction patients with imaging manifestation as "pontine hemisection sign" were collected, and their clinical manifestations, imaging features, etiology and outcomes were retrospectively analyzed based on literature review.Results The morphology of magnetic resonance imaging (MRI) in 11 patients with acute pontine infarction showed "pontine hemisection sign". All the patients were acute onset, with an average age of (72.64±8.26) years old, and the main risk factors were hypertension, diabetes and hyperlipidemia. The clinical symptoms of 11 patients were contralateral limb paralysis and dysarthria, accompanied by contralateral hemiparesis in 5 cases, central facial paralysis in 8 cases, central lingual paralysis in 7 cases, vertigo or dizziness in 5 cases, nystagmus in 4 cases and ataxia in 3 cases. The mean National Institutes of Health Stroke Scale (NIHSS) score of 11 patients at discharge was (4.91±2.54) points. MRI examination of all patients showed that the lesions involved the ventral, medial and medial areas of pons, of which 3 cases involved the anterolateral area. Severe stenosis or occlusion of vertebrobasilar artery was found in 3 patients by magnetic resonance angiography (MRA).Conclusion "Pontine hemisection sign" is a special imaging sign of acute pontine infarction, the typical clinical manifestations are sudden onset contralateral limb paralysis, dysarthria and central facial paralysis, which can be accompanied by symptoms such as vertigo and nystagmus. Its main etiological mechanism is basilar artery branch degeneration and large artery occlusive disease, and most patients have a good clinical prognosis.
-
慢性阻塞性肺疾病(COPD)是一种常见的以持续性呼吸道症状和气流受限为特征的呼吸道疾病[1]。40岁以上人群COPD发病率在全球约11.5%, 在中国约13.7%[2-3]。高血压病是其最常见的合并症,约有70.9%的COPD患者伴有原发或继发性高血压病,显著增高了心血管事件的发生风险[4-5]。COPD易伴发高血压病可能与肥胖、吸烟、冠状动脉疾病等因素有关。此外,使用长效β2受体激动剂(LABA)可增高COPD患者高血压病的患病率[4]。目前相关研究多对治疗后的COPD患者展开,不能排除COPD治疗药物的影响。本研究评估未治疗的初诊COPD伴高血压病的患病率、临床特征及危险因素,现报告如下。
1. 资料与方法
1.1 一般资料
在苏州市4个社区开展基于人群的横断面研究。根据每个社区40岁以上人口基数采用整群抽样策略决定样本量,并由本研究组对抽样人群进行进一步筛查。本研究经南京医科大学附属苏州医院伦理委员会批准(K2018013)。对抽样人群采用电话通知,在社区卫生服务中心由本研究组成员进行调查问卷和研究知情同意告知,受试者签署知情同意书。排除标准: ①患者患有不宜进行肺功能检查的疾病(气胸、肺大疱)。②患者具有肺癌、支气管扩张、继发性高血压和心肺手术病史。
本研究于2018年6月1日—12月31日共纳入4 725例受试者(2 188例男性, 2 537例女性),经肺功能检测确诊COPD 586例,排除既往确诊COPD及用药(支气管舒张剂及糖皮质激素)17例,纳入初诊COPD 569例(261例男性, 308例女性),年龄41~92岁,其中COPD伴高血压病组共249例,不伴高血压病组320例, 40岁以上初诊COPD中高血压的患病率约43.1%。
1.2 方法
纳入受试者后进行调查问卷、血液检查、握力检查和肺功能检查。调查问卷包括一般情况(年龄、性别、身高、体质量)、吸烟史、慢性支气管炎家族史、慢性病史、职业暴露史、呼吸困难评分。血液检查包括血常规、肝肾功能、血脂检测。采用XE-5000血细胞分析仪(Sysmex公司,日本)进行血常规检测。采用7600全自动生化检测仪(HITACHI公司,日本)进行血生化检测。采用EH101电子握力计(广东香山衡器集团股份有限公司,中国)进行握力测试,重复3次,结果取平均值。采用便携式肺功能仪(橙易公司,中国)进行肺功能检查。肺功能检查流程参照美国胸科协会肺功能检测标准[6], 每名受试者接受3次肺功能检测,结果取平均值。若肺功能检测提示气流受限,受试者吸入200 μg沙丁胺醇后15~20 min再行肺功能检查,重复3次,结果取平均值。COPD诊断标准及分级参照2018年慢性阻塞性肺疾病全球倡议(GOLD)。吸入支气管舒张剂后第1秒用力呼气量与用力肺活量比值(FEV1/FVC)<70%诊断为COPD。COPD分级: FEV1≥80%预计值为Ⅰ级, FEV1≥50%~<80%预计值为Ⅱ级, FEV1≥30%~<50%预计值为Ⅲ级, FEV1<30%预计值为Ⅳ级。
1.3 观察指标
对COPD伴或不伴高血压病患者的呼吸道症状及生活质量评分; 观察COPD伴或不伴高血压病患者的血液指标; 分析初诊COPD伴高血压病的高危因素。
1.4 统计学分析
采用SPSS 21.0软件进行数据统计。计数资料采用t检验或方差分析,计量资料采用卡方检验进行分析,危险因素采用二分类Logist回归分析。P<0.05为差异有统计学意义。
2. 结果
2.1 2组初诊COPD患者一般情况
COPD伴高血压病组平均年龄、男性比率、体质量指数(BMI)、吸烟指数高于COPD不伴高血压病组,差异有统计学意义(P<0.05)。COPD伴高血压病组合并糖尿病和心血管疾病比率均高于COPD不伴高血压病组,差异有统计学意义(P<0.05)。见表 1。
表 1 2组初诊COPD患者一般情况比较(x±s)[n(%)]项目 COPD伴高血压病(n=249) COPD不伴高血压病(n=320) P值 年龄/岁 71.0±9.1 66.2±10.5 <0.001 性别 男 128(51.4) 133(41.6) 0.019 女 121(48.6) 187(58.4) 身高/cm 159.2±8.9 159.2±7.9 0.951 体质量/kg 61.2±11.3 57.8±8.8 <0.001 体质量指数/(kg/m2) 24.1±3.4 22.8±2.8 <0.001 吸烟史 有 89(35.7) 92(28.8) 0.076 无 160(64.3) 228(71.2) 吸烟指数(包/年) 11.9±22.4 7.6±15.1 0.011 慢性支气管炎 有 29(11.6) 30(9.4) 0.407 无 220(88.4) 290(80.6) 糖尿病 有 53(21.3) 25(7.8) <0.001 无 196(78.7) 295(92.2) 心血管疾病 有 23(9.2) 12(3.8) 0.008 无 226(90.8) 308(96.2) 2.2 2组呼吸道症状及生活质量评分
2组均有约50%初诊COPD患者无呼吸道症状。2组初诊COPD患者在肺功能严重程度方面差异均无统计学意义(P>0.05)。在生活质量方面, COPD伴高血压病组握力低于COPD不伴高血压病组,但差异无统计学意义(P>0.05), COPD伴高血压病组改良呼吸困难指数(mMRC)和慢性阻塞性肺疾病评估测试(CAT)评分均高于COPD不伴高血压病组,差异有统计学意义(P<0.05)。见表 2。
表 2 2组呼吸道症状及生活质量评分比较(x±s)[n(%)]项目 COPD伴高血压病(n=249) COPD不伴高血压病(n=320) P 呼吸道症状 有 124(49.8) 149(46.6) 0.443 无 125(50.2) 171(53.4) mMRC/分 0.5±0.8 0.4±0.6 0.015 CAT/分 9.3±2.6 8.8±1.6 0.008 GOLD分级 1级 87(34.9) 108(33.8) 0.952 2级 117(47.0) 158(49.4) 3级 36(14.5) 43(13.4) 4级 9(3.6) 11(3.4) 握力/kg 25.5±8.2 26.5±8.4 0.271 mMRC: 改良呼吸困难指数; CAT: 慢性阻塞性肺疾病评估测试。 2.3 2组初血液指标情况
COPD伴高血压病组白细胞总数、中性粒细胞计数、嗜酸性粒细胞计数、单核细胞计数均高于COPD不伴高血压病组,差异有统计学意义(P<0.05); 2组血红蛋白、血小板计数比较,差异无统计学意义(P>0.05)。COPD伴高血压病组静脉空腹血糖、甘油三酯、尿酸、血肌酐水平均高于COPD不伴高血压病组,高密度脂蛋白胆固醇水平低于COPD不伴高血压病组,差异有统计学意义(P<0.05)。见表 3。
表 3 2组血液指标情况比较(x±s)项目 COPD伴高血压病(n=249) COPD不伴高血压病(n=320) 白细胞计数/(×109/L) 6.3±1.5* 5.8±1.5 中性粒细胞计数/(×109/L) 3.7±1.0* 3.4±1.2 淋巴细胞计数/(×109/L) 2.1±0.8* 2.0±0.6 嗜酸性粒细胞计数/(×109/L) 0.2±0.1* 0.1±0.1 单核细胞计数/(×109/L) 0.5±0.1* 0.4±0.1 血红蛋白/(g/L) 136.2±15.4 136.1±15.5 血小板计数/(×109/L) 192.4±50.3 191.4±63.7 空腹血糖/(mmol/L) 6.2±1.9* 5.6±1.0 甘油三酯/(mmol/L) 1.6±1.2* 1.2±0.6 血肌酐/(μmol/L) 81.3±31.0* 72.7±55.1 尿酸/(μmol/L) 341.3±97.8* 300.0±73.9 高密度脂蛋白胆固醇/(mmol/L) 1.3±0.3* 1.4±0.3 与COPD不伴高血压病组比较, * P<0.05。 2.4 初诊COPD伴高血压病高危因素分析
年龄、体质量、单核细胞计数、空腹血糖是COPD合并高血压病的独立危险因素。40岁以上人群年龄每增加1岁, COPD伴高血压病风险增加1.051倍(95% CI为1.015~1.088), 体质量每增加1 kg, COPD伴高血压病风险增加1.06倍(95% CI为1.017~1.105), 单核细胞计数每增加1×109/L, COPD伴高血压病风险增加26.324倍(95% CI为1.912~362.419), 空腹血糖每增加1 mmol/L, COPD伴高血压病风险增加1.557倍(95% CI为1.101~2.201)。见表 4
表 4 初诊COPD伴高血压病的高危因素项目 P OR 95% CI 年龄/岁 0.005 1.051 1.015 1.088 体质量/kg 0.006 1.060 1.017 1.105 单核细胞计数/(×109/L) 0.015 26.324 1.912 362.419 空腹血糖/(mmol/L) 0.012 1.557 1.101 2.201 3. 讨论
高血压病为COPD的一项常见合并症[4], 目前研究[5-7]认为合并高血压可增高COPD患者发生心血管疾病的风险及死亡率。高血压病可导致基线肺功能下降及COPD患者肺功能损害程度加重[8-11], 其机制尚不明确,研究[10]发现小动脉弹性和肺功能呈正相关性。此外,假说认为全身慢性炎症反应介导了肺功能和心血管疾病的相关性。
本研究共纳入569例经肺功能筛查的初诊COPD患者,其中COPD伴高血压病组249例, COPD不伴高血压病组320例。COPD伴高血压病组平均年龄显著高于不伴高血压病组。在性别构成方面, COPD伴高血压病组男性显著更多,可能与女性雌激素的保护作用及不同的生活习惯(吸烟、饮酒、饮食)有关[12]。在合并症方面, COPD伴高血压病组合并糖尿病、心血管病比例更高,出现代谢指标(高血糖、高甘油三酯血症、高密度脂蛋白胆固醇)异常的比例也更高。2组COPD患者呼吸道症状、肺功能、握力无显著差别,但COPD伴高血压病组mMRC和CAT评分更高,提示生活质量更差。多因素分析表明,高龄、体质量高、单核细胞绝对值增高、空腹血糖升高是COPD伴高血压病的独立危险因素。
随着年龄增长,高血压病和COPD的患病率呈上升趋势[13]。一项慢阻肺人群中高血压、糖尿病、心血管疾病的流行病学研究[14]表明, 45岁以上COPD中高血压患病率为40.1%, 年龄越高,高血压等合并症的患病率越高。本研究表明, 40岁以上初诊COPD中高血压病患病率为43.8%, 年龄每增加1岁,高血压病风险增加1.051倍。年龄相关的高血压共患率增高可能与高龄所致细胞衰老增加、干细胞衰竭、氧化应激增加、细胞外基质改变、内源性抗衰老分子减少等有关[15]。相关研究[16]表明,男性COPD患病率明显高于女性。本研究中,男性COPD合并高血压病的患病率为49.0%, 显著高于女性的39.3% (P<0.05), 其机制可能主要与男性生活习惯(吸烟)有关。吸烟是COPD和高血压病的共同危险因素,并导致其他共患病如冠脉疾病、心力衰竭、糖尿病的发生[17-19]。本研究中COPD伴高血压病组的吸烟指数明显高于不伴高血压病组,与相关研究[13]结果相符,提示吸烟可增加高血压病的共患风险。吸烟导致COPD合并症患病率的增加主要与氧化应激增加,上皮细胞、内皮细胞功能紊乱及动脉粥样硬化有关[20]。早中期COPD伴有高BMI更容易出现高血压、糖尿病、冠脉疾病[21], 本研究发现,体质量、BMI是COPD伴高血压病的危险因素,但多因素分析显示仅体质量是COPD伴高血压病的独立危险因素,可能与研究样本量较小有关,有待更多大样本研究验证。肥胖导致COPD合并高血压患病率的增高可能与血脂异常、胰岛素抵抗及全身炎症所致的肺损伤有关。随着COPD严重程度的增加,营养状况恶化,肌肉萎缩, BMI下降,伴发高血压病等合并症的患病率反而下降,此时,低BMI是重度COPD住院死亡的重要危险因素。
一项大规模横断面研究[22]表明,校正年龄、性别、吸烟状态、酒精摄入、教育、BMI、体力活动和冠心病等因素后,高血糖、腹部肥胖、高血压仍是肺功能损害的独立危险因素,其机制可能与胰岛素调节异常、脂肪酸增多有关[23-26]。另外,高血压、高甘油三酯血症,显著增加COPD急性加重的风险[27]。本研究发现COPD伴高血压病组代谢异常(高血糖、高甘油三酯血症、低高密度脂蛋白胆固醇水平、高尿酸)更常见,其中高血糖是COPD伴高血压病的独立危险因素,这与LEONE N等[22]研究结果相似。本研究中COPD患者为初诊,未曾接受糖皮质激素治疗,其发生高血糖可能主要与全身性炎症有关,促炎细胞因子通过阻断胰岛素受体的信号传导诱导胰岛素抵抗,增加高血糖的风险[28]。COPD往往伴随全身系统性炎症反应,稳定期COPD也有外周血白细胞、中性粒细胞、C反应蛋白、纤维蛋白原、白细胞介素6(IL-6)和肿瘤坏死因子α(TNF-α)水平增高[29],这种全身炎症反应也可见于原发性高血压、糖尿病等慢性病[30-31], 可能与吸烟、肥胖、高龄等导致的氧化应激反应有关。本研究发现, COPD伴高血压病组外周血白细胞、中性粒细胞、嗜酸性粒细胞、单核细胞明显升高,校正年龄、性别、吸烟量、糖尿病、BMI、高脂血症后,该组外周血单核细胞仍显著高于对照组,提示合并高血压病可加重COPD患者全身系统性炎症反应,造成单核巨噬细胞系统活化和更多的中性粒细胞趋化细胞因子释放。一项研[32]究显示, COPD外周血单核细胞及其中的多种细胞因子如基质金属蛋白酶-12(MMP-12)、中性粒细胞弹性蛋白酶(NE)、金属蛋白酶组织抑制剂(TIMP-4)明显高于对照组。在另一项研究[33]中,外周血单核细胞升高,白细胞介素4(IL-4)表达的增加,与血管粥样硬化和心血管疾病密切相关。
高血压是肺功能损害的重要危险因素,并且显著增加COPD急性加重风险[34]。本研究中, COPD伴高血压病组mMRC、CAT评分显著高于不伴高血压病组,提示COPD伴高血压病组生活质量更差,分析原因可能与合并症带来的症状及焦虑情绪等有关。
综上所述, 40岁以上初诊COPD中高血压的患病率约43.1%, COPD伴高血压病在男性、肥胖、吸烟者更为多见,其与血糖、血脂代谢异常密切相关。高龄、肥胖、单核细胞计数升高、空腹血糖升高是COPD伴高血压病的独立危险因素。因此,对COPD患者应进行系统化管理,减少危险因素暴露,定期监测代谢指标,预防和控制并发症,改善预后。
-
表 1 11例表现为“脑桥半切征”的急性脑桥梗死患者临床资料
序号 年龄 性别 危险因素 梗死部位 MRA检查结果 神经系统症状 入院时
NIHSS评分/分出院时
NIHSS评分/分1 64岁 男 糖尿病 右侧脑桥 未见异常 构音障碍、口角歪斜、左侧偏瘫及左侧肢体共济失调 5 4 2 79岁 女 高血压病、卒中史、高同型半胱氨酸 右侧脑桥 未见异常 头晕、构音障碍、口角歪斜及左侧偏瘫 7 4 3 60岁 男 高血压病、吸烟、高同型半胱氨酸 右侧脑桥 基底动脉重度狭窄 构音障碍、口角歪斜及左侧偏瘫 4 7 4 80岁 男 高血压病、糖尿病、高同型半胱氨酸、高脂血症 左侧脑桥 未见异常 构音障碍、口角歪斜、右侧偏瘫及偏身感觉减退 4 4 5 70岁 男 高血压、高脂血症、卒中史、吸烟及饮酒 左侧脑桥 右侧椎动脉发育不良 眩晕、构音障碍、右侧偏瘫及偏身感觉减退 6 5 6 78岁 女 糖尿病、高脂血症 左侧脑桥 左侧椎动脉发育不良 构音障碍、右侧偏瘫及右侧肢体共济失调 4 4 7 79岁 男 高血压病、高同型半胱氨酸、高脂血症 右侧脑桥 基底动脉及左侧椎动脉V4段重度狭窄 头晕、构音障碍、口角歪斜、左侧偏瘫及偏身感觉减退 9 12 8 62 女 高血压病 左侧脑桥 未见异常 构音障碍、右侧偏瘫及右侧偏身感觉减退 5 4 9 81岁 男 高血压病、糖尿病 左侧脑桥 未见异常 头晕、构音障碍、口角歪斜、右侧偏瘫及感觉减退 6 3 10 82 女 高血压病、糖尿病、高脂血症 左侧脑桥 基底动脉重度狭窄,左侧椎动脉V4段闭塞 头晕、构音障碍、口角歪斜、右侧偏瘫 5 5 11 64 女 糖尿病 左侧脑桥 未见异常 构音障碍、口角歪斜、右侧偏瘫及右侧肢体共济失调 5 2 表 2 11例急性脑桥梗死患者具体梗死部位和病灶纵深比
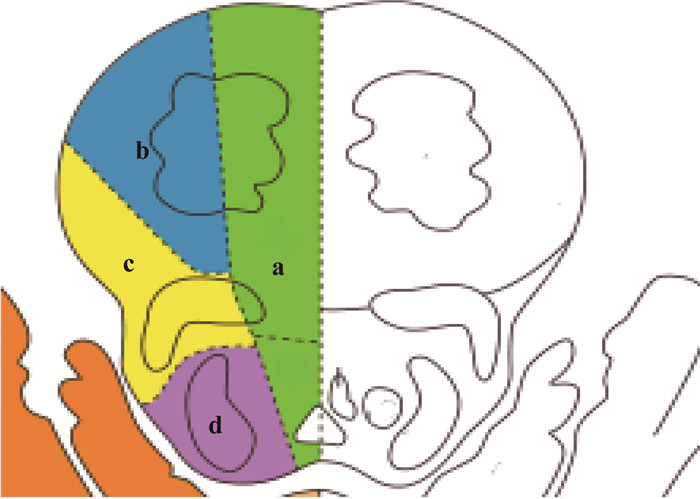
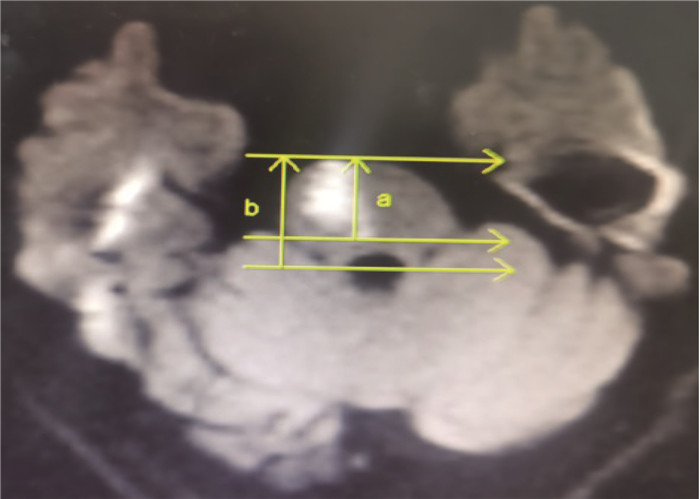
序号 梗死部位 纵深比/% 1 腹前内侧 74.5 2 腹前内侧+前外侧 78.6 3 腹前内侧 73.3 4 腹前内侧 73.0 5 腹前内侧 72.3 6 腹前内侧 67.1 7 腹前内侧+前外侧 80.9 8 腹前内侧 73.8 9 腹前内侧 73.5 10 腹前内侧+前外侧 75.3 11 腹前内侧 76.2 -
[1] 陈君, 李永秋, 高海凤, 等. 孤立性脑桥梗死病情进展相关因素分析[J]. 华北理工大学学报: 医学版, 2020, 22(5): 376-381. https://www.cnki.com.cn/Article/CJFDTOTAL-MTYX202005011.htm [2] 徐辉, 宋晶晶, 陈静, 等. 老年急性孤立性脑桥梗死患者早期运动功能缺损进展的相关危险因素分析[J]. 中华老年心脑血管病杂志, 2021, 23(1): 67-70. doi: 10.3969/j.issn.1009-0126.2021.01.017 [3] ERRO M E, G LLEGO J, HERRERA M, et al. Isolated pontine infarcts: Etiopathogenic mechanisms[J]. Eur J Neurol, 2005, 12(12): 984-988. doi: 10.1111/j.1468-1331.2005.01119.x
[4] 王丽娟, 王光彬, 刘玉波, 等. 脑干梗死的一种特殊MR征象分析[J]. 山东大学学报: 医学版, 2011, 49(5): 111-118. https://www.cnki.com.cn/Article/CJFDTOTAL-SDYB201105024.htm [5] 李彬, 姜丹, 尹世杰. "脑桥半切征"在分支动脉粥样硬化病中的意义(附4例报道及文献复习)[J]. 卒中与神经疾病, 2018, 25(6): 710-712. doi: 10.3969/j.issn.1007-0478.2018.06.021 [6] 钟迪, 张舒婷, 吴波. 《中国急性缺血性脑卒中诊治指南2018》解读[J]. 中国现代神经疾病杂志, 2019, 19(11): 897-901. doi: 10.3969/j.issn.1672-6731.2019.11.015 [7] 张铁林, 孙中武. 急性脑桥梗死危险因素和梗死部位对近期预后的影响[J]. 安徽医科大学学报, 2020, 55(5): 776-779. https://www.cnki.com.cn/Article/CJFDTOTAL-YIKE202005024.htm [8] 赵凤丽, 刘宏顺. 新发孤立脑干梗死患者的病因和影像特点研究[J]. 中国临床医学影像杂志, 2020, 31(1)774-782. https://www.cnki.com.cn/Article/CJFDTOTAL-LYYX202011006.htm [9] JU Y, HUSSAIN M, ASMARO K, et al. Clinical and imaging characteristics of isolated pontine infarcts: a one-year follow-up study[J]. Neurol Res, 2013, 35(5): 498-504. doi: 10.1179/1743132813Y.0000000207
[10] 韩新生, 张高才, 刘宁, 等. 基底动脉狭窄程度与孤立性脑桥梗死短期转归的相关性[J]. 中华老年医学杂志, 2021, 40(3): 315-318. doi: 10.3760/cma.j.issn.0254-9026.2021.03.009 [11] LI H, DAI Y, WU H, et al. Predictors of early neurologic deterioration in acute pontine infarction[J]. stroke, 2020, 5l(2): 637-640.
[12] KUMRAL E, BAYVLKEM G, EVYAPAN D. Clinical spectrum of pontine infarction. Clinical-MRI correlations[J]. J Neurol, 2002, 249(12): 1659-1670. doi: 10.1007/s00415-002-0879-x
[13] HUANG J, QIU Z, ZHOU P, et al. Topographic location of unisolated pontine infarction[J]. BMC Neurol, 2019, 19(1): 186. doi: 10.1186/s12883-019-1411-6
[14] ZHOU L, YAO M, PENG B, et al. Atherosclerosis Might Be Responsible for Branch Artery Disease: Evidence From White Matter Hyperintensity Burden in Acute Isolated Pontine Infarction[J]. Front Neurol, 2018, 9: 840. doi: 10.3389/fneur.2018.00840
[15] KOBAYASHI J, OHARA T, MINEMATSU K, et al. Etiological mechanisms of isolated pontine infarcts based on arterial territory involvement[J]. J NeurolSci, 2014, 339(1/2): 113-117. http://www.onacademic.com/detail/journal_1000036164210410_a8b8.html
[16] 高根善, 张自力, 卢祖能. 高分辨磁共振成像在脑桥旁正中梗死患者中的诊断价值[J]. 卒中与神经疾病, 2020, 27(2): 171-174. doi: 10.3969/j.issn.1007-0478.2020.02.006 [17] 杨曼纯, 白小欣, 龙玉, 等. 高分辨核磁共振对脑桥梗死不同病灶形态类型的病因机制研究[J]. 中风与神经疾病杂志, 2019, 36(9): 794-797. https://www.cnki.com.cn/Article/CJFDTOTAL-ZFSJ201909006.htm [18] 钟丽玲, 宋建勋, 徐棣豪, 等. 不同类型急性孤立性脑桥梗死患者基底动脉的HR-VWI分析[J]. 中华神经医学杂志, 2021, 20(3): 275-281. doi: 10.3760/cma.j.cn115354-20200507-00340 -
期刊类型引用(10)
1. 方敏华. 三球式呼吸训练器训练应用于无创正压通气治疗慢性阻塞性肺疾病患者的效果分析. 基层医学论坛. 2024(11): 35-37 .  百度学术
百度学术
2. 许明璐,杨萧含,刘倩楠,尹畅. 老年人慢性病共病关联规则分析. 实用临床医药杂志. 2024(13): 103-108 .  本站查看
本站查看
3. 尹宁宁,王志娟,张海霞. 慢性阻塞性肺疾病患者并发心血管疾病危险因素及预测模型建立. 川北医学院学报. 2023(05): 608-612 .  百度学术
百度学术
4. 陈婷,陈丹凤,翁克姬. 负荷拓展呼吸训练联合血糖控制对慢阻肺合并高血压患者肺功能及血压控制效果的影响. 心血管病防治知识. 2023(18): 83-85 .  百度学术
百度学术
5. 黎玲,林丽芳. 自我管理对慢性阻塞性肺疾病合并高血压患者肺功能及生活质量的影响研究. 心血管病防治知识. 2023(22): 73-75 .  百度学术
百度学术
6. 曾丹虹. 多学科协作干预对AECOPD合并高血压患者肺功能的影响. 心血管病防治知识. 2023(25): 42-44 .  百度学术
百度学术
7. 陈春红. 自我管理对慢性阻塞性肺疾病合并高血压患者肺功能及生活质量的影响. 心血管病防治知识. 2022(06): 65-67 .  百度学术
百度学术
8. 陈芳,孙莲. 老年高血压伴慢性阻塞性肺疾病患者临床研究进展. 实用医院临床杂志. 2022(03): 229-231 .  百度学术
百度学术
9. 王龙龙,许淑娣,马洪鸽,马静文,王警建,杨淑涵,张明. 慢性阻塞性肺疾病合并抑郁患者的脑皮质边缘环路研究. 实用临床医药杂志. 2022(11): 38-41 .  本站查看
本站查看
10. 石婷婷,刘双全,高晓华,张锋英. 慢性阻塞性肺疾病合并社区获得性肺炎患者的临床特征及其影响因素分析. 医学信息. 2022(19): 38-42 .  百度学术
百度学术
其他类型引用(6)




 下载:
下载:
 苏公网安备 32100302010246号
苏公网安备 32100302010246号
