Study on potential markers protein for diagnosis of latent Mycobacterium tuberculosis infection
-
摘要:目的 比较结核分枝杆菌标准株与休眠株蛋白质组差异表达情况,探讨结核潜伏性感染相关的诊断标志物。方法 选取结核分枝杆菌标准株H37Rv和由标准株诱导的潜伏性感染菌株模型(休眠株)的样本,每个样本各培养3皿。对2组样本中的菌株进行裂解并抽提蛋白,进行同位素标记相对和绝对定量(iTRAQ)检测与分析,获得标准株与休眠菌株中相关蛋白质组的表达数据,并利用蛋白富集、信号通路分析等生物信息学技术将差异蛋白进行分类,进一步确定参与能量代谢通路的相关蛋白。结果 所检测的187个蛋白质中,64个蛋白质具有差异性表达,其中40个蛋白质表达上调,24个蛋白质表达下调。P9WPC9蛋白在休眠菌株与标准株中表达量比较,差异有统计学意义(P < 0.05)。结论 P9WPC9蛋白主要参与细菌的能量代谢通路,可能成为结核潜伏性感染的潜在诊断标志物。
-
关键词:
- 结核分枝杆菌 /
- 蛋白质组学 /
- 同位素标记相对和绝对定量 /
- 潜伏性感染 /
- 诊断标志物
Abstract:Objective To compare differential expression of proteome in standard Mycobacterium tuberculosis strains and dormant Mycobacterium tuberculosis strains so as to explore diagnostic markers related to latent Mycobacterium tuberculosis infection.Methods The samples of standard Mycobacterium tuberculosis H37Rv strain and latent Mycobacterium tuberculosis infection strain induced by standard strain (dormant strains) were selected, and each sample was cultured for three dishes. The strains of two sets of samples were cracked and proteins were extracted, isobaric tags for relative and absolute quantitation (iTRAQ) detection and quantitative analysis was performed, expression data of related proteome in standard strains and dormant strains were obtained, and bioinformatics techniques such as protein enrichment and signal pathway analysis were used to classify the differential proteins and further identify the related proteins involved in the energy metabolism pathway.Results A total of 64 proteins were differently expressed in the 187 detected proteins, of which 40 proteins were up-regulated and 24 proteins were down-regulated. Differently expressed proteins were mainly related to bacterial energy metabolism. P9WPC9 expression had a significant difference between dormant strains and standard strains.Conclusion P9WPC9 protein is mainly involved in the energy metabolism pathway of bacteria and may be a potential diagnostic marker for tuberculosis latent infection. -
膀胱癌是泌尿外科常见的恶性肿瘤,据全球癌症协会[1]统计, 2020年膀胱癌新发病例为57.3万例,死亡病例为21.2万例,其发病率和致死率均呈上升趋势。复发和转移是患者死亡的常见原因,研究膀胱癌增殖、转移的分子机制,寻找新的潜在治疗靶点,对膀胱癌的防治有重要意义。长链非编码RNA(lncRNA)是一类长度超过200个核苷酸的非编码RNA, 在细胞增殖、分化、蛋白修饰等方面发挥重要作用[2], 是近年来肿瘤学研究的热点。LINC02178是新近发现的lncRNA, 在多种肿瘤中异常表达。SUN Z L等[3]基于公共数据库分析发现, LINC02178可能参与膀胱癌细胞自噬,并与患者预后不良相关。本研究在公共数据库分析的基础上,结合分子生物学实验研究LINC02178对膀胱癌细胞增殖、侵袭和迁移的影响,并初步探讨其分子机制,现将结果报告如下。
1. 材料与方法
1.1 主要试剂
细胞系J82、T24、5637、SV-HUV-1均购自中国科学院上海细胞库; Trizol购自天根公司; TransStart®Green qPCR SuperMix购自北京全式金公司; LINC02178引物由上海生工公司合成; 胎牛血清购自Gibco公司; DMEM培养基购自Hyclone公司; Lipofectamine2000购自Invitrogen公司; Transwell小室购自Corning公司; siRNA-LINC02178和阴性对照系列由湖州河马生物公司设计合成,磷脂酰肌醇-3-激酶(PI3K)、蛋白激酶B(Akt)等抗体均购自北京安诺伦公司。
1.2 方法
1.2.1 LINC02178在公共数据库中的分析
在肿瘤与癌症基因组图谱(TCGA)数据库中下载414例膀胱癌患者的RNAseq和临床病理、生存数据。采用R语言的基础R包、ggplot2包分析LINC02178在膀胱癌中的表达及其与临床病理特征的关系。采用R语言的survival包分析LINC02178与膀胱癌患者生存预后的关系,并绘制生存曲线。
1.2.2 细胞培养和转染
膀胱癌细胞系T24、J82、5637和正常膀胱上皮细胞SV-HUV-1细胞采用含10%胎牛血清、1%青霉素-链霉素的DMEM培养基进行培养,培养条件为37 ℃、5%CO2的相对饱和湿度。取对数生存期的J82细胞,采用Lipofectamine2000将LINC02178干扰系列和阴性对照系列转染至细胞中,将细胞分为si-LINC02178组和si-NC组。
1.2.3 逆转录-实时定量聚合酶链反应(RT-qPCR) 检测LINC02178表达水平
取各膀胱癌细胞系及经不同处理的各组细胞(si-LINC02178组、si-NC组、T24、J82、5637、SV-HUV-1)培养48 h, 采用胰酶消化,提取总RNA, 检测纯度合格后,按照试剂盒说明书逆转录合成互补DNA(cDNA), -20 ℃保存备用。以cDNA为模板,进行实时荧光定量PCR, LINC02178上游引物为5′-GAGGGAGCCGAGGCAGTTTC-3′, 下游引物为5′-GAGGTCCTGTACCGAGGGGG-3′; GAPDH上游引物为5′-GCGGGGCCTCTCCAGAACATC-3′, 下游引物为5′-ACTGACACGTTGGCAGTGGG-3′; 反应条件为95 ℃下35 s预变性, 95 ℃变性10 s, 60 ℃延伸35 s, 扩增38个循环,采用2-△△Ct法计算相对表达量。
1.2.4 噻唑蓝(MTT)实验检测细胞增殖
将转染si-LINC02178组、si-NC组J82细胞继续培养48 h后,将细胞接种到96孔板中,待细胞贴壁后,各组细胞在0、24、48、72 h时,每孔加MTT溶液20 μL, 在培养箱中孵育4 h。采用酶标仪测定各孔光密度值(OD值),以时间为横坐标,以450 nm处OD值(OD450 nm)为纵坐标,绘制细胞生长曲线。
1.2.5 Transwell检测细胞迁移
取各组细胞培养48 h, 胰酶消化,离心收集细胞,换无血清培养基培养,制备单细胞悬液,密度为3×105个/mL。将300 μL调好密度的细胞悬液加入上室中,下室加500 μL全培养基,培养48 h, 采用4%多聚甲醛固定20 min, 棉签擦去上室中的细胞,结晶紫室温染色10 min, 冲洗掉多余染料, 100倍显微镜拍照,计算各孔穿过膜的细胞数量。
1.2.6 Transwell检测细胞侵袭
将基质胶适当稀释,平铺于上层小室,放入37 ℃培养箱中凝固,出现“白色层”后取出小室,其他步骤同1.2.5。
1.2.7 Western blot实验
si-LINC02178和si-NC组扩大培养,收集对数生长期细胞,采用RIPA缓冲液裂解细胞,提取蛋白,采用BCA试剂盒测定蛋白浓度,随后通过凝胶电泳分离后转至PVDF膜上; 采用浓度为5%的脱脂奶粉封闭2 h, 洗膜2次,加入一抗, 4 ℃孵育过夜; 再次洗膜3次后,加入二抗,室温孵育2 h后,化学发光法检测蛋白表达水平,以GAPDH为内参蛋白。
1.3 统计学方法
采用SPSS23.0和R3.6.3软件进行分析, GraphPad Prism7.0软件制图。采用Kaplan-Meier法分析LINC02178表达与膀胱癌生存预后的关系。计量资料采用均数±标准差表示,组间比较采用t检验,计数资料采用卡方检验, P < 0.05为差异有统计学意义。
2. 结果
2.1 LINC02178在膀胱癌组织中的表达及其与临床病理特征的关系
TCGA数据库分析结果显示, LINC02178在膀胱癌组织中的表达高于膀胱正常组织,差异有统计学意义(P < 0.05)。以中位数为临界值,分为LINC02178高表达和低表达患者,结果显示LINC02178表达与临床病理T分期相关(P < 0.05), 见表 1。生存分析显示, LINC02178高表达患者生存预后相较低表达患者更差,差异有统计学意义(P < 0.05)。见图 1。
表 1 LINC02178表达与临床病理特征关系临床病理特征 分类 n LINC02178低表达 LINC02178高表达 P 年龄 ≤70岁 234 115 119 0.766 >70岁 180 92 88 性别 女 109 63 46 0.074 男 305 144 161 分级 低级别 21 11 10 0.991 高级别 390 194 196 T分期 T1 5 5 0 0.008 T2 119 67 52 T3 196 95 101 T4 60 22 38 淋巴结转移 无 239 122 117 0.095 有 128 57 71 远处转移 无 202 104 98 0.936 有 11 5 6 2.2 LINC02178在膀胱癌细胞中的表达
LINC02178在膀胱癌细胞系J82、T24、5637中相对表达量分别为(2.13±0.01)、(1.84±0.03)、(1.73±0.04), 均高于SV-HUV-1细胞中的LINC02178表达量,差异有统计学意义(P < 0.05), 见图 2。因LINC02178在J82细胞中表达最高,故选用J82细胞进行下一步的研究。
2.3 转染后细胞中LINC02718的表达
转染后si-LINC02718组J82细胞LINC02718的表达量为(0.23±0.01), 低于si-NC组,差异有统计学意义(P < 0.05), 说明细胞中LINC02178的表达被有效抑制。见图 3。
2.4 沉默LINC02178对细胞增殖的影响
沉默LINC02178后, si-NC组48 h细胞活性OD值为(0.79±0.01), si-LINC02178组为(0.61± 0.02), 差异有统计学意义(P < 0.05); si-NC组72 h细胞活性OD值为(1.21±0.02), si-LINC02178组为(0.86±0.03), 差异有统计学意义(P < 0.05), 说明抑制LINC02178表达后,膀胱癌细胞增殖速度减慢。见图 4。
2.5 沉默LINC02178后对细胞侵袭的影响
Transwell结果显示, si-NC组侵袭细胞数为(179.30±4.26)个, si-LINC02178组为(91.33±2.02)个,差异有统计学意义(P < 0.05), 说明沉默LINC02178后细胞侵袭能力减弱。见图 5。
2.6 沉默LINC02178后对细胞迁移的影响
迁移实验显示, si-LINC02178组细胞迁移数目为(98.33±3.84)个, si-NC组为(196.30±2.73)个,差异有统计学意义(P < 0.05), 说明沉默LINC02178后细胞迁移能力下降。见图 6。
2.7 沉默LINC02178后对PI3K/Akt信号通路的影响
沉默LINC02178后, si-NC组和si-LINC02178组中PI3K、Akt蛋白的表达差异无统计学意义(P>0.05); si-LINC02178组中磷酸化PI3K(p-PI3K)、磷酸化Akt(p-Akt)蛋白的表达水平低于si-NC组,差异有统计学意义(P < 0.05)。见图 7。
3. 讨论
膀胱癌在泌尿系肿瘤中发病率高,其中75%为非肌层浸润膀胱癌, 25%为肌层浸润性膀胱癌[4-5]。膀胱根治性切除是肌层浸润性膀胱癌治疗的金标准,但有约50%的患者会出现局部复发或远处转移,发生转移的患者大部分在2年内死亡[6], 其主要原因是现有的化疗方案针对进展或转移的晚期膀胱癌患者的治疗效果有限,缺乏高效的靶向药物[7]。因此,寻找新型分子标志物,研究其进展、转移的分子机制,对改善膀胱癌的诊治方式以及降低死亡率有重要的意义。
研究[8]显示lncRNA是一类无编码蛋白质功能的RNA分子,但在机体中发挥重要的生物学功能,尤其是在肿瘤的发生、发展过程中[9]。多项研究[10-11]发现lncRNA能参与调控恶性肿瘤的增殖、转移、凋亡等生物学功能, lncRNA的异常表达与多种肿瘤的病理分期、预后相关,有望成为肿瘤诊断、预后及靶向治疗的新标志物[12-13]。研究[14]发现lncRNA UCA1表达上调可促进膀胱癌细胞增殖和迁移,对膀胱癌具有较高的临床辅助诊断价值,可作为膀胱癌预后不良的标志物[15-16]。研究[17]发现lncRNA H19在多种癌症中异常表达, H19表达失调可通过多种机制影响癌症生物学,被认为是癌症的生物标志物和潜在治疗靶点[18]。LINC02178是新近发现的非编码RNA,在肿瘤中的研究较少。PAN J F等[19]基于LUSC数据库构建肺癌预后相关的lncRNA风险模型,发现LINC02178可作为预测肺腺癌预后的标志物,指导患者的个体化治疗。SUN Z L等[3]利用TCGA数据库中膀胱癌患者数据进行分析,发现LINC02178与膀胱癌自噬相关,且与患者总生存期存在显著相关性。本研究基于TCGA数据库分析LINC02178在膀胱癌组织中的表达,发现LINC02178在膀胱癌组织中表达上调,与临床病理分期有关,生存分析也发现LINC02178高表达的患者生存预后更差。上述研究表明LINC02178在癌症的诊断和预后中有重要价值,但LINC02178在癌症中的作用仍缺乏相关实验研究。
本研究在生物信息学分析的基础上,采用qRT-PCR检测LINC02178在膀胱癌细胞中的表达水平,发现LINC02178在膀胱癌细胞T24、J82、5637中的表达量均显著高于膀胱正常上皮细胞; 同时,转染下调J82细胞中LINC02178的表达后, qRT-PCR检测结果显示si-LINC02178组细胞中LINC02178表达量显著低于si-NC组,说明转染干扰细胞后LINC02178表达被有效抑制; MTT细胞增殖试验显示, si-LINC02178组细胞在48、72 h的细胞活性显著低于si-NC组,说明沉默膀胱癌细胞LINC02178后可降低细胞增殖活性,提示LINC02178可能参与了膀胱癌细胞的增殖过程; Transwell检测显示, si-LINC02178组侵袭和迁移细胞数均显著低于si-NC组,说明沉默膀胱癌细胞LINC02178可抑制细胞的侵袭、迁移。PI3K/Akt是人体内重要的信号通路,与多种癌症的发生发展密切相关,涉及细胞增殖、分化、侵袭等多个调控环节。CHEN Y等[20]报道环状RNA_0000326可以通过海绵化miR-338-3p上调ETS1, 激活PI3K/Akt通路而促进膀胱癌细胞增殖和迁移。本研究发现下调LINC02178表达后, PI3K、Akt蛋白表达水平无明显改变,而p-PI3K、p-Akt表达显著下调,提示下调LINC02178可能通过抑制PI3K/Akt通路磷酸化来调控膀胱癌细胞的增殖和迁移。
综上所述, LINC02178在膀胱癌组织中高表达,与患者预后不良有关,沉默LINC02178后可抑制细胞增殖、侵袭和迁移,其机制可能是通过PI3K/Akt通路发挥作用。
-
表 1 样本分离信息及相关标记名称
样品编号 质谱同位素标签 dor 1 114 dor 2 115 sta 1 116 sta 2 117 表 2 质谱数据分析相关参数设置
酶切方式 漏切位点数 肽段最小长度氨基酸残基/个 肽段最大修饰数 First search一级母离子质量误差容忍度 Main search一级母离子质量误差容忍度 二级碎片离子的质量误差容忍度 Trypsin/P 2 7 2 20 ppm 5 ppm 0.02 Da 表 3 差异表达蛋白信息
样本比对名称及类型 上调占比/% 下调占比/% dor/sta 40.0 24.0 表 4 蛋白及相关通路信息
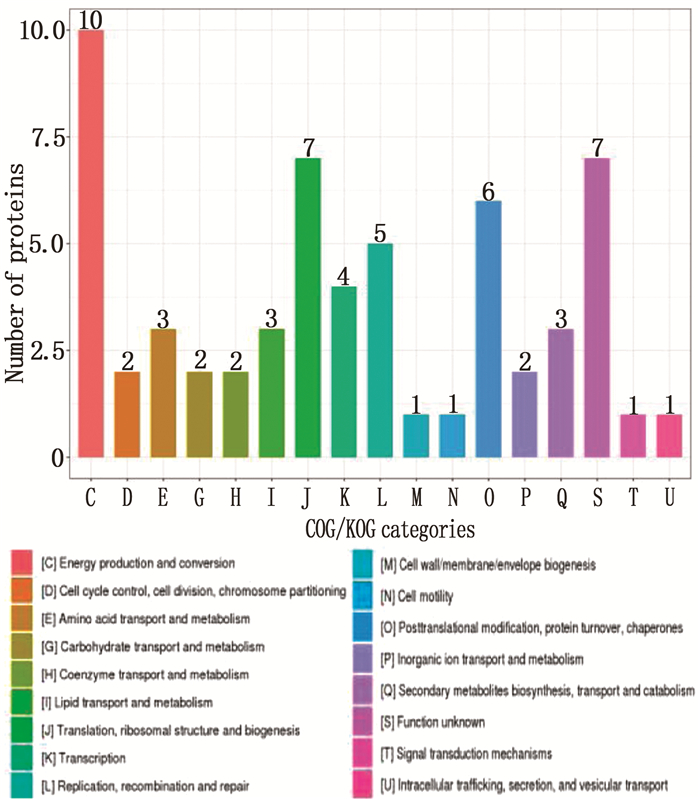
通路分类 蛋白名称 比例数值 上调及下调 变异系数 基因名称 蛋白长度 [J]Translation,ribosomal structure and biogenesis Q53538 4.752 5 Up 0.001 3677 rpsL 13.849 P9WHC7 2.422 Up 0.090 0083 rplA 24.756 P9WNU1 3.099 5 Up 0.065 0105 dnaN 42.113 P9WGD5 1.334 Up 0.029 2354 ssb 17.353 [T]Signal transduction mechanisms P9WHP5 1.33 Up 0.077 4436 Rv2744c 29.258 [M]Cell wall/membrane/envelope biogenesis P9WJC0 2.211 5 Up 0.000 6783 espK 73.909 [N]Cell motility P9WI01 1.463 Up 0.035 5434 PPE36 27.48 [U]Intracellular trafficking, secretion, and vesicular transport P9WGP1 1.847 5 Up 0.064 682 secD 60.266 [O]Posttranslational modification, protein turnover, chaperones P9WPD1 2.346 5 Up 0.033 8802 clpB 92.567 P9WPC9 2.197 5 Up 0.098 066 clpC1 93.551 P9WPB9 4.203 Up 0.021 4133 clpX 46.782 [C]Energy production and conversion P9WPV5 1.258 5 Up 0.058 4029 atpF 18.325 P9WK13 2.877 5 Up 0.050 5647 mdh 34.321 P9WIS7 1.619 Up 0.029 0303 dlaT 57.087 P9WP71 1.609 Up 0.093 8471 ctaD 63.672 O06159 1.212 5 Up 0.080 4124 bkdC 41.061 O53166 1.436 Up 0.091 922 acn 102.45 [G]Carbohydrate transport and metabolism P9WG25 1.349 Up 0.089 6961 tkt 75.588 -
[1] 朱小红, 胡颖君. 肺结核潜伏期和活动期外周血miR-29a和IFN-γ水平变化[J]. 现代诊断与治疗, 2019, 30(2): 302-303. https://www.cnki.com.cn/Article/CJFDTOTAL-XDZD201902062.htm [2] SANTOS-PEREIRA A, MAGALHES C, PMM ARAUJO, et al. Evolutionary Genetics of Mycobacterium tuberculosis and HIV-1: "The Tortoise and the Hare"[J]. Microorganisms, 2021, 9(1): 147. doi: 10.3390/microorganisms9010147
[3] LÓPEZ-AGUDELO V A, MENDUM T A, LAING E, et al. A systematic evaluation of Mycobacterium tuberculosis Genome-Scale Metabolic Networks[J]. PLoS Comput Biol, 2020, 16(6): e1007533. doi: 10.1371/journal.pcbi.1007533
[4] KANG W L, WANG G R, WU M Y, et al. Interferon-gamma release assay is not appropriate for the diagnosis of active tuberculosis in high-burden tuberculosis settings: a retrospective multicenter investigation[J]. Chin Med J: Engl, 2018, 131(3): 268-275. doi: 10.4103/0366-6999.223860
[5] 唐洁, 陈策, 查成, 等. 基于结核杆菌耐热抗原小分子多肽刺激人外周血T细胞产生TNF-α和IFN-γ鉴别肺结核和潜伏性结核感染[J]. 南方医科大学学报, 2017, 37(11): 1442-1447. doi: 10.3969/j.issn.1673-4254.2017.11.03 [6] XUAN W X, LU T T, WANG Z, et al. Diagnostic significance of Mycobacterium tuberculosis T-cell assays for active tuberculosis[J]. Chin Med J: Engl, 2017, 130(7): 811-816. doi: 10.4103/0366-6999.202738
[7] BOEHME C C, NABETA P, HENOSTROZA G, et al. Operational feasibility of using loop-mediated isothermal amplification for diagnosis of pulmonary tuberculosis in microscopy centers of developing countries[J]. J Clin Microbiol, 2007, 45(6): 1936-1940. doi: 10.1128/JCM.02352-06
[8] TORNHEIM J A, INTINI E, GUPTA A, et al. Clinical features associated with linezolid resistance among multidrug resistant tuberculosis patients at a tertiary care hospital in Mumbai, India[J]. J Clin Tuberc Other Mycobact Dis, 2020, 20: 100175. doi: 10.1016/j.jctube.2020.100175
[9] 陈晶, 张裕娴, 芮勇宇. γ干扰素释放试验在结核病诊断中的应用价值[J]. 中国感染与化疗杂志, 2020, 20(3): 255-258. https://www.cnki.com.cn/Article/CJFDTOTAL-KGHL202003004.htm [10] 张会强, 文政芳, 张冬杰, 等. IFN-γ及血清炎症因子水平变化与肺结核发病相关性及作用机制分析[J]. 中华医院感染学杂志, 2019, 29(2): 184-187. https://www.cnki.com.cn/Article/CJFDTOTAL-ZHYY201902006.htm [11] 莫胜林, 黄小红, 覃锦玉, 等. 艾滋病合并肺结核与单纯肺结核临床特征及胸部CT差异性研究[J]. 中国CT和MRI杂志, 2021, 19(4): 64-67. doi: 10.3969/j.issn.1672-5131.2021.04.021 [12] 陆恩词, 朱颖蔚. 肺结核合并糖尿病患者T淋巴细胞亚群及红细胞免疫功能的变化及意义[J]. 中国老年学杂志, 2017, 37(3): 648-649. doi: 10.3969/j.issn.1005-9202.2017.03.055 -
期刊类型引用(0)
其他类型引用(1)




 下载:
下载:







 苏公网安备 32100302010246号
苏公网安备 32100302010246号