Correlation between atherogenic index of plasma and diabetic retinopathy
-
摘要:目的
探讨血浆致动脉硬化指数(AIP)与糖尿病视网膜病变(DR)的相关性。
方法选取在徐州医科大学附属医院内分泌科住院的2型糖尿病患者445例为研究对象,根据DR诊断及分期标准将患者分为无DR(NDR)组188例、非增生型DR(NPDR)组134例、增生型DR(PDR)组123例。比较各组患者一般资料和主要生化指标,计算AIP。采用Logistic回归分析探讨发生DR的危险因素,采用Spearman相关性分析探讨AIP与各危险因素的相关性,采用受试者工作特征(ROC)曲线分析AIP筛查DR的价值。
结果PDR组的年龄大于NDR组和NPDR组,病程长于NDR组和NPDR组,空腹血糖(FBG)、糖化血红蛋白(HbA1c)、低密度脂蛋白胆固醇(LDL-C)、甘油三酯(TG)及AIP高于NDR组和NPDR组,估算肾小球滤过率(eGFR)水平低于NDR组和NPDR组,差异有统计学意义(P<0.05)。Logistic回归分析结果显示,年龄、病程、HbA1c、LDL-C、eGFR及AIP是T2DM患者发生DR的独立影响因素。T2DM患者AIP预测发生DR时的曲线下面积为0.745(95%CI为0.700~0.791)。应用AIP筛查DR的阈值为0.186, 灵敏度为74.3%, 特异度为64.4%。
结论AIP可能是T2DM患者DR筛查可靠的新指标。
Abstract:ObjectiveTo explore the correlation between atherogenic index of plasma(AIP) and diabetic retinopathy(DR).
MethodsA total of 445 patients with type 2 diabetes hospitalized in the Affiliated Hospital of Xuzhou Medical University were selected as study objects. According to DR diagnosis and staging criteria, the patients were divided into non-DR group (NDR group, n=188), nonproliferative group (NPDR group, n=134) and proliferative group (PDR group, n=123). The general information of patients and main biochemical indicators were collected. The general data and main biochemical indicators of patients in each group were compared, and AIP was calculated. The risk factors of DR were analyzed by Logistic regression, the correlations of AIP with risk factors were analyzed by Spearman correlation, and receiver operating characteristic (ROC) curve was used to analyze the value of AIP in screening DR.
ResultsAge in the PDR group was older, duration of diabetes in the PDR group was longer, the level of fasting blood glucose(FBG), glycosylated hemoglobin (HbA1c), low density lipoprotein cholesterol (LDL-C), triglyceride (TG) and AIP in the PDR group were significantly higher, and the level of estimated glomerular filtration (eGFR) were lower than those in the NDR group and NPDR group(P < 0.05). Logistic regression analysis showed that age, duration of diabetes, HbA1c, LDL-C, eGFR and AIP were independent influencing factors for DR in T2DM patients. The area under the curve of AIP in predicting DR in T2DM patients was 0.745 (95%CI, 0.700 to 0.791). The threshold of AIP for DR screening was 0.186, the sensitivity was 74.3%, and the specificity was 64.4%.
ConclusionAIP may be a reliable new indicator for DR screening in T2DM patients.
-
2型糖尿病(T2DM)导致的慢性并发症可造成多系统损害,已成为全球性公众健康问题[1]。糖尿病视网膜病变(DR)是最常见的慢性并发症之一,重度非增生型糖尿病视网膜病变(NPDR)、增生型糖尿病视网膜病变(PDR)和糖尿病性黄斑水肿(DME)等疾病均会损伤视力[2]。DR的早期筛查和诊断是预防疾病进展的重要措施,目前临床上对DR的筛查主要依靠眼底镜检查、眼底荧光造影、眼底照相等方法,但需要在综合性医疗机构由专业医务人员完成。因此临床上需要一种更加简便、可靠的生物学标志对DR进行早期筛查,减少DR导致的视力受损甚至失明。DOBIÁ SOVÁ M等[3]首次提出血浆致动脉硬化指数(AIP)的概念。AIP为血浆甘油三酯(TG)与高密度脂蛋白胆固醇(HDL-C)比值的对数。研究[4-5]提示,血管动脉粥样硬化的发生、发展与AIP密切相关。AIP也可能与肾病、骨质疏松等微血管病变有关,血脂异常同样是DR发生和发展的重要影响因素。本研究分析AIP水平与DR的相关性,探讨AIP对DR早期筛查的诊断价值,为DR的防治提供依据。
1. 资料与方法
1.1 一般资料
本研究选取2019年1月—2021年5月在徐州医科大学附属医院内分泌科住院的445例T2DM患者为研究对象,其中男272例,女173例,所有患者的诊断均符合1999年世界卫生组织糖尿病诊断分型标准。根据美国眼科学会2019年发布的《糖尿病视网膜病变(DR)国际临床分级标准》[6], 将患者分为无DR(NDR)组188例,非增生型DR(NPDR)组134例及增生型DR(PDR)组123例。排除标准: ① 1型糖尿病者; ②特殊类型糖尿病患者合并糖尿病急性并发症者; ③严重肾脏疾病、肝脏疾病者; ④急慢性心脑血管及感染性疾病者; ⑤血液系统疾病、恶性肿瘤者; ⑥合并白内障、急慢性青光眼、屈光不正等各种眼病者; ⑦妊娠期和哺乳期患者。本研究得到患者与家属同意,并通过医院伦理委员会审查。
1.2 方法
收集并记录各组研究对象的性别、年龄、病程、吸烟饮酒情况、身高、体质量、收缩压(SBP)、舒张压(DBP)等一般资料。计算体质量指数(BMI), BMI =体质量(kg)/身高2(m2)。所有研究对象均禁食8 h以上,于次日清晨采集右肘静脉血6 mL, 检测糖化血红蛋白(HbAlc)、谷丙转氨酶(ALT)、血肌酐(Scr)、血尿酸(SUA)、总胆红素(TBIL)、直接胆红素(DBIL)、总胆汁酸(TBA)、胱抑素C(CysC)和总胆固醇(TC)、甘油三酯(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、空腹血糖(FBG)水平。采用mCKD-EPI公式计算估算肾小球滤过率(eGFR), 女性Scr≤0.7 mg/dL, eGFR=151×(Scr/0.7)-0.328×(0.993)年龄; Scr >0.7 mg/dL, eGFR=151×(Scr/0.7)-1.210×(0.993)年龄。男性Scr≤0.9 mg/dL, eGFR=149×(Scr/0.9)-0.412×(0.993)年龄; Scr >0.9 mg/dL, eGFR=141×(Scr/0.9)-1.210×(0.993)年龄。计算AIP=log(TG/HDL-C)。所有患者均行散瞳眼底检查,由眼科专科医生依据散瞳眼底结果并根据美国眼科学会2019年发布的《糖尿病视网膜病变(DR)国际临床分级标准》[6]进行分级。NDR组无异常。NPDR组出现轻度、中度和重度患者。轻度: 仅有微动脉血管瘤; 中度: 不仅存在微动脉瘤,还存在轻于重度的NPDR表现; 重度: 出现下列任何1种表现,但尚无PDR。① 4个象限中,均20处以上出现出血; ② 2个以上象限出现串珠样改变(静脉); ③ 1个以上象限中有显著微血管异常变化。PDR组患者出现视网膜血管新生、视网膜前出血或玻璃体可见积血中的1种或多种体征。
1.3 统计学处理
采用SPSS 26.0软件对数据进行统计学分析。计数资料以[n(%)]表示,采用χ2检验。符合正态分布的数据采用(x±s)表示,组间比较采用单因素方差分析,进一步采用LSD法进行两两比较。非正态分布的数据以中位数(四分位数)表示,组间比较采用Kruskal-Wallis H检验,进一步采用Nemenyi法进行两两比较。采用Spearman相关性分析探讨AIP与各指标的相关性。DR的危险因素采用多因素Logistic回归分析进行探讨。应用受试者工作特征(ROC)曲线评价AIP诊断DR的价值。P<0.05为差异有统计学意义。
2. 结果
2.1 患者临床指标水平比较
与NDR组比较, NPDR组患者的年龄增大,病程延长, HbA1c、FBG、CysC、TG、LDL-C、AIP水平升高, TBIL、HDL-C、eGFR水平下降,差异有统计学意义(P<0.05)。与NDR组比较, PDR组患者的年龄增大,病程延长, HbA1c、FBG、Scr、CysC、TG、LDL-C、AIP水平升高, TBIL、HDL-C、eGFR水平下降,差异有统计学意义(P<0.05)。与NPDR组比较, PDR组患者的年龄增大,病程延长, HbA1c、FBG、Scr、TG、LDL-C、AIP水平升高, eGFR水平下降,差异有统计学意义(P<0.05)。见表 1。
表 1 各组患者临床指标水平比较(x±s)[n(%)]临床指标 NDR组(n=188) NPDR组(n=134) PDR组(n=123) F/χ2 P 男 118(62.77) 84(62.69) 70(56.91) 1.27 0.530 女 70(23.23) 50(37.31) 53(43.09) 年龄/岁 46.56±10.86 54.52±9.83* 63.85±10.75*# 100.75 <0.001 病程/年 2(1, 50) 8(3, 12)* 15(10, 20)*# 162.83 <0.001 BMI/(kg/m2) 25.10±3.12 25.46±3.56 25.66±3.70 1.11 0.330 高血压 56(29.80) 35(26.10) 44(35.80) 2.87 0.240 吸烟 48(25.50) 22(16.40) 33(26.80) 4.95 0.090 饮酒 31(16.50) 29(21.60) 17(13.80) 2.89 0.240 SBP/mmHg 128.93±12.81 130.08±17.03 133.02±19.92 2.38 0.090 DBP/mmHg 81.85±9.33 81.45±10.36 81.98±11.65 0.10 0.910 HbA1c/% 7.98±2.20 8.65±2.11* 9.38±2.09*# 15.98 <0.001 FBG/(mmol/L) 8.35±2.62 9.21±3.23* 10.10±3.19*# 12.95 <0.001 ALT/(U/L) 19.00(14.00, 28.00) 18.50(14.00, 26.00) 18.00(13.00, 26.00) 1.65 0.450 TBIL/(μmol/L) 11.80(9.00, 15.10) 10.30(7.95, 14.03)* 9.70(7.00, 12.90)* 17.48 <0.001 DBIL/(μmol/L) 3.84±1.40 3.91±1.68 3.67±1.36 0.86 0.420 TBA/(μmol/L) 3.40(2.03, 5) 3.90(2.40, 5.10) 3.50(2.20, 5.90) 2.64 0.270 UREA/(mmol/L) 5.61±1.49 5.66±1.86 6.03±2.52 1.96 0.140 Scr/(μmol/L) 56(48, 65) 58(50, 69) 65(56, 90) *# 35.77 <0.001 UA/(μmol/L) 288.32±75.81 296.31±88.92 296.13±88.61 0.49 0.615 CysC/(mg/L) 0.73±0.14 0.89±0.43* 0.96±0.38* 20.58 <0.001 TC/(mmol/lL) 5.09±1.09 5.11±1.29 5.24±1.52 0.55 0.580 TG(mmol/L) 1.47(1.13, 1.89) 1.96(1.40, 2.81) * 2.36(1.88, 3.00) *# 77.93 <0.001 HDL-C/(mmol/L) 1.20±0.33 1.07±0.27* 1.01±0.33* 14.50 <0.001 LDL-C/(mmol/L) 2.67±0.83 3.02±1.10* 3.34±1.47*# 13.25 <0.001 eGFR 120.88±22.60 106.49±28.74* 83.63±33.61*# 66.42 <0.001 AIP 0.11(-0.05, 0.27) 0.26(0.14, 0.49)* 0.39(0.25, 0.56)*# 89.06 <0.001 BMI: 体质量指数; SBP: 收缩压; DBP: 舒张压; HbA1c: 糖化血红蛋白; FBG: 空腹血糖; ALT: 谷丙转氨酶; TBIL: 总胆红素;
DBIL: 直接胆红素; TBA: 总胆汁酸; UREA: 尿素; Scr: 肌酐; UA: 尿酸; CysC: 胱抑素C; TC: 总胆固醇; TG: 甘油三酯;
HDL-C: 高密度脂蛋白胆固醇; LDL-C: 低密度脂蛋白胆固醇; eGFR: 估算肾小球滤过率; AIP: 血浆致动脉硬化指数。
与NDR组比较, * P<0.05; 与NPDR组比较, #P<0.05。2.2 T2DM患者发生DR的危险因素
以是否发生DR为因变量,以年龄、病程、HbA1c、FBG、TBIL、Scr、CysC、LDL-C、eGFR、AIP水平为自变量,采用条件向前法建立Logistic回归模型。结果显示,年龄、病程、HbA1c、LDL-C、eGFR、AIP在模型中差异均有统计学意义(P<0.05)。病程、HbA1c、LDL-C、AIP与DR的发生呈正相关(P<0.05), eGFR与DR的发生呈负相关(P<0.05), 见表 2。
表 2 T2DM患者发生DR的影响因素多元Logistic回归分析因素 B SE Wald χ2 P OR(95%CI) 年龄 0.043 0.016 7.674 0.006 1.044(1.013~1.076) 病程 0.212 0.034 39.870 <0.001 1.236(1.157~1.32) HbA1c 0.149 0.064 5.347 0.021 1.161(1.023~1.317) LDL-C 0.326 0.151 4.633 0.031 1.385(1.030~1.862) eGFR -0.022 0.006 12.389 <0.001 0.978(0.966~0.990) AIP 0.341 0.054 40.152 <0.001 1.406(1.266~1.563) 常量 -3.737 1.301 8.252 0.004 — HbA1c: 糖化血红蛋白; LDL-C: 低密度脂蛋白胆固醇; eGFR: 估算的肾小球滤过率; AIP: 血浆致动脉硬化指数。 2.3 AIP对DR的诊断价值
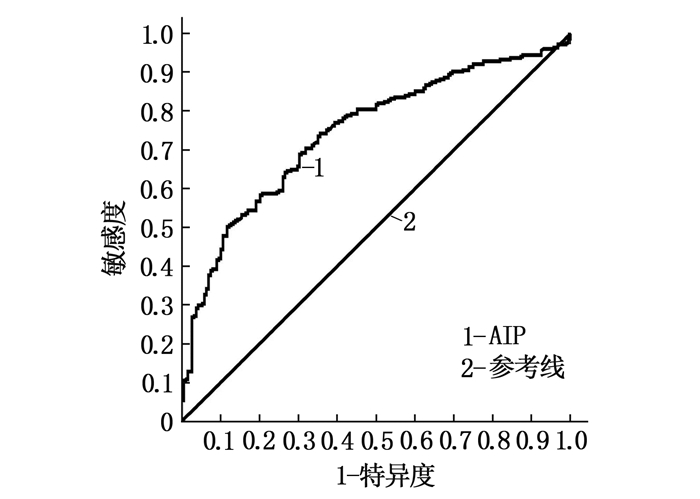
ROC曲线显示, T2DM患者AIP预测发生DR的曲线下面积(AUC)为0.745, AIP诊断DR的阈值为0.186, 敏感度为74.3%, 特异度为64.4%, 见图 1。
3. 讨论
DR是最常见的糖尿病慢性并发症之一,尽管高血糖是DR典型的危险因素,但研究[7]显示,良好的血糖控制不能完全预防DR的发生与进展。本研究发现,除年龄、病程、HbA1c、eGFR等已经被其他研究证实的DR危险因素外,血脂指标AIP、LDL-C同样为DR发生的独立危险因素,血脂紊乱可能参与了DR的发生和发展。为明确AIP对DR的诊断价值,本研究进一步应用ROC曲线进行分析,结果发现, AIP预测DR发生的AUC为0.745。AIP诊断DR的阈值为0.186, 对应的灵敏度为74.3%, 特异度为64.4%。AIP可作为一项简便、有效的DR早期筛查指标。
AIP是指TG与HDL-C浓度比值的对数,与低密度脂蛋白(LDL)颗粒直径呈负相关[8], 而LDL-C与动脉粥样硬化病变有显著相关性。因此,美国国家胆固醇教育计划建议将AIP作为预测心血管事件的可靠危险因素[9]。AIP与T2DM患者的主要不良心血管事件相关[10], 也是T2DM患者发生冠心病的一个强力预测因子[11-12]。赵洁等[13]研究发现,AIP还可以反映LDL不同亚型与不同类型冠心病的相关性。在微血管并发症方面, AKBAS E M等[14]发现, T2DM患者的AIP水平随着尿蛋白水平的增高而升高。ZHOU Y P等[4]发现,AIP水平与T2DM患者eGFR水平呈负相关。目前尚无AIP与DR相关性的报道,但已有研究提示血脂紊乱参与了DR的发生与进展。新加坡马来眼科研究(SMES)[15]报告显示,高LDL-C与DR存在相关性,这与本研究中LDL-C是DR的独立危险因素一致。RELHAN N等[16]研究发现, LDL-C对DR的进展影响很大,同时发现TG与DR的发生与发展密切相关。另一项研究[17]也显示, TG控制不佳与PDR的进展有关,未发现HDL-C、LDL-C与DR显著相关。本研究发现,除病程和血糖外, AIP、LDL-C也是DR的独立危险因素,提示除长期的高血糖外,脂代谢紊乱也参与了DR的病理生理过程, DR患者外周血AIP水平较NDR患者人群显著增高,进一步分析发现,PDR患者AIP水平较NPDR患者升高, AIP水平的升高可能与DR的进展有关。AIP可更好地反映血脂紊乱对DR的影响。目前血脂紊乱导致DR的机制仍不明确, TG可能进入细胞膜导致膜流动性发生变化以及富含TG的脂蛋白激活血液单核细胞发挥促炎作用[18-19], 进而造成血视网膜屏障(BRB)破坏和血流动力学指标异常,随着时间的推移,视网膜缺血的区域逐渐扩大,继而出现视网膜内微血管异常,导致新生血管形成或增生性DR。HDL-C可能通过抑制LDL-C的氧化和巨噬细胞的迁移而表现出抗炎、抗氧化作用[20-21], 能够减轻对视网膜的损伤。
本研究尚存在一定的局限性: ①本项目为回顾性研究,纳入的人群可能存在偏倚; ②受研究时间限制,本研究纳入的样本量较少,可能导致AIP对DR的筛查价值判断产生一定差异,未来将扩大样本量,同时进行前瞻性队列试验来进一步验证本研究结论。
综上所述, AIP水平与T2DM患者发生DR密切相关,且AIP水平与糖尿病病程、糖脂代谢紊乱等密切相关,能够反映DR发生和发展的多种危险因素,可能是早期筛查DR的一项简便、有效的指标,未来尚需进一步深入进行基础研究,以进一步明确AIP参与DR发生和发展的具体机制。
-
表 1 各组患者临床指标水平比较(x±s)[n(%)]
临床指标 NDR组(n=188) NPDR组(n=134) PDR组(n=123) F/χ2 P 男 118(62.77) 84(62.69) 70(56.91) 1.27 0.530 女 70(23.23) 50(37.31) 53(43.09) 年龄/岁 46.56±10.86 54.52±9.83* 63.85±10.75*# 100.75 <0.001 病程/年 2(1, 50) 8(3, 12)* 15(10, 20)*# 162.83 <0.001 BMI/(kg/m2) 25.10±3.12 25.46±3.56 25.66±3.70 1.11 0.330 高血压 56(29.80) 35(26.10) 44(35.80) 2.87 0.240 吸烟 48(25.50) 22(16.40) 33(26.80) 4.95 0.090 饮酒 31(16.50) 29(21.60) 17(13.80) 2.89 0.240 SBP/mmHg 128.93±12.81 130.08±17.03 133.02±19.92 2.38 0.090 DBP/mmHg 81.85±9.33 81.45±10.36 81.98±11.65 0.10 0.910 HbA1c/% 7.98±2.20 8.65±2.11* 9.38±2.09*# 15.98 <0.001 FBG/(mmol/L) 8.35±2.62 9.21±3.23* 10.10±3.19*# 12.95 <0.001 ALT/(U/L) 19.00(14.00, 28.00) 18.50(14.00, 26.00) 18.00(13.00, 26.00) 1.65 0.450 TBIL/(μmol/L) 11.80(9.00, 15.10) 10.30(7.95, 14.03)* 9.70(7.00, 12.90)* 17.48 <0.001 DBIL/(μmol/L) 3.84±1.40 3.91±1.68 3.67±1.36 0.86 0.420 TBA/(μmol/L) 3.40(2.03, 5) 3.90(2.40, 5.10) 3.50(2.20, 5.90) 2.64 0.270 UREA/(mmol/L) 5.61±1.49 5.66±1.86 6.03±2.52 1.96 0.140 Scr/(μmol/L) 56(48, 65) 58(50, 69) 65(56, 90) *# 35.77 <0.001 UA/(μmol/L) 288.32±75.81 296.31±88.92 296.13±88.61 0.49 0.615 CysC/(mg/L) 0.73±0.14 0.89±0.43* 0.96±0.38* 20.58 <0.001 TC/(mmol/lL) 5.09±1.09 5.11±1.29 5.24±1.52 0.55 0.580 TG(mmol/L) 1.47(1.13, 1.89) 1.96(1.40, 2.81) * 2.36(1.88, 3.00) *# 77.93 <0.001 HDL-C/(mmol/L) 1.20±0.33 1.07±0.27* 1.01±0.33* 14.50 <0.001 LDL-C/(mmol/L) 2.67±0.83 3.02±1.10* 3.34±1.47*# 13.25 <0.001 eGFR 120.88±22.60 106.49±28.74* 83.63±33.61*# 66.42 <0.001 AIP 0.11(-0.05, 0.27) 0.26(0.14, 0.49)* 0.39(0.25, 0.56)*# 89.06 <0.001 BMI: 体质量指数; SBP: 收缩压; DBP: 舒张压; HbA1c: 糖化血红蛋白; FBG: 空腹血糖; ALT: 谷丙转氨酶; TBIL: 总胆红素;
DBIL: 直接胆红素; TBA: 总胆汁酸; UREA: 尿素; Scr: 肌酐; UA: 尿酸; CysC: 胱抑素C; TC: 总胆固醇; TG: 甘油三酯;
HDL-C: 高密度脂蛋白胆固醇; LDL-C: 低密度脂蛋白胆固醇; eGFR: 估算肾小球滤过率; AIP: 血浆致动脉硬化指数。
与NDR组比较, * P<0.05; 与NPDR组比较, #P<0.05。表 2 T2DM患者发生DR的影响因素多元Logistic回归分析
因素 B SE Wald χ2 P OR(95%CI) 年龄 0.043 0.016 7.674 0.006 1.044(1.013~1.076) 病程 0.212 0.034 39.870 <0.001 1.236(1.157~1.32) HbA1c 0.149 0.064 5.347 0.021 1.161(1.023~1.317) LDL-C 0.326 0.151 4.633 0.031 1.385(1.030~1.862) eGFR -0.022 0.006 12.389 <0.001 0.978(0.966~0.990) AIP 0.341 0.054 40.152 <0.001 1.406(1.266~1.563) 常量 -3.737 1.301 8.252 0.004 — HbA1c: 糖化血红蛋白; LDL-C: 低密度脂蛋白胆固醇; eGFR: 估算的肾小球滤过率; AIP: 血浆致动脉硬化指数。 -
[1] LI Y Z, TENG D, SHI X G, et al. Prevalence of diabetes recorded in mainland China using 2018 diagnostic criteria from the American Diabetes Association: national cross sectional study[J]. BMJ, 2020, 369: m997.
[2] TEO Z L, THAM Y C, YU M, et al. Global prevalence of diabetic retinopathy and projection of burden through 2045: systematic review and meta-analysis[J]. Ophthalmology, 2021, 128(11): 1580-1591. doi: 10.1016/j.ophtha.2021.04.027
[3] DOBIÁSOVÁ M, RASLOVÁK, RAUCHOVÁH, et al. Atherogenic lipoprotein profile in families with and without history of early myocardial infarction[J]. Physiol Res, 2001, 50(1): 1-8.
[4] ZHOU Y P, SHANG X L. Usefulness of atherogenic index of plasma for estimating reduced eGFR risk: insights from the national health and nutrition examination survey[J]. Postgrad Med, 2021, 133(3): 278-285. doi: 10.1080/00325481.2020.1838138
[5] HERNÁNDEZ J L, OLMOS J M, PARIENTE E, et al. The atherogenic index of plasma is related to a degraded bone microarchitecture assessed by the trabecular bone score in postmenopausal women: the Camargo Cohort Study[J]. Maturitas, 2021, 148: 1-6. doi: 10.1016/j.maturitas.2021.03.008
[6] FLAXEL C J, ADELMAN R A, BAILEY S T, et al. Diabetic retinopathy preferred practice pattern[J]. Ophthalmology, 2020, 127(1): P66-P145. doi: 10.1016/j.ophtha.2019.09.025
[7] ISMAIL-BEIGI F, CRAVEN T, BANERJI M A, et al. Effect of intensive treatment of hyperglycaemia on microvascular outcomes in type 2 diabetes: an analysis of the ACCORD randomised trial[J]. Lancet, 2010, 376(9739): 419-430. doi: 10.1016/S0140-6736(10)60576-4
[8] ONAT A, CAN G, KAYA H S, et al. "Atherogenic index of plasma" (log10 triglyceride/high-density lipoprotein-cholesterol) predicts high blood pressure, diabetes, and vascular events[J]. J Clin Lipidol, 2010, 4(2): 89-98. doi: 10.1016/j.jacl.2010.02.005
[9] NATIONAL CHOLESTEROL EDUCATION PROGRAM (NCEP) EXPERT PANEL ON DETECTION E. Third Report of the National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel Ⅲ) final report[J]. Circulation, 2002, 106(25): 3143-3421. doi: 10.1161/circ.106.25.3143
[10] FU L Y, ZHOU Y, SUN J X, et al. Atherogenic index of plasma is associated with major adverse cardiovascular events in patients with type 2 diabetes mellitus[J]. Cardiovasc Diabetol, 2021, 20(1): 201. doi: 10.1186/s12933-021-01393-5
[11] 张倩倩, 时涵远, 李馨航, 等. 甘油三酯-葡萄糖指数和血浆致动脉硬化指数评价冠心病的临床价值[J]. 天津医科大学学报, 2022, 28(1): 73-76. https://www.cnki.com.cn/Article/CJFDTOTAL-TJYK202201016.htm [12] QIN Z, ZHOU K, LI Y P, et al. The atherogenic index of plasma plays an important role in predicting the prognosis of type 2 diabetic subjects undergoing percutaneous coronary intervention: results from an observational cohort study in China[J]. Cardiovasc Diabetol, 2020, 19(1): 23. doi: 10.1186/s12933-020-0989-8
[13] 赵洁, 李淑英, 张英, 等. 中青年和老年冠心病患者LDL不同亚型与AIP的相关性分析[J]. 天津医药, 2021, 49(1): 54-58. https://www.cnki.com.cn/Article/CJFDTOTAL-TJYZ202101013.htm [14] AKBAS E M, TIMUROGLU A, OZCICEK A, et al. Association of uric acid, atherogenic index of plasma and albuminuria in diabetes mellitus[J]. Int J Clin Exp Med, 2014, 7(12): 5737-5743.
[15] WONG T Y, CHEUNG N, TAY W T, et al. Prevalence and risk factors for diabetic retinopathy: the Singapore Malay Eye Study[J]. Ophthalmology, 2008, 115(11): 1869-1875. doi: 10.1016/j.ophtha.2008.05.014
[16] RELHAN N, FLYNN H W Jr. The Early Treatment Diabetic Retinopathy Study historical review and relevance to today's management of diabetic macular edema[J]. Curr Opin Ophthalmol, 2017, 28(3): 205-212. doi: 10.1097/ICU.0000000000000362
[17] SRINIVASAN S, RAMAN R, KULOTHUNGAN V, et al. Influence of serum lipids on the incidence and progression of diabetic retinopathy and macular oedema: Sankara Nethralaya Diabetic Retinopathy Epidemiology And Molecular genetics Study-Ⅱ[J]. Clin Exp Ophthalmol, 2017, 45(9): 894-900. doi: 10.1111/ceo.12990
[18] EBELING P, KOIVISTO V A. Occurrence and interrelationships of complications in insulin-dependent diabetes in Finland[J]. Acta Diabetol, 1997, 34(1): 33-38. doi: 10.1007/s005920050062
[19] KANTER J E, HSU C C, BORNFELDT K E. Monocytes and macrophages as protagonists in vascular complications of diabetes[J]. Front Cardiovasc Med, 2020, 7: 10. doi: 10.3389/fcvm.2020.00010
[20] CANPOLAT A G, EMRAL R, KESKIN Ç, et al. Association of monocyte-to-high density lipoprotein-cholesterol ratio with peripheral neuropathy in patients with Type Ⅱdiabetes mellitus[J]. Biomark Med, 2019, 13(11): 907-915. doi: 10.2217/bmm-2018-0451
[21] ROLIN J, MAGHAZACHI A A. Implications of chemokines, chemokine receptors, and inflammatory lipids in atherosclerosis[J]. J Leukoc Biol, 2014, 95(4): 575-585. doi: 10.1189/jlb.1113571
-
期刊类型引用(4)
1. 张洋洋,谭丽艳,南晓利,柳扬. 血脂相关指标与糖尿病视网膜病变的相关研究进展. 中国医药科学. 2024(19): 32-35 .  百度学术
百度学术
2. 王灵悦. 眼动脉超声血流参数诊断T2DM合并视网膜病变及对病变程度的评估价值. 实用临床医学. 2024(06): 59-63 .  百度学术
百度学术
3. 柏旭,苏洁,李凤,徐倩,沈源,肖凌凤. 我国成人糖尿病视网膜病变影响因素的Meta分析. 预防医学. 2023(07): 595-601 .  百度学术
百度学术
4. 郭婧,李芸云,刘思思,沙颖,马凯,王红. 糖尿病视网膜病变不同分期患者血清δ样蛋白4和环磷腺苷效应元件结合蛋白水平对微血管损伤的预测价值. 实用临床医药杂志. 2023(23): 68-72+78 .  本站查看
本站查看
其他类型引用(1)




 下载:
下载:
 苏公网安备 32100302010246号
苏公网安备 32100302010246号