Analysis in pathogenic bacteria distribution and risk factors of nosocomial infection in patients with extracorporeal membrane oxygenation
-
摘要:目的
分析体外膜肺氧合(ECMO)患者医院感染病原菌分布及危险因素。
方法分析76例接受ECMO治疗患者的临床资料, 分为感染组与非感染组。分析2组患者感染情况及其危险因素、检出病原菌分布及其耐药性,采用受试者工作特征(ROC)曲线分析ECMO术后医院感染的危险因素。
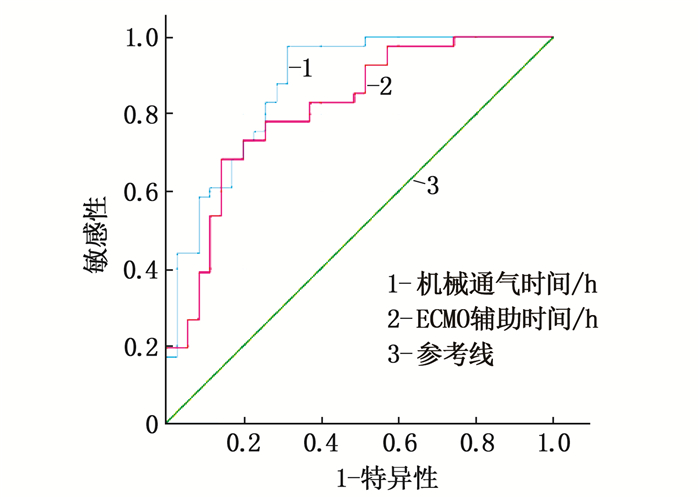
结果76例患者医院感染发生率为53.95%(41/76), 下呼吸道(76.12%)为主要感染部位,革兰氏阴性杆菌检出率最高(85.07%)。2组患者在年龄、机械通气时间、ECMO辅助时间、抗菌药使用时间、中心静脉置管时间、导尿管置管时间方面比较,差异有统计学意义(P<0.05或P<0.01)。Logistic回归分析显示, ECMO辅助时间、机械通气时间是发生医院感染的独立危险因素(P<0.05)。ROC曲线分析显示, ECMO辅助时间预测ECMO后医院感染的曲线下面积(AUC)为0.812, 最佳临界值为128.04 h, 敏感性为68.3%, 特异性为85.7%;机械通气时间预测ECMO后医院感染的AUC为0.873, 最佳临界值为64.48 h, 敏感性为97.6%, 特异性为68.6%。
结论ECMO术后医院感染率较高,下呼吸道为主要感染部位,病原菌多为革兰氏阴性杆菌,多重耐药菌比例高,机械通气时间和ECMO辅助时间是发生医院感染的独立危险因素。
Abstract:ObjectiveTo analyze the pathogenic bacteria distribution and risk factors of nosocomial infection in patients with extracorporeal membrane oxygenation (ECMO).
MethodsClinical materials of 76 patients with ECMO were analyzed, and they were divided into infection group and non-infection group. The infection situation and its risk factors as well as the distribution of detected pathogenic bacteria and their drug resistance were analyzed, and the risk factors of nosocomial infection after ECMO were analyzed by receiver operating characteristic (ROC) curve.
ResultsThe incidence of nosocomial infection in 76 patients was 53.95% (41/76), lower respiratory tract (76.12%) was the main infection site, and the detection rate of Gram-negative bacilli was the highest (85.07%). There were significant differences in age, mechanical ventilation time, ECMO assisted time, antibacterial drug use time, central venous catheterization time and catheter catheterization time between the two groups (P < 0.05 or P < 0.01). Logistic regression analysis showed that ECMO assisted time and mechanical ventilation time were the independent risk factors for nosocomial infection (P < 0.05). ROC curve analysis showed that the area under the curve (AUC) of ECMO assisted time to predict nosocomial infection after ECMO was 0.812, the best critical value was 128.04 h, the sensitivity was 68.3%, and the specificity was 85.7%; the AUC of mechanical ventilation time in predicting nosocomial infection after ECMO was 0.873, the best critical value was 64.48 h, the sensitivity was 97.6%, and the specificity was 68.6%.
ConclusionThe nosocomial infection rate after ECMO is high, the lower respiratory tract is the main infection site, and most of pathogenic bacteria are Gram-negative bacteria, the proportion of multidrug-resistant bacteria is high, and mechanical ventilation time and ECMO assisted time are the independent risk factors for nosocomial infection.
-
-
表 1 ECMO术后医院感染病原菌分布及构成比(n=67)[n(%)]
病原菌 下呼吸道 血液 泌尿道 消化道 皮肤软组织 胸膜腔 合计 革兰氏阴性杆菌 47(70.15) 5(7.46) 2(2.99) 0 2(2.99) 1(1.49) 57(85.07) 鲍曼不动杆菌 19(28.36) 1(1.49) 0 0 0 1(1.49) 21(31.34) 肺炎克雷伯菌 9(13.43) 1(1.49) 0 0 0 0 10(14.93) 铜绿假单胞菌 5(7.46) 0 0 0 1(1.49) 0 6(8.96) 嗜麦芽窄食单胞菌 5(7.46) 1(1.49) 0 0 0 0 6(8.96) 产气肠杆菌 3(4.48) 0 0 0 0 0 3(4.48) 洋葱伯克霍尔德菌 2(2.99) 0 0 0 0 0 2(2.99) 阴沟肠杆菌 1(1.49) 0 0 0 0 0 1(1.49) 奇异变形杆菌 1(1.49) 0 0 0 0 0 1(1.49) 大肠埃希菌 0 2(2.99) 2(2.99) 0 1(1.49) 0 5(7.46) 其他革兰氏阴性杆菌 2(2.99) 0 0 0 0 0 2(2.99) 革兰氏阳性球菌 1(1.49) 4(5.97) 1(1.49) 0 0 0 6(8.96) 溶血葡萄球菌 0 1(1.49) 0 0 0 0 1(1.49) 金黄色葡萄球菌 1(1.49) 0 0 0 0 0 1(1.49) 表皮葡萄球菌 0 2(2.99) 0 0 0 0 2(2.99) 屎肠球菌 0 0 1(1.49) 0 0 0 1(1.49) 粪肠球菌 0(1.49) 1(1.49) 0 0 0 0 1(1.49) 真菌 3(4.48) 0 1(1.49) 0 0 0 4(5.97) 白念珠菌 2(2.99) 0 1(1.49) 0 0 0 3(4.48) 曲霉菌 1(1.49) 0 0 0 0 0 1(1.49) 合计 51(76.12) 9(13.43) 4(5.97) 0 2(2.99) 1(1.49) 67(100.00) 表 2 主要革兰氏阴性菌对抗菌药物的耐药率
抗菌药物 鲍曼不动杆菌(n=19) 肺炎克雷伯菌(n=9) 铜绿假单胞菌(n=5) 耐药菌株数/株 耐药率/% 耐药菌株数/株 耐药率/% 耐药菌株数/株 耐药率/% 复方新诺明 12 63.16 6 66.67 3 60.00 氨曲南 16 84.21 7 77.78 4 80.00 头孢哌酮/舒巴坦 16 84.21 8 88.89 3 60.00 头孢替坦 15 78.95 5 55.56 4 80.00 头孢吡肟 13 68.42 6 66.67 3 60.00 亚胺培南 14 73.68 6 66.67 4 80.00 左旋氧氟沙星 14 73.68 5 55.56 3 60.00 美罗培南 13 68.42 7 77.78 3 60.00 米诺环素 19 100.00 6 66.67 3 60.00 哌拉西林 19 100.00 9 100.00 4 80.00 头孢呋辛 16 84.21 8 88.89 4 80.00 头孢唑肟 13 68.42 7 77.78 3 60.00 头孢他啶 13 68.42 6 66.67 3 60.00 替卡西林 19 100.00 9 100.00 3 60.00 哌拉西林/他唑巴坦 17 89.47 9 100.00 4 80.00 头孢噻肟 14 73.68 7 77.78 3 60.00 莫西沙星 12 63.16 6 66.67 3 60.00 替加环素 13 68.42 1 11.11 3 60.00 阿米卡星 11 57.89 4 44.44 2 40.00 头孢呋辛酯 15 78.95 7 77.78 4 80.00 表 3 主要革兰氏阳性菌对抗菌药物的耐药率
革兰氏阳性菌 耐药情况 氯霉素 红霉素 青霉素 左旋氧氟沙星 苯唑西林 庆大霉素 万古霉素 克林霉素 利奈唑胺 表皮葡萄球菌(n=2) 耐药菌株数/株 2 1 2 2 1 1 0 1 2 耐药率/% 100.00 50.00 100.00 100.00 50.00 50.00 0 50.00 100.00 金黄色葡萄球菌(n=1) 耐药菌株数/株 1 1 1 0 1 1 0 1 0 耐药率/% 100.00 100.00 100.00 0 100.00 100.00 0 100.00 0 溶血葡萄球菌(n=1) 耐药菌株数/株 1 1 1 1 1 1 0 0 0 耐药率/% 100.00 100.00 100.00 100.00 100.00 100.00 0 0 0 粪肠球菌(n=1) 耐药菌株数/株 1 0 1 0 0 0 0 0 0 耐药率/% 100.00 0 100.00 0 0 0 0 0 0 屎肠球菌(n=1) 耐药菌株数/株 1 1 1 1 0 1 0 1 0 耐药率/% 100.00 100.00 100.00 100.00 0 100.00 0 100.00 0 表 4 ECMO术后医院感染的单因素分析(x±s)[n(%)][M(P25, P75)]
因素 感染组(n=41) 非感染组(n=35) 年龄/岁 56.76±13.66 47.49±17.24* 男性 28(68.29) 21(60.00) 高血压 24(58.54) 12(34.28) 糖尿病 12(29.27) 13(37.14) 机械通气时间/h 221.92(134.53, 281.85) 32.73(7.87, 128.47)** ECMO辅助时间/h 158.33(115.17, 196.38) 84.05(30.45, 114.71)** 抗菌药物使用时间/d 11.00(6.00, 16.00) 5.00(2.00, 9.00)** 中心静脉置管时间/d 10.00(7.00, 16.00) 5.00(1.50, 8.00)** 导尿管置管时间/d 13.00(7.00, 17.00) 6.00(3.00, 8.50)** 与感染组比较, * P<0.05, * * P<0.01。 表 5 ECMO术后发生医院感染危险因素的Logistic回归分析
变量 B SE Wald OR 95%CI P 年龄/岁 0.026 0.025 1.058 1.026 0.977~1.079 0.304 机械通气时间/h 0.018 0.006 9.136 1.018 1.006~1.030 0.003 ECMO辅助时间/h 0.017 0.008 4.960 1.017 1.002~1.033 0.026 抗菌药物使用时间/d 0.001 0.078 0.000 1.001 0.859~1.167 0.986 中心静脉置管时间/d 0.073 0.123 0.354 1.076 0.846~1.369 0.552 导尿管置管时间/d -0.217 0.115 3.599 0.805 0.643~1.007 0.058 表 6 ECMO辅助时间及机械通气时间对ECMO后医院感染预测价值的ROC曲线分析结果
危险因素 AUC 最佳临界值 敏感性/% 特异性/% 95%CI 最大约登指数 P 下限 上限 ECMO辅助时间/h 0.812 128.04 68.3 85.7 0.714 0.909 0.54 <0.001 机械通气时间/h 0.873 64.48 97.6 68.6 0.053 0.793 0.66 <0.001 -
[1] BRODIE D, SLUTSKY A S, COMBES A. Extracorporeal life support for adults with respiratory failure and related indications: a review[J]. JAMA, 2019, 322(6): 557-568. doi: 10.1001/jama.2019.9302
[2] HILL J D, O'BRIEN T G, MURRAY J J, et al. Prolonged extracorporeal oxygenation for acute post-traumatic respiratory failure (shock-lung syndrome). Use of the Bramson membrane lung[J]. N Engl J Med, 1972, 286(12): 629-634. doi: 10.1056/NEJM197203232861204
[3] WANG D W, HU B, HU C, et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China[J]. JAMA, 2020, 323(11): 1061-1069. doi: 10.1001/jama.2020.1585
[4] 唐晓, 蒲琳, 张佳莹, 等. 体外膜肺氧合治疗危重症新型冠状病毒肺炎和新型甲型H1N1流感病毒性肺炎临床特征和预后比较[J]. 中华医学杂志, 2021, 101(8): 579-585. [5] ABRAMS D, COMBES A, BRODIE D. Extracorporeal membrane oxygenation in cardiopulmonary disease in adults[J]. J Am Coll Cardiol, 2014, 63(25 Pt A): 2769-2778.
[6] 闫晓蕾, 李群, 杨勇, 等. 心脏术后体外膜肺氧合支持治疗的医院感染分析[J]. 中华医院感染学杂志, 2011, 21(3): 462-465. https://www.cnki.com.cn/Article/CJFDTOTAL-ZHYY201103023.htm [7] 王静, 熊莹, 施颖, 等. 成人心脏术后患者体外膜肺氧合治疗相关医院感染的危险因素及病原学分析[J]. 中华临床感染病杂志, 2019, 12(1): 38-43. doi: 10.3760/cma.j.issn.1674-2397.2019.01.006 [8] AUBRON C, CHENG A C, PILCHER D, et al. Infections acquired by adults who receive extracorporeal membrane oxygenation: risk factors and outcome[J]. Infect Control Hosp Epidemiol, 2013, 34(1): 24-30. doi: 10.1086/668439
[9] SCHMIDT M, BRÉCHOT N, HARIRI S, et al. Nosocomial infections in adult cardiogenic shock patients supported by venoarterial extracorporeal membrane oxygenation[J]. Clin Infect Dis, 2012, 55(12): 1633-1641. doi: 10.1093/cid/cis783
[10] KIM G S, LEE K S, PARK C K, et al. Nosocomial infection in adult patients undergoing veno-arterial extracorporeal membrane oxygenation[J]. J Korean Med Sci, 2017, 32(4): 593-598. doi: 10.3346/jkms.2017.32.4.593
[11] GRASSELLI G, SCARAVILLI V, DI BELLA S, et al. Nosocomial infections during extracorporeal membrane oxygenation: incidence, etiology, and impact on patients'outcome[J]. Crit Care Med, 2017, 45(10): 1726-1733. doi: 10.1097/CCM.0000000000002652
[12] 谈宜斌, 王莹, 蔡书翰, 等. 成人体外膜肺氧合术支持治疗患者医院感染流行病学特点[J]. 中华医院感染学杂志, 2020, 30(22): 3434-3438. https://www.cnki.com.cn/Article/CJFDTOTAL-ZHYY202022017.htm [13] KIM H S, PARK S, KO H H, et al. Different characteristics of bloodstream infection during venoarterial and venovenous extracorporeal membrane oxygenation in adult patients[J]. Sci Rep, 2021, 11(1): 9498. doi: 10.1038/s41598-021-89108-4
[14] SUN H Y, KO W J, TSAI P R, et al. Infections occurring during extracorporeal membrane oxygenation use in adult patients[J]. J Thorac Cardiovasc Surg, 2010, 140(5): 1125-1132, e2. doi: 10.1016/j.jtcvs.2010.07.017
[15] KUMAR S, SEN P, GAIND R, et al. Prospective surveillance of device-associated health care-associated infection in an intensive care unit of a tertiary care hospital in New Delhi, India[J]. Am J Infect Control, 2018, 46(2): 202-206. doi: 10.1016/j.ajic.2017.08.037
[16] CHOUDHURI A H, CHAKRAVARTY M, UPPAL R. Epidemiology and characteristics of nosocomial infections in critically ill patients in a tertiary care Intensive Care Unit of Northern India[J]. Saudi J Anaesth, 2017, 11(4): 402-407. doi: 10.4103/sja.SJA_230_17
[17] 蔡璇, 施金玲, 李从荣, 等. 重症监护病房病原菌分布及药敏分析[J]. 中国临床药理学杂志, 2021, 37(11): 1403-1407. https://www.cnki.com.cn/Article/CJFDTOTAL-GLYZ202111024.htm [18] MOHD SAZLLY LIM S, SIME F B, ROBERTS J A. Multidrug-resistant Acinetobacter baumannii infections: current evidence on treatment options and the role of pharmacokinetics/pharmacodynamics in dose optimisation[J]. Int J Antimicrob Agents, 2019, 53(6): 726-745. doi: 10.1016/j.ijantimicag.2019.02.016
[19] MOHD SAZLLY LIM S, NAICKER S, AYFAN A K, et al. Non-polymyxin-based combinations as potential alternatives in treatment against carbapenem-resistant Acinetobacter baumannii infections[J]. Int J Antimicrob Agents, 2020, 56(4): 106115. doi: 10.1016/j.ijantimicag.2020.106115
[20] CANDEL F J, SANTERRE HENRIKSEN A, LONGSHAW C, et al. In vitro activity of the novel siderophore cephalosporin, cefiderocol, in Gram-negative pathogens in Europe by site of infection[J]. Clin Microbiol Infect, 2022, 28(3): 447.e1-447.e6.
[21] BIZZARRO M J, CONRAD S A, KAUFMAN D A, et al. Infections acquired during extracorporeal membrane oxygenation in neonates, children, and adults[J]. Pediatr Crit Care Med, 2011, 12(3): 277-281. doi: 10.1097/PCC.0b013e3181e28894
[22] 丁兴芬. ICU医院感染预防与控制的研究[J]. 实用临床医药杂志, 2017, 21(2): 138-139. doi: 10.7619/jcmp.201702045 [23] ELLOUZE O, LAMIREL J, PERROT J, et al. Extubation of patients undergoing extracorporeal life support. A retrospective study[J]. Perfusion, 2019, 34(1): 50-57. doi: 10.1177/0267659118791072
[24] LI B F, SUN G Q, CHENG Z, et al. Analysis of nosocomial infections in post-cardiac surgery extracorporeal membrane oxygenation support therapy[J]. Heart Surg Forum, 2018, 21(5): E387-E391. doi: 10.1532/hsf.1789
[25] MONTERO S, HUANG F, RIVAS-LASARTE M, et al. Awake venoarterial extracorporeal membrane oxygenation for refractory cardiogenic shock[J]. Eur Heart J Acute Cardiovasc Care, 2021, 10(6): 585-594. doi: 10.1093/ehjacc/zuab018
-
期刊类型引用(2)
1. 代晓娟,温凯,许可. 平鳍式种植体与螺纹式种植体对口腔种植患者经济负担与并发症的影响. 中国美容医学. 2023(03): 144-147 .  百度学术
百度学术
2. 王雪红,陈彩云,李莹. 低能量激光疗法治疗种植体周围炎患者的临床效果. 现代养生. 2023(17): 1288-1290 .  百度学术
百度学术
其他类型引用(1)




 下载:
下载:
 苏公网安备 32100302010246号
苏公网安备 32100302010246号
