Effects of intracoronary alteplase infusion on microcirculatory function during percutaneous coronary intervention
-
摘要:目的
探讨直接经皮冠状动脉介入治疗(PCI)期间冠状动脉内输注阿替普酶对微循环功能急性侵入性参数的影响。
方法选取心内科行急诊PCI的80例缺血时间≤6 h的急性ST段抬高型心肌梗死(STEMI)患者作为研究对象,采用随机数字表法分为阿替普酶组和对照组,每组40例。阿替普酶组于再灌注[心肌梗死溶栓试验(TIMI)血流分级≥2级]后将10 mg阿替普酶注入至冠状动脉罪犯血管中,然后植入支架;对照组于再灌注(TIMI血流分级≥2级)后立即植入支架。PCI后,检测2组微循环功能急性侵入性参数[微循环阻力指数(IMR)、阻力储备比(RRR)和血流储备分数(CFR)]。
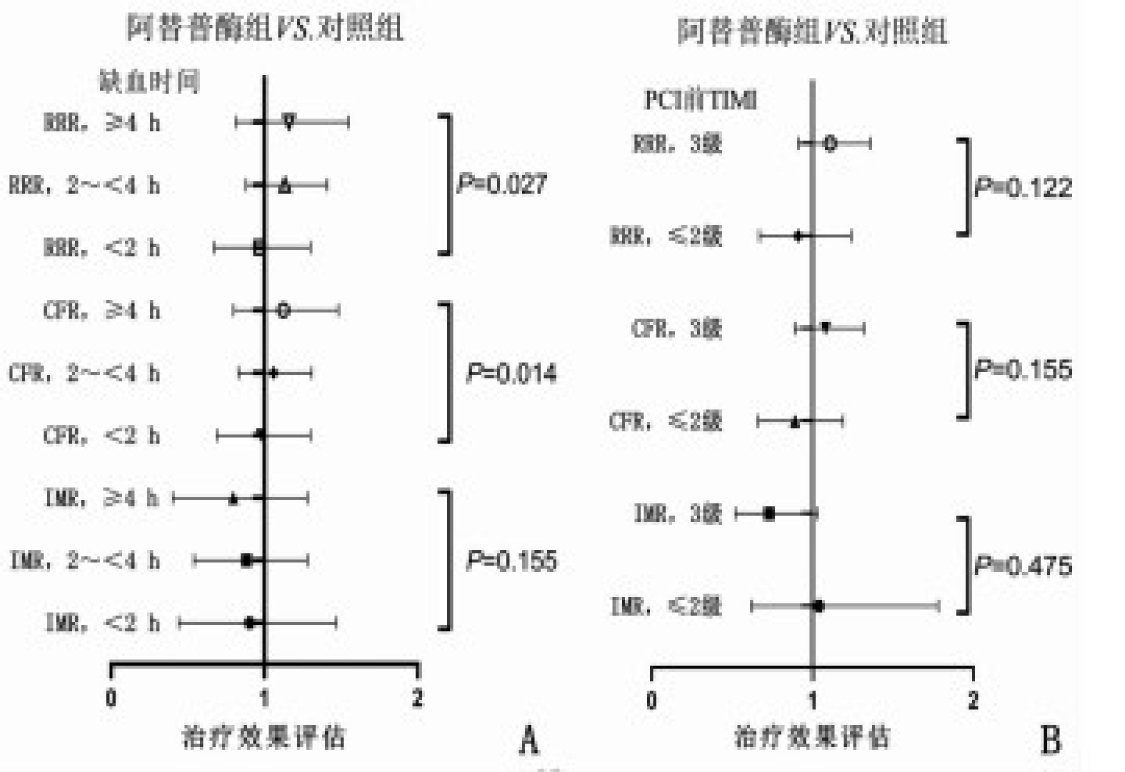
结果阿替普酶组、对照组的IMR分别为22.0(17.0,42.0)、33.0(17.0,57.0),差异无统计学意义(P>0.05);阿替普酶组的CFR、RRR分别为1.4(1.1,1.9)、1.6(1.4,2.6),对照组的CFR、RRR分别为1.3(1.1,1.8)、1.6(1.3,2.2),差异无统计学意义(P>0.05)。亚组分析显示,缺血时间和阿替普酶与IMR无交互作用(P=0.155),缺血时间和阿替普酶与CFR(P=0.014)、RRR(P=0.027)存在交互作用。在缺血时间 < 2 h的患者中,阿替普酶组CFR、RRR依次为2.0(1.7,2.3)、2.2(2.0,2.6),分别高于对照组的1.2(1.1,1.7)、1.5(1.3,1.9),差异有统计学意义(P < 0.05)。
结论直接PCI期间向冠状动脉罪犯血管中输注阿替普酶,对缺血时间≤6 h的急性STEMI患者PCI结束时罪犯血管微循环功能(IMR、CFR、RRR)无明显影响。
-
关键词:
- 经皮冠状动脉介入治疗 /
- 阿替普酶 /
- 微循环功能 /
- 急性ST段抬高型心肌梗死 /
- 急性侵入性参数
Abstract:ObjectiveTo investigate the effects of intracoronary alteplase infusion on acute invasive parameters on microcirculatory function during primary percutaneous coronary intervention (PCI).
MethodsA total of 80 acute ST-segment elevation myocardial infarction (STEMI) patients with ischemia time ≤ 6 h who underwent emergency PCI in the Department of Cardiology were included as study objects. The patients were divided into alteplase group and control group according to method of random number table, with 40 cases in each group. In the alteplase group, 10 mg of alteplase was infused into coronary criminal lesions after reperfusion[blood flow grade of thrombolysis test for myocardial infarction (TIMI) ≥ 2], followed by stent implantation. The control group was implanted with stent immediately after reperfusion (blood grade of TIMI ≥ 2). Acute invasive parameters of microcirculatory function[microcirculatory resistance (IMR), resistance reserve ratio (RRR), and flow reserve (CFR)] were measured after PCI.
ResultsThe IMR of the alteplase group and control group were 22.0(17.0, 42.0) and 33.0(17.0, 57.0), respectively, and there was no significant between-group difference (P>0.05). The CFR and RRR of the alteplase group were 1.4(1.1, 1.9) and 1.6(1.4, 2.6), respectively, and were 1.3(1.1, 1.8) and 1.6(1.3, 2.2), respectively in the control group, no significance between-group difference was observed (P>0.05). Subgroup analysis showed no interaction of ischemia time and alteplase with IMR(P=0.155). Interactions of ischemia time and alteplase with CFR (P=0.014) and RRR (P=0.027) were observed. In patients with ischemic times < 2 h, the CFR and RRR of the alteplase group were 2.0(1.7, 2.3) and 2.2(2.0, 2.6), respectively, which were higher than 1.2(1.1, 1.7) and 1.5(1.3, 1.9) of the control group (P < 0.05).
ConclusionInfusion of alteplase to culprit artery microvascular has no significant effect on culprit artery microvascular function (IMR, CFR or RRR) during PCI in acute STEMI with ischemia time ≤ 6 h.
-
-
表 1 2组患者一般资料比较(x±s)[n(%)][M(P25, P75)]
指标 分类 阿替普酶组(n=40) 对照组(n=40) 年龄/岁 60.2±10.1 61.0±8.8 性别 男 35(87.5) 33(82.5) 女 5(12.5) 7(17.5) 体质量指数/(kg/m2) 27.2±3.8 27.8±3.7 缺血时间/h 2.5(2.0, 3.5) 2.5(2.1, 3.4) 病史 高血压病 14(35.0) 10(25.0) 糖尿病 5(12.5) 3(7.5) 高胆固醇血症 9(22.5) 8(20.0) 冠心病 14(35.0) 17(42.5) 吸烟史 19(47.5) 15(37.5) PCI前用药 阿司匹林 4(10.0) 2(5.0) 降脂药 9(22.5) 7(17.5) ACE抑制剂或ARB 9(22.5) 7(17.5) β受体阻滞剂 6(15.0) 3(7.5) 钙通道阻滞剂 3(7.5) 4(10.0) 实验室指标 肌酸激酶/(U/L) 1 040.2(441.5, 1 913.6) 1 127.0(453.3, 2 170.6) 肌酸激酶同工酶/(μg/L) 86.4(28.3, 206.8) 102.1(37.4, 215.7) 肌钙蛋白T/(μg/L) 1.8(0.6, 5.0) 1.7(0.4, 4.1) PCI: 经皮冠状动脉介入治疗; ACE: 血管紧张素转化酶; ARB: 血管紧张素受体阻断剂。 表 2 2组患者冠状动脉造影特征和PCI参数比较(x±s)[n(%)]
特征/参数 分类 阿替普酶组(n=40) 对照组(n=40) 血管病变数量 2支 30(75.0) 30(75.0) 3支 10(25.0) 10(25.0) 血管造影所示罪犯血管 左前降支 12(30.0) 14(35.0) 左旋支动脉 11(27.5) 10(25.0) 右冠状动脉 17(42.5) 16(40.0) PCI前TIMI血流分级 0级 22(55.0) 24(60.0) 1级 4(10.0) 3(7.5) 2级 9(22.5) 10(25.0) 3级 5(12.5) 3(7.5) PCI后TIMI血流分级 0级 0 0 1级 1(2.5) 3(7.5) 2级 8(20.0) 3(7.5) 3级 31(77.5) 34(85.0) PCI参数 支架长度/mm 34.1±15.0 32.1±15.6 支架直径/mm 3.6±0.6 3.7±0.5 血栓切除术 3(7.5) 5(12.5) 预扩张 24(60.0) 21(52.5) 后扩张 13(32.5) 10(25.0) 使用糖蛋白Ⅱb/Ⅲa抑制剂 5(12.5) 4(10.0) PCI: 经皮冠状动脉介入治疗; TIMI: 心肌梗死溶栓试验。 表 3 冠状动脉微循环功能急性侵入性参数分析[n(%)][M(P25, P75)]
指标 全组(n=80) 对照组(n=40) 阿替普酶组(n=40) 相对差异(95%CI) P IMR 29.5(17.0, 55.0) 33.0(17.0, 57.0) 22.0(17.0, 42.0) 0.79(0.58~1.07) 0.125 IMR>40 32(40.0) 21(52.5) 11(27.5) 0.42(0.17~1.02) 0.054 IMR>32 38(47.5) 23(57.5) 15(37.5) 0.54(0.23~1.24) 0.147 CFR 1.4(1.1, 2.0) 1.3(1.1, 1.8) 1.4(1.1, 1.9) 1.01(0.86~1.19) 0.900 CFR≤2 64(80.0) 33(82.5) 31(77.5) 1.62(0.59~3.36) 0.680 RRR 1.6(1.3, 2.3) 1.6(1.3, 2.2) 1.6(1.4, 2.6) 1.04(0.88~1.23) 0.658 IMR: 微循环阻力指数; RRR: 阻力储备比; CFR: 血流储备分数。 表 4 IMR、CFR和RRR的缺血时间亚组分析[M(P25, P75)]
指标 缺血时间 对照组(n=40) 阿替普酶组(n=40) 相对差异(95%CI) P 交互P IMR < 2 h 45.0(23.0, 53.2) 29.0(17.0, 36.0) 0.52(0.26~1.04) 0.064 0.155 2~< 4 h 31.5(15.5, 51.0) 24.0(15.0, 42.0) 1.24(0.86~1.79) 0.250 ≥4 h 28.0(19.0, 60.0) 19.0(17.0, 34.0) 1.07(0.58~1.96) 0.837 CFR < 2 h 1.2(1.1, 1.7) 2.0(1.7, 2.3) 1.59(1.11~2.27) 0.012 0.014 2~< 4 h 1.3(1.1, 1.8) 1.4(1.2, 1.8) 1.00(0.82~1.21) 0.987 ≥4 h 1.7(1.4, 2.0) 1.8(1.3, 2.6) 0.82(0.60~1.13) 0.224 RRR < 2 h 1.5(1.3, 1.9) 2.2(2.0, 2.6) 1.52(1.05~2.22) 0.028 0.027 2~< 4 h 1.6(1.3, 2.2) 1.6(1.5, 2.6) 0.98(0.80~1.20) 0.848 ≥4 h 1.9(1.6, 2.3) 2.3(1.6, 2.8) 0.86(0.61~1.20) 0.367 -
[1] 汪雁博, 刁敬超, 支伟, 等. 重组人尿激酶原溶栓失败的ST段抬高型心肌梗死患者的临床特征及其影响因素分析[J]. 中国全科医学, 2021, 24(20): 2537-2541. doi: 10.12114/j.issn.1007-9572.2021.00.538 [2] 许浩军, 于宗良, 顾明, 等. 小剂量阿替普酶对重度血栓负荷急性心梗患者PCI术中的影响[J]. 中国循证心血管医学杂志, 2018, 10(12): 1520-1522, 1533. doi: 10.3969/j.issn.1674-4055.2018.12.22 [3] MAZNYCZKA A M, MCCARTNEY P J, ETEIBA H, et al. One-year outcomes after low-dose intracoronary alteplase during primary percutaneous coronary intervention: the T-TIME randomized trial[J]. Circ Cardiovasc Interv, 2020, 13(2): e008855. doi: 10.1161/CIRCINTERVENTIONS.119.008855
[4] 武艳强, 侯爱军, 傅向华, 等. 应用冠脉微循环阻力指数评价溶栓结合介入治疗的急性ST段抬高型心肌梗死患者预后的价值[J]. 心脏杂志, 2022, 34(1): 27-31. https://www.cnki.com.cn/Article/CJFDTOTAL-XGNZ202201006.htm [5] 王立珍, 刘玉荣, 武美英. 微循环阻力指数在评估经皮冠状动脉介入治疗后早期左心室重构及主要心血管不良事件风险中的价值[J]. 国际移植与血液净化杂志, 2021, 19(1): 1-5. doi: 10.3760/cma.j.cn115399-20201231-01001 [6] 陈晓会, 闫兆红, 闫冰, 等. 瞬时无波形比率(iFR)、微循环阻力指数(IMR)和血流储备分数(FFR)在诊断冠状动脉功能性狭窄中的应用[J]. 中国实验诊断学, 2020, 24(5): 870-873. doi: 10.3969/j.issn.1007-4287.2020.05.045 [7] SCARSINI R, DE MARIA G L, BORLOTTI A, et al. Incremental value of coronary microcirculation resistive reserve ratio in predicting the extent of myocardial infarction in patients with STEMI. insights from the Oxford acute myocardial infarction (OxAMI) study[J]. Cardiovasc Revasc Med, 2019, 20(12): 1148-1155. doi: 10.1016/j.carrev.2019.01.022
[8] GENG W, ZHANG Q, LIU J, et al. A randomized study of prourokinase during primary percutaneous coronary intervention in acute ST-segment elevation myocardial infarction[J]. J Interv Cardiol, 2018, 31(2): 136-143. doi: 10.1111/joic.12461
[9] LEVINE G N, O'GARA P T, BECKMAN J A, et al. Recent innovations, modifications, and evolution of ACC/AHA clinical practice guidelines: an update for our constituencies: a report of the American college of cardiology/American heart association task force on clinical practice guidelines[J]. Circulation, 2019, 139(17): e879-e886.
[10] MCCARTNEY P J, MAZNYCZKA A M, ETEIBA H, et al. Low-dose alteplase during primary percutaneous coronary intervention according to ischemic time[J]. J Am Coll Cardiol, 2020, 75(12): 1406-1421. doi: 10.1016/j.jacc.2020.01.041
[11] CLARKE J D, KENNEDY R, DUARTE LAU F, et al. Invasive evaluation of the microvasculature in acute myocardial infarction: coronary flow reserve versus the index of microcirculatory resistance[J]. J Clin Med, 2019, 9(1): E86. doi: 10.3390/jcm9010086
[12] FLORES C H, DÍEZ-DELHOYO F, SANZ-RUIZ R, et al. Microvascular dysfunction of the non-culprit circulation predicts poor prognosis in patients with ST-segment elevation myocardial infarction[J]. Int J Cardiol Heart Vasc, 2022, 39: 100997.
[13] EVERAARS H, VAN DER HOEVEN N W, JANSSENS G N, et al. Cardiac magnetic resonance for evaluating nonculprit lesions after myocardial infarction: comparison with fractional flow reserve[J]. JACC Cardiovasc Imaging, 2020, 13(3): 715-728. doi: 10.1016/j.jcmg.2019.07.019
[14] MAZNYCZKA A, HAWORTH P A J. Adjunctive intracoronary fibrinolytic therapy during primary percutaneous coronary intervention[J]. Heart Lung Circ, 2021, 30(8): 1140-1150. doi: 10.1016/j.hlc.2021.02.016
-
期刊类型引用(17)
1. 郑雅群. 坚强概念健康宣教联合全程化优质服务对肺结核大咯血患者服药依从性的影响. 基层医学论坛. 2024(24): 131-133+137 .  百度学术
百度学术
2. 杨英,王丽萍. 个性化优质护理在肺结核咯血患者行支气管动脉栓塞术后的临床价值. 临床医学研究与实践. 2021(01): 130-132 .  百度学术
百度学术
3. 宋萍伟,桑桂凤,李红霞,姜娟. 咯血病人介入治疗时接污装置的设计与应用. 护理研究. 2021(01): 177-179 .  百度学术
百度学术
4. 密芳,庞志敏,刘雨佳,张菁. 一体化链式急救模式在大咯血行支气管动脉栓塞术治疗患者中的应用. 中国现代医生. 2021(23): 177-180 .  百度学术
百度学术
5. 饶争丽. 急救护理在肺结核伴发大咯血患者中的应用效果. 中华灾害救援医学. 2020(01): 37-39 .  百度学术
百度学术
6. 林瑛,肖海燕,周通纲. 优质护理连续供给模式在大咯血行支气管动脉介入栓塞治疗患者中的应用. 齐鲁护理杂志. 2020(01): 103-105 .  百度学术
百度学术
7. 万小艳. 全程优质护理配合支气管动脉栓塞对咳血患者病情转归及不良反应的影响. 医疗装备. 2020(05): 185-186 .  百度学术
百度学术
8. 刘文丽. 中医护理模式辅助介入治疗肺动脉栓塞的临床观察. 中国民间疗法. 2019(11): 85-87 .  百度学术
百度学术
9. 马忠丽,王梦娇,李艳. 围手术期全程护理在反复大咯血患者超选择支气管动脉栓塞术护理中的应用. 河南医学研究. 2019(20): 3788-3790 .  百度学术
百度学术
10. 王万花,陈道琴,徐寒梅. 对进行支气管动脉栓塞术的患者实施预见性护理的效果分析. 当代医药论丛. 2019(19): 210-212 .  百度学术
百度学术
11. 严文娟. 咯血患者支气管动脉栓塞术后不同护理方法的观察研究. 中国医药指南. 2019(30): 2-3 .  百度学术
百度学术
12. 王建中,王筱,刘洋. 明胶海绵联合PVA颗粒支气管动脉栓塞治疗大咯血综合康复护理. 中外女性健康研究. 2019(23): 19-20+31 .  百度学术
百度学术
13. 刘欢,万晓蓉. 优质护理在介入栓塞术救治急重症大咯血患者中的应用分析. 实用临床护理学电子杂志. 2019(46): 89-90 .  百度学术
百度学术
14. 刘辉,刘慧. 对肺结核并发咯血患者进行全程护理的效果分析. 当代医药论丛. 2018(15): 198-199 .  百度学术
百度学术
15. 覃金贞,党惠枝. 浅析支气管动脉栓塞止血术应用于治疗肺结核咯血的护理. 实用临床护理学电子杂志. 2018(15): 43+47 .  百度学术
百度学术
16. 李秋丽. 大咯血患者介入治疗围术期优质护理效果观察. 中国校医. 2018(03): 226-227+229 .  百度学术
百度学术
17. 王楠楠,王莉莉. 支气管动脉介入栓塞治疗大咯血患者应用优质护理的效果研究. 中西医结合心血管病电子杂志. 2018(23): 134-135 .  百度学术
百度学术
其他类型引用(0)




 下载:
下载:
 苏公网安备 32100302010246号
苏公网安备 32100302010246号