Establishment and value of a diagnostic model for gastric precancerous lesions based on hematological indicators
-
摘要:目的
构建基于多个血液学指标的胃癌前病变(GPL)诊断模型,探讨其临床诊断效能。
方法纳入经上消化道肿瘤筛查确诊GPL的1 142例受试者,同时以1 222例正常或浅表性胃炎的受试者作为对照。采用Rand随机函数将所有受试者按7∶3的比例分为训练组(1 655例,其中GPL者779例,对照者876例)和验证组(709例,其中GPL者363例,对照者346例)。比较训练组中GPL患者与对照者的临床特征和实验室指标; 绘制受试者工作特征(ROC)曲线,获得GPL相关危险因素的诊断效能及最佳临界值,建立诊断模型。采用Hosmer-Lemeshow检验评估模型的拟合度,通过验证组进行内部验证; 采用曲线下面积(AUC)评估诊断模型的区分度。
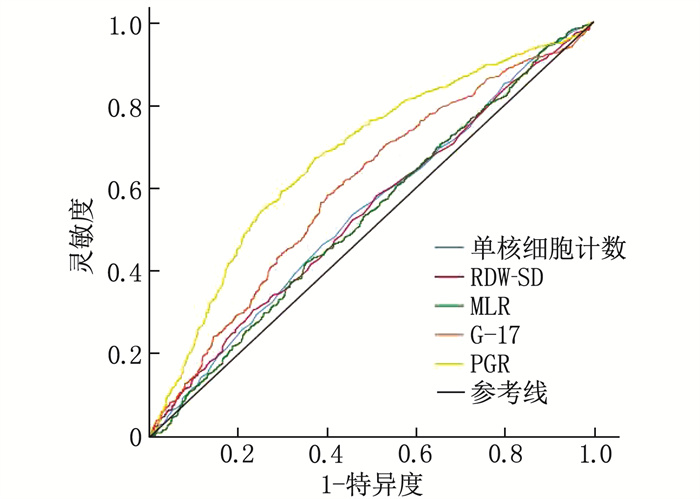
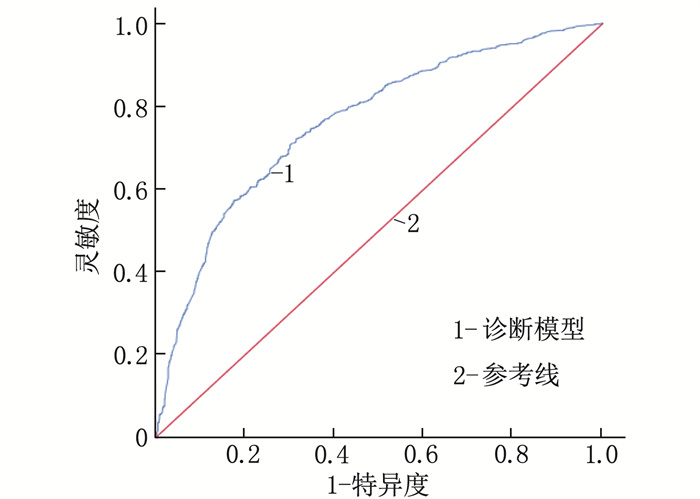
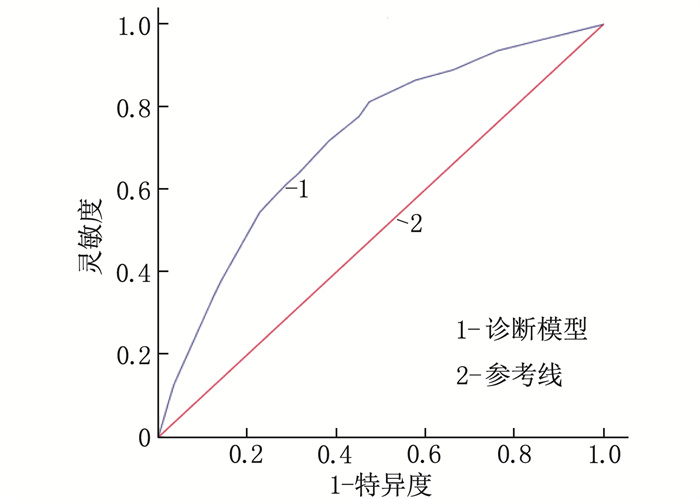
结果训练组中,男性、有吸烟史、饮酒史和幽门螺杆菌(H.pylori)感染史的受试者更易出现GPL, 而对照者进食速度更快、更易出现消化不良症状和胃病史,差异有统计学意义(P < 0.05); GPL组的单核细胞计数、红细胞分布宽度标准差(RDW-SD)、单核细胞与淋巴细胞比值(MLR)、血清胃泌素-17(G-17)最佳临界值依次为0.34×109/L、46.55 fL、0.23、3.98 pmol/L, 均高于对照组,差异有统计学意义(P < 0.05); GPL组胃蛋白酶原Ⅰ与胃蛋白酶原Ⅱ比值(PGR)的最佳临界值为11.80, 低于对照组,差异有统计学意义(P < 0.05)。多因素回归分析显示,具有H.pylori感染史、RDW-SD>46.55 fL、PGR < 11.80和G-17>3.98 pmol/L是GPL的独立危险因素(P < 0.001)。在训练组中,诊断模型的AUC=0.762(95%CI: 0.739~0.785, P < 0.001), 灵敏度为72.2%, 特异度为68.5%。将该模型应用于验证组进行内部验证,结果显示模型的AUC=0.719(95%CI: 0.681~0.756, P < 0.001), 灵敏度为81.3%, 特异度为52.6%, 提示该模型的区分能力较好。Hosmer-Lemeshow检验提示模型的拟合优度较好。
结论基于RDW、PGR、G-17和H.pylori感染史建立的GPL诊断模型具有较好的区分度和校准度,可以帮助早期识别GPL患者。
Abstract:ObjectiveTo establish a diagnostic model for gastric precancerous lesions (GPL) based on multiple hematological indicators, and to explore its clinical diagnostic efficiency.
MethodsA total of 1 142 subjects diagnosed as GPL by upper gastrointestinal cancer screening were enrolled, and 1 222 healthy subjects or patients with superficial gastritis were enrolled as controls. All the subjects were divided into training group (n=1 655, including 779 GPL cases and 876 controls) and validation group (n=709, including 363 GPL cases and 346 controls) at a ratio of 7 to 3 by Rand random function. Clinical characteristics and laboratory parameters were compared between GLP patients and controls in the training group; the receiver operator characteristic curve (ROC) was drawn to obtain the diagnostic efficacy and optimal threshold valuesfor GPL related risk factors, and the diagnostic model was established. The Hosmer-Lemeshow test was used to evaluate the fit of the model, and internal validation was performed through the validation group; the discrimination of the diagnostic model was evaluated by area under the curve (AUC).
ResultsIn the training group, patients with gender of male, a history of smoking, a history of drinking and a history of H.pylori infection were more likely to develop GPL, while the controls were faster in eating, had more digestive symptoms and history of stomach disease (P < 0.05). The optimal cut-off values of monocyte count, standard deviation of red blood cell distribution width (RDW-SD), monocyte-to-lymphocyte ratio (MLR), and serum gastrin-17 (G-17) were 0.34×109/L, 46.55 fL, 0.23, 3.98 pmol/L, respectively in the GPL group, which were higher than those of the control group (P < 0.05). The optimal cut-off value of pepsinogen Ⅰ-to-pepsinogen Ⅱ ratio (PGR) was 11.80 in the GPL group, which was significantly lower than that in the control group (P < 0.05). Multivariate regression analysis showed that a history of H.pylori infection, RDW-SD>46.55 fL, PGR < 11.80 and G-17>3.98 pmol/L were independent risk factors for GPL (P < 0.001). In the training cohort, the diagnostic model had an AUC of 0.762 (95%CI, 0.739 to 0.785; P < 0.001), sensitivity of 72.2%, and specificity of 68.5%. Validation of this model using the validation cohort showed that the model had an AUC of 0.719 (95%CI, 0.681 to 0.756; P < 0.001), sensitivity of 81.3%, and specificity of 52.6%, suggesting that the model had good discriminatory ability. The Hosmer-Lemeshow test indicated that the model had a good fitting.
ConclusionThe diagnostic model for GPL established based on RDW, PGR, G-17 and a history of H.pylori infection has good discrimination and calibration, and is a useful tool for the early identification of GPL patients.
-
溃疡性结肠炎(UC)是临床常见的慢性非特异性炎症性疾病,主要临床症状表现为腹痛、腹泻及脓血便。UC病因复杂,治疗不及时易引发严重并发症(下消化道大出血、中毒性巨结肠、癌变)。UC发病年龄范围较广,发病高峰年龄为20~49岁[1]。目前,临床治疗UC多为促进肠黏膜愈合,减轻炎症反应,抑制病情加重。常用药物氨基水杨酸制剂有一定的治疗效果,但易复发。熊去氧胆酸是结肠细菌代谢产生的胆汁酸,具有保护结肠上皮细胞屏障、抑制炎症反应的作用,在动物模型试验中表现出抑制小鼠结肠炎症反应、改善肠黏膜屏障功能的效果[2]。熊去氧胆酸可用于预防UC相关的肠上皮细胞屏障受损,抑制机体炎症反应及调控肠道菌群,但具体治疗UC的作用机制尚不清楚[3]。布拉氏酵母菌是一种微生态制剂,对于抑制细菌生长、抑制肠道炎症反应、改善肠黏膜屏障损伤具有一定的疗效,但长期单一用药治疗UC疗效不理想。本研究分析布拉氏酵母菌与熊去氧胆酸联合用药治疗直肠型UC患者的临床疗效,现报告如下。
1. 资料与方法
1.1 一般资料
选取2020年6月—2022年6月在本院治疗的88例直肠型UC患者为研究对象,根据治疗时间顺序随机分为观察组和对照组,每组44例。观察组男23例,女21例,年龄20~60岁,平均(36.72±6.77)岁; 病程5个月~4年,平均(2.36±0.95)年; 病情严重程度[4]为轻度21例,中度23例。对照组男22例,女22例,年龄21~60岁,平均(35.25±6.58)岁; 病程4个月~4年,平均(2.42±0.93)年; 病情严重程度为轻度23例,中度21例。2组患者基线资料比较,差异无统计学意义(P>0.05)。纳入标准: ①年龄18~70周岁者; ②所有患者符合《炎症性肠病诊断与治疗的共识意见(2018年·北京)》[4]中直肠型UC相关诊断标准,经结肠镜检查炎症病变累及的最大范围局限于直肠,未达乙状结肠; ③患者及家属自愿签署研究知情同意书。排除标准: ①合并严重脏器功能障碍者; ②对研究所用药物(布拉氏酵母菌散、熊去氧胆酸)过敏者; ③入院前自主治疗或者有他院治疗史者; ④重度直肠型UC患者; ⑤妊娠期、哺乳期女性; ⑥合并急慢性肠道炎或其他类型的肠道感染者; ⑦近期接受过胃肠手术者; ⑧合并自身免疫系统疾病者; ⑨合并精神疾病或神经系统异常而无法自主配合研究者。本研究通过伦理委员会审核。
1.2 治疗方法
所有研究对象均给予相同的基本管理和治疗,包括指导患者自我管理、给予心理支持及对患者进行基本教育,每天睡前0.9%生理盐水灌肠,直肠塞入2枚美沙拉嗪栓。对照组在此基础上给予熊去氧胆酸胶囊(德国Losan Pharma GmbH, 生产许可证号H20181059, 规格为250 mg/粒),每日给药剂量根据患者体质量为5 mg/kg, 2次/d。观察组在对照组基础上加用布拉氏酵母菌散(法国百科达制药厂,药品编号151039, 规格为0.25 g/袋),用药剂量为2袋/次, 2次/d。治疗期间, 2组均停用其他相关药物,忌食生冷、刺激性食物,保持心情舒畅,注意休息。2组均持续治疗8周。
1.3 评价标准
1.3.1 观察指标
(1) 主要症状评分[5-6]。对2组受试者主要症状(腹痛、腹泻、脓血便)进行评分,每项症状均按照正常(0分)、轻度(1分)、中度(2分)、重度(3分)共4个等级进行评分,分值越高提示症状越严重。①腹泻: 无、 < 3次/d、3~5次/d、>5次/d依次计0、1、2、3分; ②腹痛: 无、轻微隐痛,偶尔发作、腹痛腹胀,频发、腹部反复绞痛,或剧痛依次计0、1、2、3分; ③脓血便: 无、少量便血、脓血便为主、一直脓血便依次计0、1、2、3分。(2) 生活质量评估。采用炎症性肠病问卷(IBDQ)[7]进行评分, IBDQ共涉及肠道症状、全身症状、情感能力、社会能力4个方面共32个问题,每个问题计1~7分,总分32~224分,分值越高代表生活质量越好。(3) 实验室指标检测。治疗前后收集患者尿液,采用Aglient 1260高效液相色谱仪检测尿液中乳果酸与甘露醇的比值(L/M); 治疗前后分别采集患者空腹外周静脉血8 mL, 3 000转/min离心10 min, 吸取上清液置于-20 ℃冷藏待测。采用酶联免疫吸附法检测患者血清D-乳酸(D-LA)(上海舒话生物科技有限公司, SH-1201)、二胺氧化酶(DAO)(上海生工生物工程有限公司,D711173)、脂多糖(LPS, 上海酶联生物科技有限公司, ml061109)、白细胞介素-6(IL-6)(上海生工生物工程有限公司, D711391)、白细胞介素-1β(IL-1β)(上海生工生物工程有限公司, D711068)及肿瘤坏死因子-α(TNF-α)(上海生工生物工程有限公司, D711045)表达水平,试验操作步骤严格按照试剂盒说明书进行。
1.3.2 疗效判定标准[4]
① 完全缓解是指腹痛、腹泻、脓血便、发热等临床症状完全消失,结肠镜检肠黏膜正常或无活动性炎症; ②有效是指腹痛、腹泻、脓血便、发热等临床症状明显改善,结肠镜复检结果显示肠黏膜轻度炎症(红斑、黏膜充血或未见血管纹理); ③无效是指腹痛、腹泻、脓血便、发热等临床症状无改善,患者黏膜病变无明显改善甚至进一步加重。总有效率=(完全缓解例数+有效例数)/总例数×100%。
1.3.3 不良反应
记录2组患者治疗期间出现的与药物相关的不良反应,包括顽固型便秘、上腹部疼痛、过敏、荨麻疹等。
1.4 统计学分析
采用SPSS 25.0进行数据分析,计量资料均符合正态分布,以(x±s)表示,组间比较采用独立样本t检验,组内比较采用配对样本t检验,计数资料以[n(%)]表示,比较采用χ2检验。P < 0.05为差异有统计学意义。
2. 结果
2.1 2组治疗前后主要临床症状、IBDQ评分比较
治疗后, 2组腹痛、腹泻和脓血便评分均较治疗前降低, IBDQ评分高于治疗前,且观察组腹痛、腹泻和脓血便评分低于对照组, IBDQ评分高于对照组,差异均有统计学意义(P < 0.05), 见表 1。
表 1 2组主要临床症状、IBDQ评分比较(x±s)分 指标 时点 对照组(n=44) 观察组(n=44) 腹痛评分 治疗前 2.83±0.62 2.86±0.68 治疗后 2.32±0.47* 1.89±0.32*# 腹泻评分 治疗前 2.73±0.51 2.63±0.53 治疗后 2.13±0.39* 1.69±0.35*# 脓血便评分 治疗前 2.34±0.38 2.24±0.43 治疗后 1.61±0.32* 1.11±0.28*# IBDQ评分 治疗前 112.48±14.11 108.92±12.79 治疗后 148.36±14.25* 172.48±16.82*# IBDQ: 炎症性肠病问卷。与治疗前比较, * P < 0.05; 与对照组比较, #P < 0.05。 2.2 2组治疗前后肠黏膜屏障功能指标比较
治疗后, 2组血清D-LA、DAO、LPS和尿中L/M均降低,且观察组上述指标水平低于对照组,差异均有统计学意义(P < 0.05), 见表 2。
表 2 2组肠黏膜屏障功能指标比较(x±s)指标 时点 对照组 观察组 L/M 治疗前 0.036±0.006 0.038±0.005 治疗后 0.032±0.003* 0.029±0.003*# D-LA/(U/L) 治疗前 19.58±4.19 18.72±4.07 治疗后 10.32±2.78* 7.21±2.14*# DAO/(mg/L) 治疗前 12.28±2.33 12.54±2.24 治疗后 7.52±1.38* 5.21±1.26*# LPS/(pg/mL) 治疗前 84.48±11.11 88.54±10.59 治疗后 31.27±5.25* 22.48±4.62*# L/M: 乳果酸与甘露醇的比值; D-LA: D-乳酸; DAO: 二胺氧化酶; LPS: 脂多糖。与治疗前比较, * P < 0.05; 与对照组比较, #P < 0.05。 2.3 2组治疗前后炎性因子水平比较
治疗后, 2组血清IL-6、TNF-α和IL-1β水平降低,且观察组上述指标水平低于对照组,差异有统计学意义(P < 0.05), 见表 3。
表 3 2组治疗前后血清炎性因子水平比较(x±s)μg/L 组别 n IL-6 IL-1β TNF-α 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 对照组 44 44.31±5.33 30.15±3.38* 82.47±12.16 49.87±6.26* 40.48±5.11 25.27±4.26* 观察组 44 45.24±5.64 24.44±3.76*# 81.44±12.42 40.08±5.72*# 41.54±5.29 20.08±4.02*# IL-6: 白细胞介素-6; IL-1β: 白细胞介素-1β; TNF-α: 肿瘤坏死因子-α。与治疗前比较, * P < 0.05; 与对照组比较, #P < 0.05。 2.4 2组临床疗效比较
2组患者均接受8周治疗,观察组治疗总有效率为86.36%, 高于对照组的68.18%, 差异有统计学意义(P < 0.05), 见表 4。
表 4 2组临床疗效比较[n(%)]组别 n 完全缓解 有效 无效 总有效 观察组 44 18(40.91) 20(45.45) 6(13.64) 38(86.36)* 对照组 44 10(22.73) 20(45.45) 14(31.82) 30(68.18) 与对照组比较, * P < 0.05。 2.5 2组不良反应发生率比较
2组下腹部疼痛、过敏、顽固型便秘等不良反应发生率比较,差异无统计学意义(P>0.05), 见表 5。
表 5 2组不良反应发生率比较[n(%)]组别 n 下腹部疼痛 过敏 荨麻疹 顽固型便秘 对照组 44 3(6.82) 1(2.27) 0 4(9.09) 观察组 44 2(4.55) 1(2.27) 0 3(6.82) 3. 讨论
直肠型UC是临床常见的慢性非特异性炎性肠病,是以溃疡为主侵犯结肠和直肠的炎性疾病,发病年龄范围广,男女发病比例接近。目前UC病因尚不完全清晰,多认为与自身免疫、感染、遗传、肠黏膜屏障功能相关。UC患者肠黏膜屏障过度免疫,肠道微生物被破坏,肠道菌群紊乱,启动病理性炎症反应,激活炎性细胞活性,介导肠上皮细胞损坏。临床治疗轻、中度UC患者常用氨基水杨酸类制剂,重度患者以手术治疗为主。熊去氧胆酸是一种二羟基胆酸,具有保护细胞膜稳定和免疫调节作用。布拉氏酵母菌是一种真菌类益生菌,具有抗病原微生物、抗毒素和免疫调节作用,因具有较好耐酸性,不受胃肠液破坏,在肠道内具有较高活性。
既往研究[8]显示,小鼠结肠炎严重程度与胆汁酸的疏水程度相关,疏水性较强的高浓度胆汁酸带有细胞毒性作用,可促进细胞凋亡。亲水性胆汁酸具有较强的抗炎作用,熊去氧胆酸是亲水性胆汁酸,在体内与牛磺酸结合生成牛磺熊去氧胆汁酸,表现出较强的细胞保护作用[9], 极大地减轻了肠道炎症及缓解氧化应激,抑制UC疾病发展进程[10]。约90%的口服熊去氧胆酸成分在回肠被吸收,水解产生石胆酸与Takeda G蛋白偶联受体5(TGR5)结合,激活TGR5信号通路,抑制肠道炎症反应,调节屏障功能[11]。熊去氧胆酸能竞争性结合细胞膜表面毒性胆酸分子,阻止疏水性胆汁酸对细胞产生毒性损害,减少细胞凋亡,达到保护细胞、缓解肠黏膜屏障受损的效果。不同剂量的熊去氧胆酸治疗UC的研究存在争议,有文献[12]指出低剂量[8~15 mg/(kg·d)]长期服用熊去氧胆酸能明显降低结直肠癌发病率,长期服用高剂量[17~23 mg/(kg·d)]熊去氧胆酸预防结直肠癌的效果是不确定的。本研究以低剂量熊去氧胆酸治疗直肠型UC患者作为对照组,治疗后其主要症状评分、IBDQ评分以及肠黏膜屏障指标水平变化均提示治疗有效。
研究[13]显示,布拉氏酵母菌通过多种作用途径发挥抗毒素、抑制病原菌生长的作用,同时还为肠道黏膜细胞提供营养物质,增强细胞代谢能力,调控肠黏膜屏障功能,增强肠道免疫功能。研究[14]发现, UC发生、发展过程与丙酮酸激酶M2(PKM2)相关,布拉氏酵母菌通过PKM2发挥作用。庄鑫[15]研究发现,布拉氏酵母菌辅助治疗UC患者,能更好地抑制肠道炎症反应,进入肠道菌群发挥正向调控作用,降低LPS分泌水平,从而抑制机体IL-6、IL-1β和TNF-α等炎性因子活性及释放,缓解肠黏膜屏障损伤。本研究结果显示,相较于对照组,观察组血清IL-6、TNF-α和IL-1β炎性因子水平降低。上述研究均提示布拉氏酵母菌辅助治疗UC具有较好疗效。
肠道黏膜屏障功能障碍是UC患者的主要病理特征,表现为肠黏膜通透性增加。研究[16]表明,尿L/M是检测肠黏膜屏障受损较为灵敏的指标,肠黏膜屏障受损时,膜通透性增加,胞间连接紧密性降低,吸收乳果糖量增加,而吸收甘露醇的量不变或减少,造成尿中L/M值增大,以此判断肠黏膜损伤。D-LA是肠道乳酸菌酵解的产物, DAO是一种存在于肠黏膜绒毛细胞中高活性细胞内酶,当机体肠黏膜屏障受损时, D-LA与DAO入血进入体循环,作为检测肠黏膜屏障功能障碍的有效指标[17]。研究[18]显示, LPS是革兰氏阴性菌产生的糖脂,在肠道内发挥促炎作用,肠黏膜屏障受损时LPS进入体循环,同时其自身可介导慢性炎症反应,加剧黏膜损伤。本研究结果显示,观察组治疗后尿L/M减小,血清D-LA、DAO、LPS水平低于治疗前和对照组。熊去氧胆酸联合布拉氏酵母菌治疗直肠型UC患者,能够保护直肠上皮细胞,改善肠黏膜通透性,抑制炎症反应,缓解肠黏膜屏障功能障碍疗效理想。本研究中,相较于对照组,观察组治疗总有效率更高,不良反应发生率无显著差异。分析原因可能是熊去氧胆酸在回肠发挥细胞保护和抗炎作用,可减少细胞凋亡和减轻炎症损伤。布拉氏酵母菌辅助纠正肠道菌群状态,与熊去氧胆酸协同调控肠道免疫反应,抑制炎症反应,修复受损细胞,提供营养物质,加速肠黏膜屏障受损恢复过程。同时,熊去氧胆酸竞争性结合细胞膜表面毒性胆汁酸因子,进一步阻止细胞膜被侵袭。
综上所述,布拉氏酵母菌联合熊去氧胆酸治疗直肠型UC患者疗效优异,能够有效改善腹痛、腹泻和脓血便等症状,抑制机体炎症反应,缓解肠黏膜屏障受损,短期内可控制患者病情进展,提高生活质量。
-
表 1 训练组与验证组的基线资料比较[M(P25, P75)][n(%)]
基线资料 分类 训练组(n=1 655) 验证组(n=709) χ2/Z P 性别 男 660(39.9) 294(41.5) 0.520 0.471 女 995(60.1) 415(58.5) 年龄/岁 56.0(51.0, 65.0) 56.0(50.0, 64.0) -0.926 0.354 体质量指数/(kg/m2) 24.1(22.2, 26.3) 24.0(22.1, 26.1) -0.875 0.381 吸烟史 从不 1 200(72.5) 495(69.8) 1.978 0.372 已戒烟 91(5.5) 46(6.5) 吸烟 364(22.0) 168(23.7) 饮酒史 无 1 362(82.3) 582(82.1) 0.015 0.903 有 293(17.7) 127(17.9) 每日三餐情况 规律 1 443(87.2) 614(86.6) 0.165 0.921 较规律/偶尔不规律 182(11.0) 82(11.6) 经常不规律 30(1.8) 13(1.8) 进食速度 过慢 79(4.8) 33(4.7) 0.647 0.724 正常 1 293(78.1) 564(79.5) 过快 283(17.1) 112(15.8) 进食温度 过冷 41(2.5) 11(1.6) 2.347 0.309 温度适中 1 489(90.0) 649(91.5) 过烫 125(7.5) 49(6.9) 一级亲属癌症家族史 否 1 082(65.4) 471(66.4) 0.245 0.621 是 573(34.6) 238(33.6) H.pylori感染史 无 857(51.8) 363(51.2) 0.068 0.795 有 798(48.2) 346(48.8) 反复的消化不良症状 否 1 212(73.2) 518(73.1) 0.007 0.931 是 443(26.8) 191(26.9) 胃病史 无 1 003(60.6) 456(64.3) 2.894 0.089 有 652(39.4) 253(35.7) 中性粒细胞计数/(×109/L) 3.4(2.8, 4.3) 3.5(2.9, 4.4) 1.706 0.088 淋巴细胞计数/(×109/L) 1.7(1.3, 2.1) 1.7(1.4, 2.1) 1.274 0.202 单核细胞计数/(×109/L) 0.3(0.2, 0.5) 0.3(0.2, 0.5) 0.791 0.429 红细胞计数/(×1012/L) 4.6(4.3, 4.9) 4.6(4.3, 4.9) 0.546 0.585 血小板计数/(×109/L) 161.0(127.0, 201.0) 163.0(128.0, 206.5) 1.098 0.272 红细胞分布宽度标准差/fL 43.7(42.2, 45.8) 43.9(42.2, 45.7) 0.819 0.413 单核细胞与淋巴细胞比值 0.2(0.1, 0.3) 0.2(0.1, 0.3) -0.105 0.916 胃蛋白酶原Ⅰ与胃蛋白酶原Ⅱ比值 11.6(7.2, 16.8) 11.1(7.1, 15.6) -1.565 0.118 血清胃泌素-17/(pmol/L) 3.8(2.0, 8.4) 3.9(2.0, 8.6) 0.805 0.421 表 2 训练组中GPL相关参数的单因素分析[M(P25, P75)][n(%)]
参数 分类 GPL组(n=779) 对照组(n=876) χ2/Z P 性别 男 333(42.7) 327(37.3) 5.049 0.025 女 446(57.3) 549(62.7) 年龄/岁 56.0(51.0, 64.5) 56.0(51.0, 65.0) 0.249 0.803 体质量指数/(kg/m2) 24.0(22.2, 26.0) 24.3(22.3, 26.4) -1.505 0.132 吸烟史 从不 535(68.7) 665(75.9) 11.007 0.004 已戒烟 47(6.0) 44(5.0) 吸烟 197(25.3) 167(19.1) 饮酒史 无 621(79.7) 741(84.6) 6.716 0.010 有 158(20.3) 135(15.4) 每日三餐情况 规律 673(86.4) 770(87.9) 4.734 0.094 较规律/偶尔不规律 86(11.0) 96(11.0) 经常不规律 20(2.6) 10(1.1) 进食速度 过慢 32(4.1) 47(5.4) 7.121 0.028 正常 631(81.0) 662(75.6) 过快 116(14.9) 167(19.0) 进食温度 过冷 20(2.6) 21(2.4) 0.846 0.655 温度适中 705(90.5) 784(89.5) 过烫 54(6.9) 71(8.1) 一级亲属癌症家族史 否 504(64.7) 578(66.0) 0.300 0.584 是 275(35.3) 298(34.0) H.pylori感染史 无 257(33.0) 600(68.5) 208.144 < 0.001 有 522(67.0) 276(31.5) 反复的消化不良症状 否 589(75.6) 623(71.1) 4.243 0.039 是 190(24.4) 253(28.9) 胃病史 无 513(65.9) 490(55.9) 16.986 < 0.001 有 266(34.1) 386(44.1) 中性粒细胞计数/(×109/L) 3.5(2.8, 4.3) 3.4(2.8, 4.2) 1.622 0.105 淋巴细胞计数/(×109/L) 1.7(1.4, 2.1) 1.7(1.3, 2.1) 0.735 0.462 单核细胞计数/(×109/L) 0.3(0.2, 0.5) 0.3(0.2, 0.4) 3.058 0.002 红细胞计数/(×1012/L) 4.6(4.3, 4.9) 4.6(4.3, 4.9) -0.394 0.693 血小板计数/(×109/L) 161.0(127.0, 201.5) 161.0(128.0, 199.0) -0.205 0.837 红细胞分布宽度标准差/fL 43.9(42.3, 46.3) 43.5(42.1, 45.4) 2.884 0.004 单核细胞与淋巴细胞比值 0.2(0.1, 0.3) 0.2(0.1, 0.3) 2.321 0.020 胃蛋白酶原Ⅰ与胃蛋白酶原Ⅱ比值 9.0(6.0, 13.5) 13.8(9.6, 18.7) -12.408 < 0.01 血清胃泌素-17/(pmol/L) 4.7(2.4, 10.0) 3.1(1.7, 7.1) 7.007 < 0.001 表 3 多因素Logistic回归模型分析GPL的独立危险因素
参数 分类 回归系数 OR 95%CI P 性别 男 — — — — 女 — — — 0.975 吸烟史 从不 — — — — 已戒烟 — — — 0.168 吸烟 — — — 0.823 饮酒史 无 — — — — 有 — — — 0.587 进食速度 过慢 — — — — 正常 — — — 0.245 过快 — — — 0.290 H.pylori感染史 无 — 1.000 — — 有 -1.325 0.266 0.213~0.332 < 0.001 反复出现消化不良症状 否 — — — — 是 — — — 0.465 胃病史 无 — — — — 有 — — — 0.096 单核细胞计数 ≤0.34×109/L — — — — > 0.34×109/L — — — 0.123 红细胞分布宽度标准差 ≤45.55 fL — 1.000 — — > 45.55 fL -0.646 0.524 0.400~0.687 < 0.001 单核细胞与淋巴细胞比值 ≤0.23 — — — — > 0.23 — — — 0.094 胃蛋白酶原Ⅰ与胃蛋白酶原Ⅱ比值 ≥11.80 — 1.000 — — < 11.80 -0.867 0.420 0.335~0.527 < 0.001 血清胃泌素-17 ≤3.98 pmol/L — 1.000 — — > 3.98 pmol/L -0.459 0.632 0.507~0.788 < 0.001 常量 1.881 — — — -
[1] 赫捷, 陈万青, 李兆申, 等. 中国胃癌筛查与早诊早治指南(2022, 北京)[J]. 中国肿瘤, 2022, 31(7): 488-527. https://www.cnki.com.cn/Article/CJFDTOTAL-ZHLU202207009.htm [2] ZHANG Y J, WU X, ZHANG C L, et al. Dissecting expression profiles of gastric precancerous lesions and early gastric cancer to explore crucial molecules in intestinal-type gastric cancer tumorigenesis[J]. J Pathol, 2020, 251(2): 135-146. doi: 10.1002/path.5434
[3] 廖专, 孙涛, 吴浩, 等. 中国早期胃癌筛查及内镜诊治共识意见(2014年4月·长沙)[J]. 胃肠病学, 2014, 19(7): 408-427. https://www.cnki.com.cn/Article/CJFDTOTAL-WIEC201407008.htm [4] 张华颖, 黄鑫宇, 薛会光, 等. 慢性萎缩性胃炎发生胃癌的危险因素: 一项长期随访研究[J]. 世界华人消化杂志, 2018, 26(31): 1812-1817. https://www.cnki.com.cn/Article/CJFDTOTAL-XXHB201831005.htm [5] 王青青, 王子安. 外周血红细胞分布宽度、超氧化物歧化酶与胃癌预后的相关性[J]. 现代肿瘤医学, 2022, 30(6): 1041-1046. https://www.cnki.com.cn/Article/CJFDTOTAL-SXZL202206018.htm [6] SHEN H Z, XIONG K W, WU X Y, et al. The diagnostic value of serum gastrin-17 and pepsinogen for gastric cancer screening in eastern China[J]. Gastroenterol Res Pract, 2021, 2021: 6894248.
[7] HIROAKI S, SHOTA S, YUJI S, et al. Prognostic significance of the combination of preoperative red cell distribution width and platelet distribution width in patients with gastric cancer[J]. BMC Cancer, 2021, 21(1): 1317. doi: 10.1186/s12885-021-09043-5
[8] 牟龙霞, 王萍, 李冰, 等. 农村居民相对精准胃癌筛查评分系统的研究与应用[J]. 中华肿瘤防治杂志, 2022, 29(17): 1249-1255. https://www.cnki.com.cn/Article/CJFDTOTAL-QLZL202217002.htm [9] YIN X Y, PANG T, LIU Y, et al. Development and validation of a nomogram for preoperative prediction of lymph node metastasis in early gastric cancer[J]. World J Surg Oncol, 2020, 18(1): 2. doi: 10.1186/s12957-019-1778-2
[10] 房静远, 杜奕奇, 刘文忠, 等. 中国慢性胃炎共识意见(2017年, 上海)[J]. 胃肠病学, 2017, 22(11): 670-687. https://www.cnki.com.cn/Article/CJFDTOTAL-WIEC201711013.htm [11] SUNG H, FERLAY J, SIEGEL R L, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2021, 71(3): 209-249. doi: 10.3322/caac.21660
[12] YOSHIDA N, DOYAMA H, YANO T, et al. Original research: Early gastric cancer detection in high-risk patients: a multicentre randomised controlled trial on the effect of second-generation narrow band imaging[J]. Gut, 2021, 70(1): 67. doi: 10.1136/gutjnl-2019-319631
[13] 陈万青, 左婷婷. 中国上消化道癌防控初显成效[J]. 中华预防医学杂志, 2017, 51(5): 378-380. [14] 朱云峰, 陈新民, 沈永洲, 等. 2019年浙江省海宁市上消化道肿瘤机会性筛查效果评价[J]. 中国肿瘤, 2020, 29(12): 910-913. https://www.cnki.com.cn/Article/CJFDTOTAL-ZHLU202012004.htm [15] KHANDIA R, MUNJAL A. Interplay between inflammation and cancer[J]. Adv Protein Chem Struct Biol, 2020, 119: 199-245.
[16] FANG T Y, WANG Y M, YIN X, et al. Diagnostic sensitivity of NLR and PLR in early diagnosis of gastric cancer[J]. J Immunol Res, 2020, 2020: 9146042.
[17] OHSAWA M, HAMAI Y, EMI M, et al. Blood biomarkers as predictors of pathological lymph node metastasis in clinical stage T1N0 esophageal squamous cell carcinoma[J]. Dis Esophagus, 2022, 36(1): doac042.
[18] LIANG L, HUANG L Y, ZHAO X M, et al. Prognostic value of RDW alone and in combination with NT-proBNP in patients with heart failure[J]. Clin Cardiol, 2022, 45(7): 802-813.
[19] LIU J, HUANG X Y, YUE S R, et al. Association of red cell distribution width-to-platelet ratio and mortality in patients with Sepsis[J]. Mediators Inflamm, 2022, 2022: 4915887.
[20] TARGONSKI R, SADOWSKI J, STAREK-STELMASZCZYK M, et al. Prognostic significance of red cell distribution width and its relation to increased pulmonary pressure and inflammation in acute heart failure[J]. Cardiol J, 2020, 27(4): 394-403.
[21] PIETRZYK L, PLEWA Z, DENISOW-PIETRZYK M, et al. Diagnostic power of blood parameters as screening markers in gastric cancer patients[J]. Asian Pac J Cancer Prev, 2016, 17(9): 4433-4437.
[22] ALSALMAN A, AL-MTERIN M A, ABU-DAYEH A, et al. Associations of complete blood count parameters with disease-free survival in right- and left-sided colorectal cancer patients[J]. J Pers Med, 2022, 12(5): 816.
[23] ILHAN A, GURLER F, YILMAZ F, et al. The relationship between hemoglobin-RDW ratio and clinical outcomes in patients with advanced pancreas cancer[J]. Eur Rev Med Pharmacol Sci, 2023, 27(5): 2060-2067.
[24] SAYED I M, SAHAN A Z, VENKOVA T, et al. Helicobacter pylori infection downregulates the DNA glycosylase NEIL2, resulting in increased genome damage and inflammation in gastric epithelial cells[J]. J Biol Chem, 2020, 295(32): 11082-11098.
[25] 冯娟. 血清胃蛋白酶原与幽门螺旋杆菌筛查对胃癌早期诊断的临床价值分析[J]. 实用临床医药杂志, 2018, 22(19): 21-24. doi: 10.7619/jcmp.201819006 [26] KRIKE P, SHUMS Z, POLAKA I, et al. The diagnostic value of anti-parietal cell and intrinsic factor antibodies, pepsinogens, and gastrin-17 in corpus-restricted atrophic gastritis[J]. Diagnostics, 2022, 12(11): 2784.
-
期刊类型引用(11)
1. 张媛媛,赵志杰,刘青,李鹏飞,苑文娟. 血清NT-pro-BNP、IGFBP-7和CTRP12在慢性心力衰竭患者中的水平及意义. 检验医学与临床. 2025(01): 107-111+118 .  百度学术
百度学术
2. 陈伟光,谢冠聪,李桂云,龚宇锋,徐文波,王悦宁,许香广. 利用半乳糖凝集素-3、N末端B型利钠肽原联合超声心动图评估心力衰竭预后的研究. 齐齐哈尔医学院学报. 2022(09): 862-865 .  百度学术
百度学术
3. 吴利杰,董发. 左卡尼汀治疗慢性心力衰竭患者的疗效及安全性. 实用临床医药杂志. 2020(02): 104-107 .  本站查看
本站查看
4. 邓凡. BNP的检测在危重烧伤患者病情评估中的临床应用价值. 当代医学. 2020(18): 61-63 .  百度学术
百度学术
5. 李润琴,郑晓轩,柴慧. 左西孟旦联合复方丹参滴丸治疗慢性心力衰竭的临床研究. 中国药物与临床. 2020(23): 3949-3951 .  百度学术
百度学术
6. 孙婧,赵沱,刘亚荣. 自拟芪红汤在慢性心力衰竭患者康复治疗中的应用对心脏标记物、生活质量的影响. 四川中医. 2019(07): 86-88 .  百度学术
百度学术
7. 林傲,孙晗嫣,孙晗然,吕焕然,张钧宇,魏艳丽,王凤玲,黄佳滨. 半乳凝素3与超敏C反应蛋白在老年舒张性心力衰竭的相关性研究. 黑龙江医药科学. 2019(03): 45-46 .  百度学术
百度学术
8. 李振超. IL-27、树突状细胞在慢性心力衰竭患者外周血中的表达变化. 医学理论与实践. 2019(20): 3342-3343 .  百度学术
百度学术
9. 张建霞,杨培亮,王焕. 冠心病合并慢性心力衰竭患者GDF15、BNP、sST2的表达及其与心功能的相关性. 临床误诊误治. 2019(12): 67-71 .  百度学术
百度学术
10. 盛洋,郑学敏,王伟,沈盛晖. 酒石酸美托洛尔片联合左卡尼汀注射剂治疗慢性心力衰竭的临床研究. 中国临床药理学杂志. 2018(04): 410-413 .  百度学术
百度学术
11. 邓威. 血清Gal-3、NT-pro-BNP在慢性心力衰竭中的表达及临床意义. 中国民康医学. 2018(16): 20-21 .  百度学术
百度学术
其他类型引用(0)




 下载:
下载:
 苏公网安备 32100302010246号
苏公网安备 32100302010246号
