Value of Wilms tumor 1 gene combined with multiparameter flow cytometry for minimal residual disease in evaluating prognosis of children with acute myeloid leukemia
-
摘要:
目的分析肾母细胞瘤1(WT1)基因联合多参数流式细胞术检测微小残留病灶(FCM-MRD)对急性髓系白血病(AML)患儿预后的预测价值。
方法回顾性分析76例AML患儿的临床资料及一般信息。患儿治疗前均采用实时荧光定量聚合酶链式反应(qRT-PCR)检测WT1基因表达,并经FCM检测MRD。所有患儿随访1年,根据预后情况的不同分为预后良好组(n=40)和预后不良组(n=36)。观察2组患儿治疗前及治疗后3、9、12个月的WT1基因及MRD变化情况; 比较不同治疗方案患儿治疗前后WT1基因及MRD变化情况; 分析AML患儿临床病理特征与WT1基因表达及FCM-MRD阳性率的关系。采用Spearman相关系数分析WT1基因表达、FCM-MRD阳性率与AML患儿预后的关系; 绘制Kaplan-Meier生存曲线,分析WT1基因表达、FCM-MRD阳性率对AML患儿复发的影响及相关性; 绘制受试者工作特征(ROC)曲线分析WT1基因、FCM-MRD单一及联合检测对AML患儿预后的预测效能; 分析WT1基因、MRD与AML患儿FLT3 ITD/TKD突变的关系。
结果预后良好组患儿治疗后9、12个月的WT1表达量及FCM-MRD阳性率低于预后不良组,差异有统计学意义(P<0.05); 接受DAH化疗方案患儿的WT1基因表达、FCM-MRD阳性率低于接受DAE化疗方案患儿,预后良好率高于接受DAE化疗方案患儿,但差异无统计学意义(P>0.05); WT1基因表达及FCM-MRD阳性率与AML患儿白细胞计数、FAB分型、骨髓原始细胞及细胞遗传学分组具有相关性(P<0.05)。Spearman相关系数分析显示, WT1基因表达、FCM-MRD阳性率与AML患儿预后呈显著负相关(P<0.05); Kaplan-Meier生存曲线验证显示, WT1高表达患儿总生存期(OS)、无进展生存期(PFS)均低于WT1低表达患儿,差异有统计学意义(χ2=4.215、9.530, P=0.040、0.002), FCM-MRD阳性患儿OS、PFS均低于FCM-MRD阴性患儿, 差异也有统计学意义(χ2=5.144、6.381, P=0.023、0.012); Spearman相关系数分析显示, WT1基因表达与AML患儿OS、PFS呈显著负相关(P<0.05); ROC曲线显示, WT1联合FCM-MRD的曲线下面积显著高于单一指标检测结果,敏感度为88.89%, 特异度为87.50%; Spearman相关性分析显示,WT1基因表达、FCM-MRD阳性率与FLT3 ITD/TKD突变无相关性(P>0.05)。
结论WT1表达水平及FCM-MRD阳性率在不同预后AML患儿中具有特异性变化,与AML患儿预后具有强关联性,二者联合检测能够有效预测AML患儿的预后。
Abstract:ObjectiveTo analyze the value of Wilms tumor 1 (WT1) gene combined with multiparameter flow cytometry for minimal residual disease (FCM-MRD) in evaluating prognosis of children with acute myeloid leukemia (AML).
MethodsThe clinical data and general information of 76 children with AML were retrospectively analyzed. Before treatment, WT1 gene expression was detected by real-time fluorescence quantitative polymerase chain reaction (qRT-PCR) in all the children, and MRD was detected by FCM. All the children were followed up for a year, and they were divided into good prognosis group (n=40) and poor prognosis group (n=36) according to prognosis condition. The changes of WT1 gene and MRD before treatment and 3, 9 and 12 months after treatment were observed in both groups; the changes of WT1 gene and MRD before and after treatment were compared in the children with different therapeutic plans; the relationships of clinicopathological features with WT1 gene expression and positive rate of FMM-MRD were analyzed in AML children. Spearman correlation coefficient was used to analyze the relationships of WT1 gene expression and positive rate of FCM-MRD with the prognosis of AML children; the Kaplan-Meier survival curve was drawn to analyze the effects of WT1 gene expression and positive rate of FMM-MRD on the recurrence of AMLchildren and their correlations; the receiver operating characteristic (ROC) curve was drawn to analyze the efficiencies of single detection with WT1 gene and FMM-MRD and combined detection in predicting prognosis of AML children; the relationships of WT1 gen and MRD with FLT3 ITD/TKD mutation were analyzed in AML children.
ResultsThe WT1 expression levels and positive rates of FCM-MRD at 9 and 12 months after treatment in the good prognosis group were significantly lower than those in the poor prognosis group (P<0.05); the WT1 gene expression level and positive rate of FCM-MRD in children with DAH chemotherapy regimen were lower than those in children with DAE chemotherapy regimen, while the rate of good prognosis was higher than thatin children with DAE chemotherapy regimen, but there were no significant differences between children with different chemotherapy regimens (P>0.05); the WT1 gene expression and the positive rate of FCM-MRD were significantly correlated with white blood cell count, FAB typing, bone marrow primitive cells, and cytogenetic grouping in AML children (P<0.05). Spearman correlation coefficient analysis showed the WT1 gene expression and positive rate of FCM-MRD were significantly negatively correlated with prognosis of AML children (P<0.05); the Kaplan-Meier survival curve validation showed that overall survival (OS) and progression free survival (PFS) in children with high expression of WT1 were significantly lower than those in children with low expression of WT1 (χ2=4.215, 9.530; P=0.040, 0.002), and OS and PFS in children with positive FCM-MRD were also significantly lower than those in children with negative FCM-MRD (χ2=5.144, 6.381; P=0.023, 0.012); the Spearman correlation coefficient analysis showed that the WT1 gene expression was significantly negatively correlated with OS and PFS in AML children (P<0.05); the ROC curve showed that the area under the curve of WT1 combined with FCM-MRD was significantly higher than that of single indicator detection, with a sensitivity of 88.89% and a specificity of 87.50%; the Spearman correlation analysis showed that there were no significant correlations of WT1 gene expression and positive rate of FCM-MRD with FLT3 ITD/TKD mutation (P>0.05).
ConclusionThe expression level of WT1 and the positive rate of FCM-MRD show specific changes in AML children with different prognosis, and are strongly correlated with the prognosis of AML children. Combined detection of the two indicators can effectively predict the prognosis of AML children.
-
急性髓系白血病(AML)属于血液系统的恶性肿瘤疾病,是造血干祖细胞发生恶性克隆所致,临床症状多表现为感染、贫血、髓外组织器官浸润等[1-2]。临床流行病学数据调查[3]显示,在35岁以下人群中,急性白血病在中国恶性肿瘤中致死率排名首位,在儿童患者中, AML占儿童白血病的15%~20%, 治疗效果远不如儿童急性淋巴细胞白血病(ALL)。随着治疗手段的不断进步, AML患者的死亡率有所下降,但总体上患者5年生存率仍处于较低水平,复发是导致AML患者预后较差的主要原因[4]。研究[5]指出,微小残留病灶(MRD)作为引发AML患者复发的主要危险因素,对治疗无反应或具有一定耐药性,因此治疗后在患者体内有少量残留。
目前临床中对于MRD的检测无固定标准,其中多参数流式细胞术(FCM)以快速、准确、特异度高等特点成为检测MRD的主要技术手段[6]。由于AML患者具有高度的疾病异质性,部分患者缺乏特异融合基因标记,因此单纯的FCM-MRD检测也无法精确预测AML患者的预后复发情况[7]。肾母细胞瘤1(WT1)基因作为一种肿瘤抑制基因,可通过调控恶性肿瘤细胞增殖、分化情况来参与血液系统疾病的发生[8]。本研究选取76例AML患儿作为研究对象,观察WT1基因联合多参数FCM-MRD检测对该类患儿的预后预测价值,现将结果报告如下。
1. 资料与方法
1.1 一般资料
回顾性分析2015年1月—2020年12月本院收治的76例非急性早幼粒细胞白血病(APL)的AML患儿的临床资料及一般信息,对所有患儿随访至2023年5月,根据预后情况的不同将76例AML患儿分为预后良好组(n=40)和预后不良组(n=36)。预后良好组男24例,女16例,年龄0~12岁,中位年龄4.0岁,治疗前白细胞水平中位值为12.62×109/L; 预后不良组男22例,女14例,年龄0~12岁,中位年龄5.5岁,治疗前白细胞水平中位值为17.42×109/L。2组患儿一般信息及治疗前的病历资料比较,差异无统计学意义(P>0.05)。所有患儿及家属均对本研究取得知情权,本研究经本院伦理委员会批准进行,本研究所收集的患者信息及临床资料均采取保密措施。
纳入标准: ①依据患儿症状、体征,经细胞形态学、流式细胞学、细胞遗传学及分子遗传学(MICM)诊断体系确诊为AML(非APL)[9]者; ②具有完整的临床资料及一般信息者; ③无儿童多动症等精神系统类疾病者; ④在本院接受AML治疗者。排除标准: ①随访期间失访者; ②对治疗方案中用药具有禁忌证者; ③合并其他血液系统疾病者; ④依从性较低、无法配合研究者; ⑤合并其他恶性肿瘤者。
1.2 方法
1.2.1 化疗方案
76例AML患儿中, 35例患儿采用DAH化疗方案,具体药物方案为阿糖胞苷注射液(每次100 mg/m2, 第1~7天, 12 h给药1次)+注射用盐酸柔红霉素(每天40 mg/m2, 第1、3、5天)+高三尖杉酯碱(每天3 mg/m2, 第1~5天); 另外41例患儿采用DAE化疗方案,具体药物方案为阿糖胞苷注射液(每次100 mg/m2, 第1~7天, 12 h给药1次)+注射用盐酸柔红霉素(每天40 mg/m2, 第1、3、5天)+依托泊苷(VP-16, 每天100 mg/m2, 第1~5天),以28 d为1个治疗周期。
1.2.2 实时荧光定量聚合酶链式反应(qRT-PCR)检测WT1基因表达
采集患者外周血2 mL, EDTA抗凝, 1∶2加入红细胞裂解液震荡混匀, 3 500转/min离心10 min弃上清,加入1 mL红细胞裂解液重复洗涤1次, 3 500转/min离心10 min弃上清,并采用Trizol法提取全血基因组总RNA。应用荧光定量PCR仪(型号为LightCycler480 Ⅱ)及WT基因定量检测试剂盒(上海源奇生物)进行扩增检测, ABL为内参基因,引物序列为上游5′TGGAGATAACACTCTAAG CATAACTAAAGGT-3′, 下游5′-GATGTAGTTGCT TGGGACCCA-3′; WT1基因上游引物5′-GATAAC CACACAACGCCCATC-3′, 下游5′-CACACGTCGC ACATCCTGAAT-3′。扩增反应条件: 42 ℃, 30 min; 94 ℃, 5 min; 94 ℃、15 s, 60 ℃、60 s, 共40个循环,反应体系为25 μL。在PCR循环第2步60 ℃时收集荧光信号。采用2-△△Ct法计算WT1的相对表达水平。
1.2.3 FCM-MRD检测
流式细胞仪(型号为Canto Ⅱ)及实验所需单克隆抗体均购自美国BD公司,以Diva 9.1软件进行分析,每管≥500 000个有核细胞,通过CD45和侧向角散射设门; 按照各单抗组合加入对应的特异性抗体; 震荡混匀后室温避光放置15 min; 加入溶血素对红细胞进行裂解10 min, 1 500转/min离心5 min弃上清, PBS重复洗涤1次, 1 500转/min离心5 min弃上清,加入500 μL PBS混匀,采用流式细胞仪进行检测,检测灵敏度为0.1%,骨髓中白血病细胞<0.1%为MRD阴性; 骨髓细胞形态学≥5%为复发,多管抗体组合以数值最大者为MRD值[10]。
1.2.4 FLT3 ITD/TKD突变检测
采集纳入对象骨髓2 mL于EDTA抗凝管保存,使用淋巴细胞分离液分离得到骨髓单个核细胞,采用天根血液基因组DNA提取试剂盒(DP348)提取DNA。PCR反应扩增FLT3基因第14、15外显子检测FLT3-ITD突变,扩增FLT3基因第20号外显子检测FLT3-TKD点突变,运用一代测序技术进行测序,采用Chromas软件对结果进行比对分析,获得突变信息。
1.2.5 随访及预后评估标准
所有患儿均进行为期1年的随访,在治疗后3、9、12个月通过电话形式要求患儿定期到医院进行复查,截止时间为2023年5月。对患儿预后情况进行评估[11], 主要终点为总生存期(OS), 次要终点为无进展生存期(PFS), 将此期间发生OS及PFS的纳入预后不良组(n=36), 其他纳入预后良好组(n=40)。
1.3 统计学分析
采用SPSS 26.0分析数据,符合正态分布的计量资料以均数±标准差表示,组间对比使用t检验,同组内不同时点采用重复测量方差分析; 计数资料用[n(%)]表示,比较行χ2检验; Spearman相关系数分析WT1基因表达、FCM-MRD阳性率与AML患儿预后的关系; 绘制Kaplan-Meier生存曲线观察WT1基因表达、FCM-MRD阳性率对AML患儿复发的影响; 采用受试者工作特征(ROC)曲线分析WT1基因、FCM-MRD单一及联合检测对预测AML患儿预后的临床价值。P<0.05为差异有统计学意义。
2. 结果
2.1 2组AML患儿不同时点WT1基因表达及FCM-MRD阳性率变化
治疗前及治疗后3个月, 2组患儿WT1基因及FCM-MRD阳性率比较,差异无统计学意义(P>0.05); 预后良好组患儿治疗后9、12个月的WT1表达量及FCM-MRD阳性率低于预后不良组,差异有统计学意义(P<0.05)。见表 1。
表 1 2组AML患儿不同时点WT1基因表达及FCM-MRD阳性率变化(x±s)[n(%)]组别 时点 WT1基因 FCM-MRD阳性 预后良好组(n=40) 治疗前 0.80±0.34 — 治疗后3个月 0.85±0.31 23(57.50) 治疗后9个月 0.59±0.26 21(52.50) 治疗后12个月 0.73±0.37 19(47.50) 预后不良组(n=36) 治疗前 0.88±0.33 — 治疗后3个月 0.81±0.32 28(77.78) 治疗后9个月 0.73±0.37* 32(88.89)* 治疗后12个月 0.82±0.41* 29(80.56)* WT1: 肾母细胞瘤; FCM-MRD: 流式细胞术检测微小残留病灶。与预后良好组比较, *P<0.05。 2.2 不同治疗方案患儿WT1基因、FCM-MRD阳性率变化及预后良好率比较
治疗前, DAH化疗方案与DAE化疗方案患儿WT1基因表达及FCM-MRD阳性率比较,差异无统计学意义(P>0.05); 治疗后, DAH化疗方案患儿的WT1基因表达、FCM-MRD阳性率均低于DAE化疗方案患儿,预后良好率高于DAE化疗方案患儿,但差异无统计学意义(P>0.05)。见表 2。
表 2 不同方案患儿WT1基因、FCM-MRD阳性率变化及预后良好率比较(x±s)[n(%)]治疗方案 时点 WT1 FCM-MRD阳性 预后良好 DAH化疗方案(n=35) 治疗前 0.83±0.32 — — 治疗后 0.67±0.31 16(41.03) 19(48.72) DAE化疗方案(n=41) 治疗前 0.85±0.37 — — 治疗后 0.81±0.41 32(60.38) 21(39.62) 2.3 AML患儿临床病理特征与WT1基因表达及FCM-MRD阳性率的关系
WT1基因表达及FCM-MRD阳性率均与AML患儿白细胞计数、FAB分型[法国(France)、美国(American)和英国(Britain)等三国血细胞形态学专家讨论、制订的关于急性白血病的分型诊断标准]、骨髓原始细胞及细胞遗传学分组具有相关性(P<0.05)。见表 3。
表 3 AML患儿临床病理特征与WT1基因表达及FCM-MRD阳性率关系(x±s)[n(%)]临床特征 n WT1表达 t、F/P FCM-MRD阳性 χ2/P 性别 0.242/0.810 2.056/0.152 男 46 0.78±0.31 32(69.57) 女 30 0.76±0.41 16(53.33) 年龄 -0.120/0.904 1.040/0.308 >5岁 49 0.77±0.36 33(67.35) ≤5岁 27 0.78±0.32 15(55.56) 白细胞计数 -3.374/0.001 6.523/0.011 ≤50×109/L 37 0.64±0.32 18(48.65) >50×109/L 39 0.90±0.35 30(76.92) FAB分型 20.211/<0.001 6.445/0.012 M0 2 0.69±0.33 2(100.00) M1 5 0.68±0.31 2(40.00) M2 23 0.68±0.38 16(69.57) M4 9 0.74±0.34 6(66.67) M5 26 0.79±0.32 15(57.69) M7 11 0.88±0.42 7(63.64) 骨髓原始细胞 -2.643/0.010 6.124/0.013 <50% 43 0.68±0.33 22(51.16) ≥50% 33 0.89±0.36 26(78.79) 细胞遗传学分组 17.234/<0.001 5.667/0.021 良好核型组 29 0.67±0.34 12(41.38) 中等核型组 20 0.71±0.37 19(95.00) 不良核型组 27 0.85±0.36 17(62.96) FAB分型: 法国(France)、美国(American)和英国(Britain)等三国血细胞形态学专家讨论、制订的
关于急性白血病的分型诊断标准。2.4 WT1基因表达、FCM-MRD阳性率与AML患儿预后的关系
Spearman相关系数分析显示, WT1基因表达、FCM-MRD阳性率与AML患儿预后呈显著负相关(r=-0.642、-0.612, P<0.001)。
2.5 WT1基因表达对AML患儿预后的影响
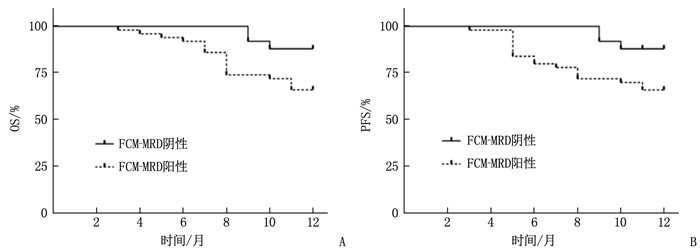
以76例AML患儿治疗后12个月的WT1基因表达均数(0.63)作为分界线,高于均数水平纳入WT1高表达组(n=34), 低于均数水平纳入WT1低表达组(n=42)。Kaplan-Meier生存曲线验证显示, WT1高表达组患儿OS、PFS均低于WT1低表达组,差异有统计学意义(χ2=4.215、9.530, P=0.040、0.002), 见图 1。Spearman相关系数分析显示, WT1基因表达与AML患儿OS、PFS呈显著负相关(r=-0.645、-0.591, P<0.001)。
2.6 FCM-MRD阳性率对AML患儿预后的影响
以76例AML患儿治疗后12个月的FCM-MRD阴性率、阳性率作为分界线, FCM-MRD阴性纳入阴性组(n=28),阳性纳入阳性组(n=48)。Kaplan-Meier生存曲线验证显示, FCM-MRD阳性组患儿OS、PFS均低于FCM-MRD阴性组,差异有统计学意义(χ2=5.144、6.381, P=0.023、0.012),见图 2。Spearman相关系数分析显示, FCM-MRD阳性率与AML患儿OS、PFS呈显著负相关(r=-0.622、-0.612, P<0.001)。
2.7 WT1基因联合FCM-MRD对AML患儿预后的预测价值
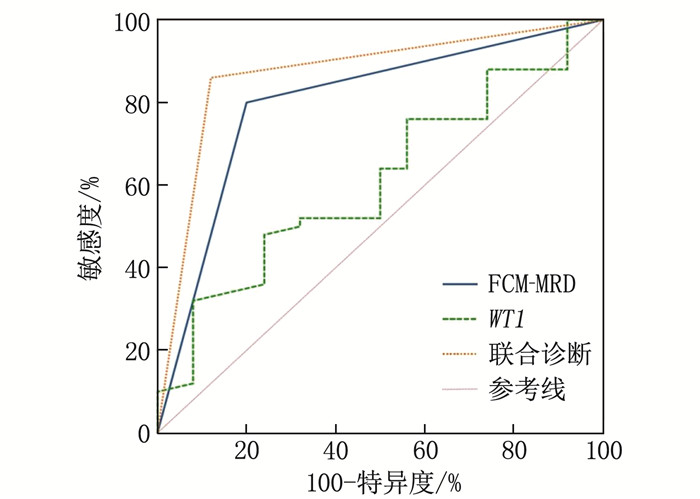
ROC曲线显示,WT1联合FCM-MRD的曲线下面积高于单一检测,且具有较高的敏感度与特异度,见表 4、图 3。
表 4 WT1基因联合FCM-MRD对AML患儿预后的预测效能指标 曲线下面积 95%CI 敏感度/% 特异度/% 截断值 约登指数 WT1 0.571* 0.452~0.684 41.67 80.00 >0.775 0.217 FCM-MRD 0.751* 0.639~0.843 77.78 72.50 — 0.503 联合诊断 0.882 0.788~0.945 88.89 87.50 — 0.764 与联合诊断比较, *P<0.05。 2.8 WT1基因、MRD与AML患儿FLT3 ITD/TKD突变的相关性分析
在76例AML患儿中,共有11例患儿发生FLT3 ITD突变, 9例患儿发生FLT3 TKD突变, 6例患儿发生FLT3 ITD/TKD双突变。Spearman相关性分析显示, WT1基因表达、FCM-MRD阳性率均与FLT3 ITD/TKD突变无相关性(P>0.05), 见表 5。
表 5 WT1基因、FCM-MRD阳性率与FLT3 ITD/TKD突变的相关性分析指标 FLT3 ITD突变 FLT3 TKD突变 FLT3 ITD/TKD双突变 r P r P r P WT1基因 0.122 0.062 0.221 0.059 0.198 0.060 FCM-MRD阳性率 0.210 0.059 0.111 0.102 0.144 0.078 3. 讨论
AML是一组造血干细胞分化障碍及增殖过度所致骨髓或外周血中原始、幼稚髓细胞发生异常克隆性增生的血液系统疾病,临床表现为贫血、出血、感染及白血病细胞浸润等症状,多数病情急重且预后较差。儿童患者中, AML占儿童白血病的15%~20%, 治疗效果远不如儿童ALL。AML患儿预后异质性较强,受到多种因素的影响,例如年龄、外周血白细胞计数、细胞遗传学异常、免疫学分型、髓外白血病、分子生物因素(基因突变、基因过表达)等,若不及时采取有效手段治疗,会对患儿的生命健康造成极大威胁[12-13]。随着临床治疗技术的不断进步, AML患儿接受治疗后的诱导缓解率逐渐上升,但是疾病复发仍是导致AML患儿预后不良的主要因素[14]。随着分子生物学检测手段的不断更新,定期、动态MRD检测对识别预后不良高危患者、早期发现有潜在复发概率的AML患者具有关键作用,尤其FCM-MRD识别具有高效、准确的特征,为预测AML患者预后提供了关键信息[15]。但AML患者仍存在一定的个体差异,因此通过特异性融合基因联合FCM-MRD或许能够进一步提高对AML患者预后的预测准确度。
WT1基因作为能够调控造血细胞生物学行为的一项基因,位于人染色体11P13位点,在多种血液肿瘤的发病中均具有重要作用[16]。本研究结果显示, WT1表达水平与AML患儿预后呈显著负相关(P<0.05), 即WT1表达越高, AML患儿预后越差; 预后不良组患儿在治疗后9、12个月的WT1表达量显著高于预后良好组(P<0.05), 主要是因为WT1能够影响多种与肿瘤发展具有密切联系的靶基因,如锌指蛋白[17]、血管内皮生长因子[18]等,通过干扰上述靶基因促进AML的发展进程。STEGER B等[19]研究发现WT1表达量越高提示肿瘤负荷也同样增高,主要是因为WT1存在癌基因的特性,尤其在未成熟的原始幼稚细胞中具有较高的表达水平,能够进一步促进肿瘤细胞的转录激活与抑制作用,因此高表达的WT1患者往往预后更差。本研究Kaplan-Meier生存曲线分析显示, WT1高表达组患儿的OS、PFS显著低于WT1低表达组,主要是因为WT1表达的上调会影响去甲基化TET2等因子的表达,从而导致癌细胞产生异常生物学行为,导致AML患儿不良预后的发生[20]。
MRD作为最能客观、直接反映AML患者疗效的一项指标,尤其是在通过FCM技术使用多参数单克隆抗体进行标记后,能够更加特异、全面地对AML异常抗原分布情况进行检测[21]。本研究结果显示,预后不良组患儿治疗后9、12个月的FCM-MRD阳性率显著高于预后良好组,且与AML患儿预后呈显著负相关(P<0.05), 即FCM-MRD阳性率越高, AML患儿预后越差。MRD作为肿瘤复发的主要原因,在AML患儿治疗、得到完全缓解后,传统影像学或实验室方法无法对残留的病灶直接发现,只能通过液体活检发现癌来源分子异常,从而提示AML的持续存在与进展的可能性。Kaplan-Meier生存曲线显示, FCM-MRD阳性AML患儿的OS、PFS显著低于FCM-MRD阴性患儿,与上述分析机制相同。
分析不同化疗方案结果显示,不同化疗方案对AML患儿WT1表达及FCM-MRD阳性率无显著影响,但DAH方案在一定程度上能够进一步降低WT1表达及FCM-MRD阳性率,主要是DAH方案中应用的高三尖杉酯碱作为传统中药提取的生物碱,在细胞增殖期发挥作用最强,可通过抑制真核细胞中蛋白质合成并抑制核糖体与肽链形成,从而表现出较强的肿瘤抑制作用。ROC曲线结果显示,单独FCM-MRD检测能够对AML患儿预后进行有效预测,但仍存在一定局限性,临床中超过半数的AML患者无特异性融合基因标记,因此联合一项能够识别大部分患者的分子标记至关重要[22]。本研究FLT3 ITD/TKD突变与WT1基因、MRD阳性率的关系分析显示,WT1基因、MRD阳性率与FLT3 ITD/TKD单突变、双突变均无显著关系,分析WT1基因、MRD阳性率在AML患儿FLT3 ITD/TKD突变过程无参与价值,且目前临床中尚无具体探讨WT1基因、MRD阳性率参与FLT3 ITD/TKD突变过程机制的研究,推测其在AML患儿FLT3 ITD/TKD突变过程中的具体影响机制还不明确,有待更多的基础研究进一步论证。
综上所述, WT1联合FCM-MRD能够作为跟踪AML患儿预后的重要检测手段,对了解病情进展、预防复发、改善AML患儿预后、指导临床早期干预均有关键作用。
-
表 1 2组AML患儿不同时点WT1基因表达及FCM-MRD阳性率变化(x±s)[n(%)]
组别 时点 WT1基因 FCM-MRD阳性 预后良好组(n=40) 治疗前 0.80±0.34 — 治疗后3个月 0.85±0.31 23(57.50) 治疗后9个月 0.59±0.26 21(52.50) 治疗后12个月 0.73±0.37 19(47.50) 预后不良组(n=36) 治疗前 0.88±0.33 — 治疗后3个月 0.81±0.32 28(77.78) 治疗后9个月 0.73±0.37* 32(88.89)* 治疗后12个月 0.82±0.41* 29(80.56)* WT1: 肾母细胞瘤; FCM-MRD: 流式细胞术检测微小残留病灶。与预后良好组比较, *P<0.05。 表 2 不同方案患儿WT1基因、FCM-MRD阳性率变化及预后良好率比较(x±s)[n(%)]
治疗方案 时点 WT1 FCM-MRD阳性 预后良好 DAH化疗方案(n=35) 治疗前 0.83±0.32 — — 治疗后 0.67±0.31 16(41.03) 19(48.72) DAE化疗方案(n=41) 治疗前 0.85±0.37 — — 治疗后 0.81±0.41 32(60.38) 21(39.62) 表 3 AML患儿临床病理特征与WT1基因表达及FCM-MRD阳性率关系(x±s)[n(%)]
临床特征 n WT1表达 t、F/P FCM-MRD阳性 χ2/P 性别 0.242/0.810 2.056/0.152 男 46 0.78±0.31 32(69.57) 女 30 0.76±0.41 16(53.33) 年龄 -0.120/0.904 1.040/0.308 >5岁 49 0.77±0.36 33(67.35) ≤5岁 27 0.78±0.32 15(55.56) 白细胞计数 -3.374/0.001 6.523/0.011 ≤50×109/L 37 0.64±0.32 18(48.65) >50×109/L 39 0.90±0.35 30(76.92) FAB分型 20.211/<0.001 6.445/0.012 M0 2 0.69±0.33 2(100.00) M1 5 0.68±0.31 2(40.00) M2 23 0.68±0.38 16(69.57) M4 9 0.74±0.34 6(66.67) M5 26 0.79±0.32 15(57.69) M7 11 0.88±0.42 7(63.64) 骨髓原始细胞 -2.643/0.010 6.124/0.013 <50% 43 0.68±0.33 22(51.16) ≥50% 33 0.89±0.36 26(78.79) 细胞遗传学分组 17.234/<0.001 5.667/0.021 良好核型组 29 0.67±0.34 12(41.38) 中等核型组 20 0.71±0.37 19(95.00) 不良核型组 27 0.85±0.36 17(62.96) FAB分型: 法国(France)、美国(American)和英国(Britain)等三国血细胞形态学专家讨论、制订的
关于急性白血病的分型诊断标准。表 4 WT1基因联合FCM-MRD对AML患儿预后的预测效能
指标 曲线下面积 95%CI 敏感度/% 特异度/% 截断值 约登指数 WT1 0.571* 0.452~0.684 41.67 80.00 >0.775 0.217 FCM-MRD 0.751* 0.639~0.843 77.78 72.50 — 0.503 联合诊断 0.882 0.788~0.945 88.89 87.50 — 0.764 与联合诊断比较, *P<0.05。 表 5 WT1基因、FCM-MRD阳性率与FLT3 ITD/TKD突变的相关性分析
指标 FLT3 ITD突变 FLT3 TKD突变 FLT3 ITD/TKD双突变 r P r P r P WT1基因 0.122 0.062 0.221 0.059 0.198 0.060 FCM-MRD阳性率 0.210 0.059 0.111 0.102 0.144 0.078 -
[1] POLLYEA D A, BIXBY D, PERL A, et al. NCCN guidelines insights: acute myeloid leukemia, version 2. 2021[J]. J Natl Compr Canc Netw, 2021, 19(1): 16-27. doi: 10.6004/jnccn.2021.0002
[2] LONG N A, GOLLA U, SHARMA A, et al. Acute myeloid leukemia stem cells: origin, characteristics, and clinical implications[J]. Stem Cell Rev Rep, 2022, 18(4): 1211-1226. doi: 10.1007/s12015-021-10308-6
[3] 吴秀继, 王永卿, 杨晓阳, 等. 急性期蛋白对急性髓系白血病患者预后的预测价值[J]. 中国实验血液学杂志, 2022, 30(4): 1086-1093. [4] ZHAI Y N, SINGH P, DOLNIK A, et al. Longitudinal single-cell transcriptomics reveals distinct patterns of recurrence in acute myeloid leukemia[J]. Mol Cancer, 2022, 21(1): 166. doi: 10.1186/s12943-022-01635-4
[5] AITKEN M J L, RAVANDI F, PATEL K P, et al. Prognostic and therapeutic implications of measurable residual disease in acute myeloid leukemia[J]. J Hematol Oncol, 2021, 14(1): 137. doi: 10.1186/s13045-021-01148-5
[6] VONK C M, AL HINAI A S A, HANEKAMP D, et al. Molecular minimal residual disease detection in acute myeloid leukemia[J]. Cancers, 2021, 13(21): 5431. doi: 10.3390/cancers13215431
[7] TAGA T, TANAKA S, HASEGAWA D, et al. Post-induction MRD by FCM and GATA1-PCR are significant prognostic factors for myeloid leukemia of Down syndrome[J]. Leukemia, 2021, 35(9): 2508-2516. doi: 10.1038/s41375-021-01157-w
[8] CHAPUIS A G, EGAN D N, BAR M, et al. T cell receptor gene therapy targeting WT1 prevents acute myeloid leukemia relapse post-transplant[J]. Nat Med, 2019, 25(7): 1064-1072. doi: 10.1038/s41591-019-0472-9
[9] 王平, 熊昊, 李建新, 等. CCLG-AML-2015方案治疗儿童急性髓系白血病的临床分析[J]. 中国实验血液学杂志, 2022, 30(2): 373-380. [10] 张丽, 邹尧, 艾晓非, 等. 儿童TCF3-PBX1+急性淋巴细胞白血病中微小残留病与预后的相关性[J]. 中国实验血液学杂志, 2020, 28(6): 1831-1836. [11] CREUTZIG U, KASPERS G J L. Revised recommendations of the international working group for diagnosis, standardization of response criteria, treatment outcomes, and reporting standards for therapeutic trials in acute myeloid leukemia[J]. J Clin Oncol, 2004, 22(16): 3432-3433. doi: 10.1200/JCO.2004.99.116
[12] 赵明一, 李嘉华, 江华. 儿童急性髓系白血病造血干细胞移植后复发的预防和治疗[J]. 临床儿科杂志, 2023, 41(3): 167-174. [13] 司君齐, 田晨. 急性髓系白血病细胞与骨髓基质细胞相互作用的研究进展[J]. 中国肿瘤临床, 2023, 50(2): 88-91. [14] 娄典, 刘利, 严学倩, 等. 异基因造血干细胞移植治疗难治/复发急性髓系白血病的疗效及预后因素分析[J]. 中国实验血液学杂志, 2022, 30(5): 1577-1585. [15] PATKAR N, KAKIRDE C, SHAIKH A F, et al. Clinical impact of panel-based error-corrected next generation sequencing versus flow cytometry to detect measurable residual disease (MRD) in acute myeloid leukemia (AML)[J]. Leukemia, 2021, 35(5): 1392-1404. doi: 10.1038/s41375-021-01131-6
[16] AUGSBERGER C, HÄNEL G, XU W, et al. Targeting intracellular WT1 in AML with a novel RMF-peptide-MHC-specific T-cell bispecific antibody[J]. Blood, 2022, 139(13): 2086-2087. doi: 10.1182/blood.2022015672
[17] HAJDU B, HUNYADI-GULYÁS É, KATO K, et al. Zinc binding of a Cys2His2-type zinc finger protein is enhanced by the interaction with DNA[J]. J Biol Inorg Chem, 2023, 28(3): 301-315. doi: 10.1007/s00775-023-01988-1
[18] BELALI T, WODI C, CLARK B, et al. WT1 activates transcription of the splice factor kinase SRPK1 gene in PC3 and K562 cancer cells in the absence of corepressor BASP1[J]. Biochim Biophys Acta Gene Regul Mech, 2020, 1863(12): 194642. doi: 10.1016/j.bbagrm.2020.194642
[19] STEGER B, FLORO L, AMBERGER D C, et al. WT1, PRAME, and PR3 mRNA expression in acute myeloid leukemia (AML)[J]. J Immunother, 2020, 43(6): 204-215. doi: 10.1097/CJI.0000000000000322
[20] KREUTMAIR S, PFEIFER D, WATERHOUSE M, et al. First-in-human study of WT1 recombinant protein vaccination in elderly patients with AML in remission: a single-center experience[J]. Cancer Immunol Immunother, 2022, 71(12): 2913-2928. doi: 10.1007/s00262-022-03202-8
[21] 王卫国. 急性白血病微小残留病检测方法临床应用的研究进展[J]. 山东医药, 2017, 57(38): 110-113. [22] PATKAR N, KAKIRDE C, BHANSHE P, et al. Utility of immunophenotypic measurable residual disease in adult acute myeloid leukemia-real-world context[J]. Front Oncol, 2019, 9: 450. doi: 10.3389/fonc.2019.00450




 下载:
下载:

 苏公网安备 32100302010246号
苏公网安备 32100302010246号
