Causal relationship between gastroesophageal reflux disease and chronic obstructive pulmonary disease based on Mendelian randomization analysis
-
摘要:目的
基于双向两样本孟德尔随机化(MR)方法分析胃食管反流病(GERD)与慢性阻塞性肺疾病(COPD)的因果关系。
方法从全基因组关联研究(GWAS)中获取GERD与COPD的遗传变异信息, 并以此作为工具变量。采用逆方差加权法(IVW)、加权中位数法和MR-Egger回归分析法进行MR分析,并通过敏感性分析验证结果的稳健性。
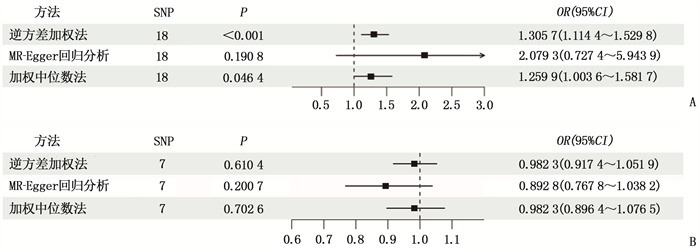
结果遗传预测的GERD与COPD发生风险具有显著正相关性,而COPD与GERD发生风险无统计学关联。正向IVW结果显示比值比(OR)=1.305 7, 95%置信区间(95%CI)为1.114 4~1.529 8, P=0.000 9; 逆向IVW结果显示OR=0.982 3, 95%CI为0.917 4~1.051 9, P=0.610 4。敏感性分析未发现任何潜在偏倚。
结论MR分析显示GERD是COPD的一个风险因子,治疗GERD可能有助于预防或延缓COPD的进展。
Abstract:ObjectiveTo analyze the causal relationship between gastroesophageal reflux disease (GERD) and chronic obstructive pulmonary disease (COPD) based on the bidirectional two-sample Mendelian randomization (MR).
MethodsGenetic variation information of GERD and COPD was obtained from Genome-Wide Association Studies (GWAS) and used as instrumental variables. Inverse variance-weighted (IVW), weighted median and MR-Egger methods were used for MR analysis, and sensitivity analysis was performed to validate the robustness of the results.
ResultsA significant positive correlation was observed between genetically predicted GERD and the incidence risk of COPD, but there was no statistical association between COPD and the incidence risk of GERD. Positive IVW result showed that the odds ratio (OR) was 1.305 7, the 95% confidence interval (95%CI) was 1.114 4 to 1.529 8, and the P value was 0.000 9; the reverse IVW result showed that the OR was 0.982 3, the 95%CI was 0.917 4 to 1.051 9, and the P value was 0.610 4. Sensitivity analysis did not find any potential bias.
ConclusionMR analysis shows that GERD is a risk factor for COPD, and treating GERD may help prevent or delay the progression of COPD.
-
原发性干燥综合征(pSS)是慢性炎症性自身免疫性疾病干燥综合征(SS)的一种类型,不合并其他自身免疫性疾病,在结缔组织疾病中占比较高,并由淋巴细胞介导,会导致患者唾液腺、泪腺等外分泌腺体功能减退或丧失,表现出口干、眼干等干燥症状,但其发病机制尚不完全清楚,可能与遗传、感染、内分泌等因素有关[1-3]。研究[4]报道,抗干燥综合征抗原A(SSA)抗体、抗干燥综合征抗原B(SSB)抗体、抗核抗体(ANA)是pSS最常见的自身抗体,其存在是诊断pSS的主要依据之一,与pSS病情显著相关。
BTB/POZ结构域蛋白7(BTBD7)是近年来新发现的上皮间质转化调控的关键因子,能够降低上皮钙黏素(E-cadherin)表达,进而破坏细胞间的黏附关系,促进恶性肿瘤的浸润、转移[5-6]。有研究[7-8]发现,基质金属蛋白酶-9(MMP-9)在自身免疫性疾病中发挥重要作用,其异常升高会造成细胞外基质、基底膜组织损伤,破坏细胞间的黏附关系,导致淋巴细胞浸润侵袭性增强。目前研究[9]发现MMP-9在pSS中存在异常表达,但BTBD7在pSS中的表达情况尚缺乏研究。本研究检测pSS患者唇腺组织中BTBD7、MMP-9表达水平,并分析二者与pSS患者自身抗体ANA、抗SSA抗体、抗SSB抗体的关系,现将结果报告如下。
1. 资料与方法
1.1 一般资料
选取2016年9月—2020年10月在本院首次诊断为pSS的46例患者唇腺组织为pSS组,其中女44例,男2例,年龄27~76岁,平均(51.36±8.74)岁,均已发生唇腺淋巴细胞浸润,尚未接受治疗。另选取同期怀疑为pSS但最后排除诊断的46例口干燥症患者的唇腺组织为对照组,其中女45例,男1例,年龄31~80岁,平均(52.44±9.35)岁。2组患者性别、年龄比较,差异无统计学意义(P>0.05), 具有可比性。所有组织样本离体后立刻用生理盐水清洗、液氮速冻,然后置于-70 ℃低温冰箱中长期保存。纳入标准: ①符合2016年美国风湿病学会/欧洲抗风湿病联盟制定的pSS分类标准者[10]; ②本研究方案经本院伦理委员会审核通过后实施; ③所有受试者均知晓此次诊治方案,并自愿签署知情同意书。排除标准: ①合并高血压、糖尿病、丙型肝炎、结节病、器官功能异常及其他自身免疫性疾病者; ②有头颈部放疗史者; ③处于妊娠期、哺乳期者; ④中途退出研究者。
1.2 主要试剂与仪器
TRIzol试剂、SYBR Green PCR master mix(货号: 15596026、4312704)购自美国Invitrogen; 逆转录试剂盒(货号: 205111)购自德国QIAGEN; RIPA裂解液(货号: 28192)购自加拿大Norgen Biotek; BCA试剂盒(货号: 701780-480)购自美国Cayman; 兔抗人一抗BTBD7抗体、MMP-9抗体、GAPDH抗体,HRP标记的羊抗兔IgG二抗(货号: ab154685、ab38898、ab245355、ab6271)购自abcam公司; ANA检测试剂盒(货号: H300L)购自美国SCIMEDX; 抗核抗体谱(IgG)检测试剂盒(货号: DL 1590-1601-1 G)购自欧蒙医学诊断(中国)有限公司; ECL试剂盒(货号: AS16-ECL-SN)购自瑞典Agrisera。荧光定量PCR仪(型号: ABI 7500)购自美国Applied Biosystems; 凝胶成像系统(型号: MG8000)购自美国Thmorgan; 荧光显微镜(型号: 80i)购自尼康公司; 免疫印迹仪(型号: EURO Blot MasterⅡ)购自欧蒙公司。
1.3 唇腺组织中BTBD7、MMP-9的mRNA及蛋白表达水平检测
将2组的唇腺组织从冰箱中取出,在冰上解冻,分为2份。先取1份样本,加Trizol匀浆,提取总RNA, 测定RNA纯度、浓度合格后,使用逆转录试剂盒在PCR仪上合成cDNA,参照SYBR Green PCR master mix配制反应体系后,在荧光定量PCR仪上扩增,以GAPDH为内参,采用2-△△Ct法表示BTBD7 mRNA、MMP-9 mRNA水平,其中Ct值为扩增产物荧光信号达临界阈值时的循环数, △Ct=Ct待测基因-Ct内参基因, △△Ct=△Ct测试组织中待测基因-△Ct对照组织中待测基因。引物序列: ① BTBD7上游为5′-CTGAGCCACTGACAGGAGAGG-3′, 下游为5′-GATCCAGCAGCCTCTTTTCATCC-3′; ② MMP-9上游为5′-ATCCAAGGCCAATCCTACT-3′, 下游为5′-CGTCGAGTCAGCTCGGGT-3′; ③ GAPDH上游为5′-GCACCGTCAAGGCTGAGAAC-3′, 下游为5′-TGGTGAAGACGCCAGTGGA-3′。
再另取1份样本,加入含1 mmol/L蛋白酶抑制剂PMSF的预冷RIPA裂解液,将组织研磨匀浆、充分裂解, 12 000×g离心5 min, 分离上清液(即总蛋白),用BCA试剂盒对总蛋白进行定量。各样本取总蛋白40 μg, 加入上样缓冲液,用沸水煮沸5 min, 将总蛋白充分变性,进行10% SDS-PAGE凝胶电泳将目的蛋白分离,然后将目的蛋白转印到PVDF膜上; 在室温下用5%脱脂奶粉封闭2 h, 按比例加入一抗稀释液(BTBD7抗体、MMP-9抗体、GAPDH抗体,均为1∶1 000稀释)在4 ℃下孵育过夜,PBS洗涤3次,加入二抗稀释液(HRP标记的羊抗兔IgG抗体, 1∶1 500稀释)室温下孵育1 h, PBS洗涤3次,加入ECL显色液显色,凝胶成像仪下观察、扫描图像。采用Image J软件测定各条带的灰度值,将目的蛋白与GAPDH灰度值的比值作为目的蛋白表达量。
1.4 自身抗体指标
收集所有pSS患者的检验科原始数据,记录并整理血清自身抗体ANA、抗SSA抗体、抗SSB抗体的数据,其中ANA检测采用间接免疫荧光法,具体操作严格按照ANA检测试剂盒、荧光显微镜操作步骤执行,抗SSA抗体、抗SSB抗体检测采用线性免疫印迹法,具体操作严格按照IgG检测试剂盒、免疫印迹仪操作步骤执行。根据数据分析结果将46例pSS患者分为抗SSA抗体阴性22例与抗SSA抗体阳性24例,抗SSB抗体阴性34例与抗SSB抗体阳性12例,以及ANA阴性4例与ANA阳性42例。
1.5 统计学方法
采用SPSS 19.0软件对实验数据进行统计学分析。计量资料均呈正态分布,采用均数±标准差描述,组间比较行t检验; 采用Pearson相关分析法分析pSS患者唇腺组织中BTBD7蛋白表达水平与MMP-9蛋白表达水平的相关性。P<0.05为差异有统计学意义。
2. 结果
2.1 2组患者唇腺组织中BTBD7、MMP-9的mRNA及蛋白表达水平比较
与对照组相比, pSS组患者唇腺组织中BTBD7、MMP-9的mRNA及蛋白表达水平较高,差异有统计学意义(P<0.05), 见表 1。
表 1 2组患者唇腺组织中BTBD7、MMP-9的mRNA及蛋白表达水平比较(x±s)组别 n BTBD7 mRNA MMP-9 mRNA BTBD7/GAPDH MMP-9/GAPDH 对照组 46 1.00±0 1.00±0 0.34±0.05 0.27±0.06 pSS组 46 1.79±0.15* 2.14±0.16* 0.89±0.08* 0.93±0.12* BTBD7: BTB/POZ结构域蛋白7; MMP-9: 基质金属蛋白酶-9。与对照组比较, *P<0.05。 2.2 pSS患者唇腺组织中BTBD7、MMP-9的mRNA及蛋白表达水平与血清自身抗体的关系
在pSS患者的抗SSA抗体、抗SSB抗体以及ANA的检测结果中,各抗体阳性者唇腺组织中BTBD7、MMP-9的mRNA及蛋白表达水平均高于阴性者,差异均有统计学意义(P<0.05), 见表 2。
表 2 不同血清自身抗体结果的pSS患者唇腺组织中BTBD7、MMP-9的mRNA及蛋白表达水平比较(x±s)抗体表达 n BTBD7 mRNA MMP-9 mRNA BTBD7/GAPDH MMP-9/GAPDH 抗SSA抗体阴性 22 1.59±0.12 1.98±0.14 0.82±0.07 0.85±0.09 抗SSA抗体阳性 24 1.97±0.13* 2.29±0.15* 0.96±0.11* 1.01±0.13* 抗SSB抗体阴性 34 1.72±0.15 2.05±0.15 0.84±0.08 0.89±0.11 抗SSB抗体阳性 12 1.98±0.10* 2.38±0.11* 1.05±0.10* 1.06±0.10* ANA阴性 7 1.54±0.09 1.88±0.10 0.64±0.06 0.70±0.08 ANA阳性 39 1.84±0.14* 2.19±0.14* 0.93±0.12* 0.97±0.13* SSA: 干燥综合征抗原A; SSB: 干燥综合征抗原B; ANA: 抗核抗体。与同种抗体阴性者比较, *P<0.05。 2.3 pSS患者唇腺组织中BTBD7蛋白表达水平与MMP-9蛋白表达水平的相关性
相关性分析结果显示, pSS患者唇腺组织中BTBD7蛋白表达水平与MMP-9蛋白表达水平呈显著正相关(r=0.493, P<0.05)。见图 1。
3. 讨论
研究[11-12]发现,SS发病是因机体自身免疫过度应答而引起外分泌腺存在大量淋巴细胞、浆细胞浸润,致使腺体细胞被大量破坏,表现出口干、眼干、发热、乏力等一系列临床症状[13]。SS可分为pSS和继发性SS, 其中pSS不合并其他自身免疫性疾病,而继发性SS则会同时表现出SS及其他疾病的症状[14]。pSS主要侵犯唇腺和泪腺,病理性变化为大量淋巴细胞浸润、组织间质纤维化及腺体组织萎缩等,临床表现为口唇干燥、口渴、难以进食干硬食物、舌体干裂等,严重影响患者的身体健康[15-17]。
BTBD7基因定位于染色体14q32.12区域,约有1 233 bp, 能引导上皮细胞发生“分支形态”改变过程,是近年来新发现的癌基因,在调控肿瘤细胞发生上皮-间质转化方面具有重要功能[18]。CHEN B等[5]研究显示,BTBD7可促进前列腺癌的增殖、侵袭及上皮-间质转化,加速肿瘤进展。杜望磊等[19]研究表明, E-cadherin在pSS患者唇腺组织中呈异常低表达,其表达情况与病理等级相关,参与pSS发病机制,推测BTBD7可能通过影响E-cadherin表达在pSS发病中发挥作用。本研究结果显示, pSS患者唇腺组织中BTBD7 mRNA及BTBD7蛋白表达水平较口干燥症患者显著升高,提示BTBD7参与pSS发生过程。由于E-cadherin能够阻止淋巴细胞的侵袭,推测BTBD7可能在pSS发病过程中发挥调控上皮-间质转化过程的作用,能增强淋巴细胞的侵袭性,促进淋巴细胞浸润发生。pSS自身抗体ANA、抗SSA抗体、抗SSB抗体可反映pSS病情,其阳性结果对pSS具有较高的诊断价值。本研究结果显示,抗SSA抗体阳性、抗SSB抗体阳性以及ANA阳性的pSS患者唇腺组织中BTBD7蛋白表达水平较上述抗体阴性者显著升高,提示BTBD7表达与pSS患者血清ANA、抗SSA抗体、抗SSB抗体水平关系密切,可反映pSS病情。
pSS发病伴随大量淋巴细胞浸润,而细胞的浸润过程与细胞间的黏附关系有密切联系。MMP-9是基质金属蛋白酶家族成员,其主要作用是降解细胞外基质及基底膜,打破细胞发生转移、浸润的天然组织屏障,促进细胞的侵袭、转移、浸润过程[20]。杜望磊等[19]研究发现,MMP-9在pSS患者唇腺组织中高表达,与病理等级相关,可能参与pSS的致病过程。AOTA K等[21]研究发现, MMP-9在pSS患者唇唾液腺中表达上调,可调节CXC基序趋化因子10表达及活性,有望成为pSS的新型疗法。SHAH N R等[22]研究也表明, MMP-9在pSS患者唇唾液腺中的mRNA及蛋白水平均显著上调。本研究结果显示, pSS患者唇腺组织中MMP-9 mRNA及MMP-9蛋白表达水平较口干燥症患者显著升高,提示MMP-9参与pSS的发生过程; 进一步比较发现, ANA阳性、抗SSA抗体阳性以及抗SSB抗体阳性的pSS患者唇腺组织中MMP-9蛋白表达水平均显著高于对应抗体阴性患者,提示MMP-9可影响pSS患者自身免疫状况。本研究相关性分析结果表明, pSS患者唇腺组织中BTBD7蛋白水平与MMP-9蛋白水平呈正相关,表明二者可能共同影响pSS患者的自身免疫状况。
综上所述, pSS患者唇腺组织中BTBD7、MMP-9均呈高表达,且与自身抗体的抗SSA抗体、抗SSB抗体、ANA表达密切相关,可能共同影响患者自身免疫状况。
-
表 1 工具变量信息
暴露 单核苷酸多态性 效应位点 其他位点 P Beta SE F COPD rs11846838 A G 4.67E-08 0.062 2 0.011 4 29.850 8 rs12449174 A G 2.91E-08 0.148 6 0.026 8 30.767 2 rs13270042 G A 2.28E-08 0.098 7 0.017 7 31.242 3 rs28929474 T C 2.06E-18 0.326 6 0.037 3 76.635 5 rs3025383 C T 2.33E-08 -0.084 5 0.015 1 31.195 0 rs7671167 T C 1.88E-08 0.062 9 0.011 2 31.611 1 rs8089390 T C 2.17E-08 -0.070 4 0.012 6 31.332 0 GERD rs111472920 T G 4.47E-08 0.098 7 0.018 0 30.066 9 rs12706746 A G 4.24E-09 0.036 9 0.006 3 34.306 1 rs12939066 T C 3.13E-11 0.041 5 0.006 2 44.803 6 rs13167137 T G 2.82E-08 -0.032 8 0.005 9 30.906 1 rs1473115 T C 3.95E-10 0.039 6 0.006 3 39.510 2 rs15071 T C 1.01E-08 -0.042 8 0.007 5 32.566 0 rs1858828 T G 3.23E-08 0.032 7 0.005 9 30.717 9 rs3072 T C 1.86E-08 -0.034 5 0.006 1 31.987 4 rs62046253 T C 1.30E-08 -0.035 2 0.006 2 32.233 1 rs62442944 T G 3.49E-08 0.041 8 0.007 6 30.250 0 rs6683411 A G 4.82E-08 0.032 4 0.005 9 30.156 9 rs6710685 T C 1.96E-09 0.039 1 0.006 5 36.184 9 rs6762606 T C 4.18E-08 -0.035 9 0.006 5 30.504 4 rs6809836 A G 3.70E-09 0.038 3 0.006 5 34.719 3 rs6991878 T C 2.71E-08 -0.033 8 0.006 1 30.702 5 rs72704785 A G 6.81E-09 0.045 9 0.007 9 33.757 6 rs7552188 T C 1.07E-08 0.041 3 0.007 2 32.903 0 rs769671 T C 9.28E-10 -0.038 5 0.006 3 37.345 7 表 2 敏感性分析结果
暴露 结局 SNPs/个 异质性检验 MR-Egger多效性检验 MR-PRESSO离群值检测 Q P 截距值 P 残差平方和 P 离群SNP GERD COPD 18 17.926 12 0.393 5 -0.017 9 0.392 7 20.311 47 0.404 9 无 COPD GERD 7 5.513 072 0.479 9 0.009 4 0.222 2 7.259 081 0.524 4 无 GERD: 胃食管反流病; COPD: 慢性阻塞性肺疾病; SNPs: 单核苷酸多态性; MR-PRESSO: 孟德尔随机多态性残差和离群值。 -
[1] MARET-OUDA J, MARKAR S R, LAGERGREN J. Gastroesophageal Reflux Disease: A Review[J]. Jama, 2020, 324(24): 2536-2547. doi: 10.1001/jama.2020.21360
[2] 燕晶晶, 李颖, 于明娟, 等. 胃食管反流病的诊治研究进展[J]. 现代中西医结合杂志, 2023, 32(9): 1309-1314. doi: 10.3969/j.issn.1008-8849.2023.09.030 [3] RAHERISON C, GIRODET P O. Epidemiology of COPD[J]. Eur Respir Rev, 2009, 18(114): 213-221. doi: 10.1183/09059180.00003609
[4] CHEN Y. Gastroesophageal reflux disease and non-digestive tract diseases[J]. Expert Rev Gastroenterol Hepatol, 2015, 9(5): 685-692. doi: 10.1586/17474124.2015.1012495
[5] 樊建勇, 秦燕. 慢性阻塞性肺疾病与胃食管反流病相互作用的研究进展[J]. 中国呼吸与危重监护杂志, 2020, 19(01): 88-91. [6] GARCíA RODRíGUEZ L A, RUIGóMEZ A, MARTíN-MERINO E, et al. Relationship between gastroesophageal reflux disease and COPD in UK primary care[J]. CHEST, 2008, 134(6): 1223-1230. doi: 10.1378/chest.08-0902
[7] LICCARDI G, SALZILLO A, CALZETTA L, et al. Gastroesophageal reflux and COPD exacerbations: Is cholinergic-mediated oesophago-bronchial reflex a possible link[J]. RESPIROLOGY, 2016, 21(8): 1496-1497. doi: 10.1111/resp.12896
[8] AN J, GHARAHKHANI P, LAW M H, et al. Gastroesophageal reflux GWAS identifies risk loci that also associate with subsequent severe esophageal diseases[J]. Nat Commun, 2019, 10(1): 4219. doi: 10.1038/s41467-019-11968-2
[9] KURKI M I, KARJALAINEN J, PALTA P, et al. FinnGen provides genetic insights from a well-phenotyped isolated population[J]. NATURE, 2023, 613(7944): 508-518. doi: 10.1038/s41586-022-05473-8
[10] ZAGKOS L, DIB M J, PINTO R, et al. Associations of genetically predicted fatty acid levels across the phenome: A mendelian randomisation study[J]. PLoS Med, 2022, 19(12): e1004141. doi: 10.1371/journal.pmed.1004141
[11] CHEN X, KONG J, DIAO X, et al. Depression and prostate cancer risk: A Mendelian randomization study[J]. Cancer Med, 2020, 9(23): 9160-9167. doi: 10.1002/cam4.3493
[12] WANG S, ZHU H, PAN L, et al. Systemic inflammatory regulators and risk of acute-on-chronic liver failure: A bidirectional mendelian-randomization study[J]. Front Cell Dev Biol, 2023, 11: 1125233. doi: 10.3389/fcell.2023.1125233
[13] 张晓莉, 李晗瑜, 郑松柏. 重视老年人胃食管反流病及其相关疾病的诊治[J]. 国际老年医学杂志, 2023, 44(4): 385-389. [14] LEE A S, LEE J S, HE Z, et al. Reflux-Aspiration in Chronic Lung Disease[J]. Ann Am Thorac Soc, 2020, 17(2): 155-164. doi: 10.1513/AnnalsATS.201906-427CME
[15] LEE A S, RYU J H. Aspiration Pneumonia and Related Syndromes[J]. Mayo Clin Proc, 2018, 93(6): 752-762. doi: 10.1016/j.mayocp.2018.03.011
[16] SAKAE T M, PIZZICHINI M M, TEIXEIRA P J, et al. Exacerbations of COPD and symptoms of gastroesophageal reflux: a systematic review and meta-analysis[J]. J Bras Pneumol, 2013, 39(3): 259-271. doi: 10.1590/S1806-37132013000300002
[17] 李路, 杨阳, 孙亚男, 等. 慢性阻塞性肺疾病急性加重期患者心功能不全相关危险因素及其与预后的关系[J]. 实用临床医药杂志, 2021, 25(15): 43-48, 52. doi: 10.7619/jcmp.20211756 [18] LI X, LIN S, WANG Z, et al. Gastroesophageal reflux disease and chronic cough: A possible mechanism elucidated by ambulatory pH-impedance-pressure monitoring[J]. Neurogastroenterol Motil, 2019, 31(12): e13707. doi: 10.1111/nmo.13707
[19] CIBELLA F, CUTTITTA G. Nocturnal asthma and gastroesophageal reflux[J]. Am J Med, 2001, 111(Suppl 8A): 31s-36s.
[20] 阿卜杜喀迪尔·阿卜杜热合曼, 柔孜麦麦提·艾则孜, 合贝尔江·力提甫. 胃食管反流病相关呼吸系统疾病研究进展[J]. 新疆医学, 2022, 52(2): 207-210. [21] REYNOLDS C J, DEL GRECO M F, ALLEN R J, et al. The causal relationship between gastro-oesophageal reflux disease and idiopathic pulmonary fibrosis: a bidirectional two-sample Mendelian randomisation study[J]. Eur Respir J, 2023, 61(5): 2201585. doi: 10.1183/13993003.01585-2022
[22] ZHU J, ZHOU D, WANG J, et al. A Causal Atlas on Comorbidities in Idiopathic Pulmonary Fibrosis: A Bidirectional Mendelian Randomization Study[J]. CHEST, 2023, 164(2): 429-440. doi: 10.1016/j.chest.2023.02.038
[23] LEE A L, GOLDSTEIN R S. Gastroesophageal reflux disease in COPD: links and risks[J]. Int J Chron Obstruct Pulmon Dis, 2015, 10: 1935-1949.
[24] BECKER B S, BURAKOFF R. The effect of verapamil on the lower esophageal sphincter pressure in normal subjects and in achalasia[J]. Am J Gastroenterol, 1983, 78(12): 773-775.
[25] HONGO M, TRAUBE M, MCALLISTER R G JR, et al. Effects of nifedipine on esophageal motor function in humans: correlation with plasma nifedipine concentration[J]. GASTROENTEROLOGY, 1984, 86(1): 8-12. doi: 10.1016/0016-5085(84)90583-3
[26] BERQUIST W E, RACHELEFSKY G S, KADDEN M, et al. Effect of theophylline on gastroesophageal reflux in normal adults[J]. J Allergy Clin Immunol, 1981, 67(5): 407-411. doi: 10.1016/0091-6749(81)90087-7
[27] STEIN M R, TOWNER T G, WEBER R W, et al. The effect of theophylline on the lower esophageal sphincter pressure[J]. Ann Allergy, 1980, 45(4): 238-241.
[28] JOHANNESSON N, ANDERSSON K E, JOELSSON B, et al. Relaxation of lower esophageal sphincter and stimulation of gastric secretion and diuresis by antiasthmatic xanthines. Role of adenosine antagonism[J]. Am Rev Respir Dis, 1985, 131(1): 26-30.
[29] 顾章明, 孙丽. 氟哌噻吨美利曲辛片联合舒肝解郁胶囊对难治性胃食管反流患者疗效及焦虑、抑郁状态的影响[J]. 实用临床医药杂志, 2019, 23(12): 32-35. doi: 10.7619/jcmp.201912010 [30] 殷江龙, 彭卓嵛, 石林韬, 等. 基于Citespace中医药治疗胃食管反流病相关研究的可视化分析[J]. 实用临床医药杂志, 2022, 26(22): 65-71. doi: 10.7619/jcmp.20221681




 下载:
下载:

 苏公网安备 32100302010246号
苏公网安备 32100302010246号
