Chinese version of the Nine-Item Avoidant/Restrictive Food Intake Disorder Scale in patients with inflammatory bowel disease: a test of reliability and validity
-
摘要:目的
检验中文版逃避与限制性饮食障碍量表(NIAS)在炎症性肠病患者中的信度和效度。
方法采用便利抽样的方法, 选取江苏省2所三甲医院炎症性肠病诊疗中心304例患者作为研究对象,采用一般资料调查表、NIAS、与食物相关的生活满意度量表(SWFL)对患者进行调查。对量表进行项目分析(区分度分析法、相关系数法)、总量表及分量表的信度分析(Cronbach's α系数)。采用探索性因子分析、验证性因子分析、效标关联度、聚合效度和区分效度检验量表的效度。
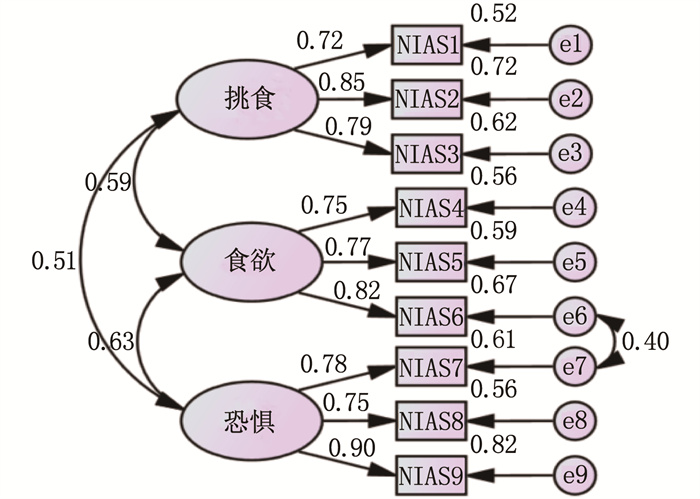
结果中文版NIAS共9个条目,包括挑食、食欲、恐惧3个维度; 验证性因素分析显示3因子模型拟合指数良好[χ2/df=2.340, 近似误差均方根(RMSEA)=0.078, 标准化残差均方根(SRMR)=0.046, 增值拟合指数(IFI)=0.969, 比较拟合指数(CFI)=0.969, 规范拟合指数(NFI)=0.948, 拟合优度指数(GFI)=0.951, 非规范拟合指数(TLI)=0.951]; 中文版NIAS总分和效标量表SWFL相关系数为-0.353, 具有较强的关联性; 量表各维度的聚合效度CR值为0.821~0.855, AVE分别为0.606(食欲)、0.621(挑食)、0.664(恐惧)。中文版NIAS总的Cronbach's α系数为0.82, 挑食、食欲、恐惧维度的Cronbach's α系数分别为0.87、0.71、0.92, 说明中文版NIAS具有较好的内部一致性和稳定性。
结论中文版NIAS具有良好的信效度,可用于评估炎症性肠病(IBD)患者的逃避与限制性饮食障碍行为。
-
关键词:
- 炎症性肠病 /
- 逃避与限制性饮食障碍 /
- 信度 /
- 效度 /
- 量表
Abstract:ObjectiveTo test the reliability and validity of the Chinese version of the Nine-Item Avoidant/Restrictive Food Intake Disorder Scale (NIAS) in patients with inflammatory bowel disease (IBD).
MethodsBased on convenience sampling method, 304 patients from the Treatment Center for Inflammatory Bowel Disease of two Grade Ⅲ Level hospitals A in Jiangsu Province were selected as the research objects, and they were investigated by a general information questionnaire, NIAS, and the Satisfaction with Food-Related Life (SWFL). Item analysis (discrimination analysis, correlation coefficient) and reliability analysis of the total scale and subscales (Cronbach's α coefficient) were performed. Exploratory factor analysis, confirmatory factor analysis, criterion-related validity, convergent validity, and discriminant validity were used to test the validity of the scale.
ResultsThe Chinese version of NIAS contained 9 items, including 3 subscales of picky eating, appetite and fear; the confirmatory factor analysis indicated a good construct validity in 3-factor model[χ2/df=2.340, root mean square error of approximation (RMSEA)=0.078, standardized root mean square residual (SRMR)=0.046, incremental fit index (IFI)=0.969, comparative fit index (CFI)=0.969, normed fit index (NFI)=0.948, goodness of fit index (GFI)=0.951, the Tucker-Lewis index (TLI)=0.951]; the correlation coefficient between the total score of the Chinese version of NIAS and the SWFL scale was -0.353, indicating a strong correlation; the aggregated validity CR values for each dimension of the scale were 0.821 to 0.855, and the AVE values were 0.606 for appetite, 0.621 for picky eating, and 0.664 for fear. The total Cronbach's α coefficient of the Chinese version of the NIAS scale was 0.82, and the Cronbach's α coefficients for dimensions of picky eating, appetite and fear were 0.87, 0.71 and 0.92 respectively, indicating the Chinese version of the NIAS scale had good internal consistency and stability.
ConclusionThe Chinese version of the NIAS scale has good reliability and validity, and can be used to evaluate avoidant and restrictive food intake disorder behaviors in IBD patients.
-
外伤性蛛网膜下腔出血(tSAH)是神经外科常见病之一,致残率及致死率高,预后不良,因此早期干预对蛛网膜下腔出血患者的预后尤为重要[1]。神经元特异性烯醇化酶(NSE)属于细胞能量代谢过程中的一种酶类,由神经细胞分泌,与新生儿缺血缺氧性脑病、脑梗死、脑出血等疾病损伤程度有关,可用于脑损伤预后的评估[2]。目前,关于蛛网膜下腔出血患者外周血不同时点NSE的表达与预后的关系尚不清楚[3-4]。本研究观察tSAH患者外周血中NSE的表达情况及其与预后的关系,旨在为tSAH患者的预后评估提供新的标志物,现报告如下。
1. 资料与方法
1.1 一般资料
选取2019年3月—2020年6月本院接受住院治疗的110例蛛网膜下腔出血患者为研究对象。入选标准: 所有入选患者均为单纯tSAH, 经颅脑CT明确诊断; 无精神疾病者; 受伤至入院24 h内的患者; 未合并其他脏器损伤者; 无恶性肿瘤者。排除标准: 存在血小板减少症等其他出血性疾病者; 患者合并颅脑其他疾病,如动脉瘤、肿瘤等; 孕妇; 合并其他器官恶性肿瘤者。110例tSAH患者中,女29例,男81例; 年龄18~72岁,平均(45.78±12.36)岁; 发病至入院时间20 min~10 h, 平均(3.08±0.02) h。
1.2 方法
患者入院后完善各项检查,如颅脑CT检查及其他常规检查,给予止血、抗感染、护脑、护胃、降颅压、镇静、营养支持、吸氧、监护等对症处理,密切关注各项生命体征变化。
记录CT检查结果, Fisher分级,Morris-Marshall CT分级,高血压、糖尿病、吸烟、饮酒病史,急性生理与慢性健康状况评分Ⅱ(APACHE Ⅱ)评分,格拉斯哥昏迷量表(GCS)评分。检测入院时和治疗后第1、3、7天时血清NSE水平,抽取患者清晨空腹外周静脉血10 mL于抗凝管中, 2 500转/min离心10 min后取上层血清, -70 ℃保存待检。采用酶联免疫吸附测定(ELISA)试剂盒[美国Sigma公司(货号为2018121312)]检测NSE, 严格按照说明书步骤进行操作。
根据出院时格拉斯哥结局量表(GOS)评分将110例患者分为预后良好组(n=70, 4~5分)和预后不良组(n=40, 1~3分); 根据Fisher分级将其分为Ⅰ~Ⅱ级组(n=20)和Ⅲ~Ⅳ级组(n=90); 根据Morris-Marshall CT分级将其分为Ⅰ~Ⅲ级组(n=47)和Ⅳ~Ⅴ级组(n=63)。
1.3 统计学方法
本研究采用SPSS 17.0软件对数据进行处理,计量资料以均数±标准差表示, 2组比较采用t检验,计数资料以[n(%)]表示,组间比较采用χ2检验。采用多因素Logistic回归分析对患者预后影响因素进行分析。采用受试者工作特征(ROC)曲线分析各因素对蛛网膜下腔出血患者预后不良的预测价值。以α=0.05作为检验水准, P < 0.05表示差异有统计学意义。
2. 结果
2.1 预后不良组及预后良好组临床资料比较
预后不良组Fisher分级Ⅲ~Ⅳ级及Morris-Marshall CT分级Ⅳ~Ⅴ级占比高于预后良好组,差异有统计学意义(P < 0.05); 预后不良组收缩压(SBP)、舒张压(DBP)、入院GCS评分低于预后良好组, APACHE Ⅱ评分及入院时NSE水平高于预后良好组,差异有统计学意义(P < 0.05)。见表 1。
表 1 各组临床资料比较(x±s)[n(%)]项目 预后良好组(n=70) 预后不良组(n=40) 年龄/岁 42.34±10.46 55.43±12.45 性别 男 51(72.86) 30(75.00) 女 19(27.14) 10(25.00) 入院时间/h 2.74±0.12 3.04±0.35 血压 SBP/mmHg 124.44±19.35 108.43±13.26 DBP/mmHg 76.72±9.83 60.44±6.51 心率/(次/min) 87.44±9.74 90.46±11.37 入院GCS评分/分 12.61±3.30 7.14±1.36 APACHE Ⅱ评分/分 12.17±4.33 22.88±6.14 Fisher分级 Ⅰ~Ⅱ级 19(27.14) 1(2.50) Ⅲ~Ⅳ级 51(72.86) 39(97.50) Morris-Marshall CT分级 Ⅰ~Ⅲ级 44(62.86) 3(7.50) Ⅳ~Ⅴ级 26(37.14) 37(92.50) 入院时NSE水平/(μg/L) 13.39±5.13 18.33±4.16 SBP: 收缩压; DBP: 舒张压; GCS: 格拉斯哥昏迷量表; APACHE Ⅱ: 急性生理与慢性健康状况评分Ⅱ。 2.2 不同Fisher、Morris-Marshall CT分级NSE水平比较
Fisher分级Ⅲ~Ⅳ级组和Morris-Marshall CT分级Ⅳ~Ⅴ级组患者入院时、治疗后第1天、治疗后第3天及治疗后第7天NSE水平分别高于Fisher分级Ⅰ~Ⅱ级组和Morris-Marshall CT分级Ⅰ~Ⅲ级组,差异有统计学意义(P < 0.05)。见表 2、3。
表 2 不同Fisher分级NSE水平比较(x±s)μg/L 组别 n 入院时 治疗后第1天 治疗后第3天 治疗后第7天 Ⅰ~Ⅱ级组 20 12.35±1.72 11.05±1.05 9.63±0.24 7.64±0.23 Ⅲ~Ⅳ级组 90 20.02±4.51* 18.62±2.64* 16.12±2.07* 11.86±1.58* 与Ⅰ~Ⅱ级组比较, *P < 0.05。 表 3 不同Morris-Marshall CT分级NSE水平比较(x±s)μg/L 组别 n 入院时 治疗后第1天 治疗后第3天 治疗后第7天 Ⅰ~Ⅲ级组 47 11.65±2.07 10.01±1.11 9.24±1.04 6.99±1.04 Ⅳ~Ⅴ级组 63 22.36±6.84* 17.82±3.25* 14.84±3.12* 11.46±0.92* 与Ⅰ~Ⅲ级组比较, *P < 0.05。 2.3 tSAH患者预后不良的多因素Logistic回归分析
多因素Logistic回归分析表明, Fisher分级(Ⅲ~Ⅳ级)、Morris-Marshall CT分级(Ⅳ~Ⅴ级)、SBP(< 100 mmHg)、DBP(< 60 mmHg)、入院GCS评分(< 8分)、APACHE Ⅱ评分(>23分)及入院时NSE水平(>15.5 μg/L)是tSAH患者预后不良的独立危险因素(P < 0.05), 见表 4。
表 4 tSAH患者预后不良的多因素Logistic分析影响因素 回归系数 标准误 Wald值 95%CI P SBP 1.500 0.485 9.536 1.731~11.615 0.002 DBP 0.813 0.312 6.801 1.224~4.161 0.009 APACHE Ⅱ评分 0.064 0.301 4.601 1.057~3.445 0.032 Fisher分级 1.375 0.319 18.637 2.118~7.383 0.001 Morris-Marshall分级 1.762 0.316 31.300 3.138~10.781 <0.001 GCS评分 1.032 0.415 6.189 1.244~6.322 0.013 NSE水平 1.878 0.916 4.197 1.084~39.379 0.040 SBP: 收缩压; DBP: 舒张压; APACHE Ⅱ: 急性生理与慢性健康量表; GCS: 格拉斯哥昏迷量表; NSE: 神经元特异性烯醇化酶。 2.4 ROC曲线分析各指标对tSAH患者预后不良的预测价值
ROC曲线分析结果表明,低血压(SBP < 100 mmHg、DBP < 60 mmHg)、Fisher分级(Ⅲ~Ⅳ级)、Morris-Marshall CT分级(Ⅳ~Ⅴ级)、入院GCS评分(< 8分)、APACHE Ⅱ评分(>23分)及入院时NSE(>15.5 μg/L)预测tSAH患者预后不良的曲线下面积(AUC)分别是0.945、0.960、0.976、0.947、0.958、0.977, 其中NSE预测价值最高。见图 1。
3. 讨论
蛛网膜下腔出血是神经外科常见病之一,致残率、致死率高,预后不良,因此对患者进行早期干预尤为重要。生命体征、GCS评分、APACHE Ⅱ评分及CT检查都可用于预测患者预后[5-8]。但上述指标不能客观反映患者预后,因此寻找一种客观、准确的临床指标对判断蛛网膜下腔出血患者的预后尤为重要[9-10]。
NSE属于细胞能量代谢过程中的一种酶类,由神经细胞分泌,与新生儿缺血缺氧性脑病、脑梗死、脑出血等疾病的损伤程度有关,可用于脑损伤预后的评估,被认为是评估颅脑损伤的特异性实验室标志物[11-13]。颅脑受到撞击后,神经细胞会出现坏死,细胞内NSE释放进入血液,因此检测外周血中NSE含量可用于评估脑损伤程度及预后[14]。研究[15]报道,蛛网膜下腔出血患者血乳酸、儿茶酚胺在发病6 h内出现高峰,之后逐渐降低,术后1 d出现小幅度增高。本研究发现,血清NSE从入院开始逐渐降低,提示tSAH患者NSE水平与应激反应有关。黄铭等[16]研究表明,老年高血压脑出血术后预后恶劣组NSE含量高于预后良好组。研究[17]表明,重症颅脑损伤后12 h内患者的NSE含量高于预后良好患者。PETRASHENKO V A等[18]研究提示,血清NSE含量变化与颅脑损伤患者的CT征象有关,损伤越重NSE含量越高。目前,关于NSE与蛛网膜下腔出血的预后研究鲜有文献报道。本研究结果表明,预后不良组NSE水平高于预后良好组, Fisher分级Ⅲ~Ⅳ级组、Morris-Marshall CT分级Ⅳ~Ⅴ级组患者入院时、治疗后第1、3、7天NSE水平均高于Fisher分级Ⅰ~Ⅱ级组和Morris-Marshall CT分级Ⅰ~Ⅲ级组,表明NSE与tSAH患者的严重程度、预后有关。Morris-Marshall CT分级及Fisher分级是临床上常用的评估蛛网膜下腔出血患者病情严重程度的分级方法,分级越高,病情越重,提示NSE可以作为评估蛛网膜下腔出血患者病情严重程度的血清标志物。
现在研究[19]认为, GCS评分是颅脑损伤预后不良甚至是死亡的危险因素, GCS评分越低,预后越差。研究[20]认为, Morris-Marshall CT分级可用于评价蛛网膜下腔出血的量及部位,与GCS评分密切相关。本研究结果表明,预后不良组不同Fisher分级及Morris-Marshall CT分级患者比率与预后良好组比较,差异有统计学意义(P < 0.05); 预后不良组SBP、DBP、入院GCS评分低于预后良好组, APACHE Ⅱ评分及入院时NSE水平高于预后良好组,差异有统计学意义(P < 0.05)。多因素Logistic回归分析表明, Fisher分级(Ⅲ~Ⅳ级)、Morris-Marshall CT分级(Ⅳ~Ⅴ级)、SBP(< 100 mmHg)、DBP(< 60 mmHg)、入院GCS评分(< 8分)、APACHEⅡ评分(>23分)及入院时NSE水平(>15.5 μg/L)是tSAH患者预后不良的独立危险因素(P < 0.05)。ROC曲线分析结果表明,低血压(SBP < 100 mmHg、DBP < 60 mmHg)、Fisher分级(Ⅲ~Ⅳ级)、Morris-Marshall CT分级(Ⅳ~Ⅴ级)、入院GCS评分(< 8分)、APACHE Ⅱ评分(>23分)及入院时NSE(>15.5 μg/L)预测tSAH患者预后不良的AUC分别为0.945、0.960、0.976、0.947、0.958、0.977, 其中NSE预测价值最高。因此,影响tSAH患者的预后因素较多,机制复杂,有待进一步分析各因素与预后的关系。本研究选取样本量较少,对影响tSAH的预后因素纳入不全,尚需扩大样本量进一步证实。
综上所述, tSAH患者NSE表达水平明显升高,与患者预后不良有关,对患者的预后不良具有较好的预测价值。
-
表 1 中文版NIAS项目分析(x±s)
题项 得分/分 题项与总分相关 决断值 与挑食维度的相关系数 与食欲维度的相关系数 与恐惧维度的相关系数 NIAS1 2.52±1.03 0.549** -3.391** 0.906** — — NIAS2 2.27±0.76 0.641** -3.337** 0.879** — — NIAS3 2.53±0.95 0.649** -3.897** 0.902** — — NIAS4 2.21±0.79 0.631** -4.066** — 0.760** — NIAS5 2.85±0.78 0.644** -4.876** — 0.813** — NIAS6 2.80±0.81 0.664** -5.968** — 0.813** — NIAS7 2.58±0.86 0.715** -8.402** — — 0.888** NIAS8 2.94±0.73 0.638** -6.017** — — 0.932** NIAS9 2.86±0.88 0.653** -5.975** — — 0.933** **在0.01级别(双尾)相关性显著。 表 2 中文版NIAS旋转后因子矩阵
条目 因子1 因子2 因子3 1. 我是个挑食的人 -0.092 0.883 0.149 2. 我不喜欢别人吃的大部分食物 0.125 0.882 0.105 3. 我喜欢且会吃的食物名单比我不吃的食物名单要短 0.054 0.881 0.194 4. 我对吃东西不太感兴趣,我的胃口似乎比别人小 0.086 0.298 0.793 5. 我不得不强迫自己一整天都规律饮食,或者在吃饭时吃足够多的食物 0.272 0.159 0.760 6. 即使当我在吃我真正喜欢的食物时,我也很难在吃饭时吃得足够多 0.698 -0.094 0.548 7. 我避免或推迟进食,因为我害怕肠胃不适、被噎或呕吐 0.824 0.143 0.221 8. 我限制自己只吃某些食物,因为我担心其他食物会引起肠胃不适、被噎或呕吐 0.938 0.053 0.026 9. 我吃小份的食物,因为我害怕肠胃不适、被噎或呕吐 0.933 -0.038 0.169 特征值 42.320 27.195 10.033 累计方差贡献率(%) 42.320 69.515 79.548 表 3 中文版NIAS验证性因子分析结果
项目 参考标准 修正前 修正后 卡方自由度比(χ2/df) <5.000 3.120 2.340 标准化残差均方根(SRMR) <0.050 0.050 0.046 近似误差均方根(RMSEA) <0.080 0.098 0.078 拟合优度指数(GFI) >0.850 0.933 0.951 比较拟合指数(CFI) >0.900 0.949 0.969 非规范拟合指数(TLI) >0.900 0.923 0.951 增值拟合指数(IFI) >0.900 0.949 0.969 规范拟合指数(NFI) >0.900 0.927 0.948 表 4 中文版NIAS的聚合效度值
项目 挑食 食欲 恐惧 挑食 — — — 食欲 0.591 — — 恐惧 0.513 0.630 — CR 0.830 0.821 0.855 AVE 0.621 0.606 0.664 -
[1] LENNARD-JONES J E. Classification of inflammatory bowel disease[J]. Scand J Gastroenterol Suppl, 1989, 170: 2-6, 16-19.
[2] 吴开春, 梁洁, 冉志华, 等. 炎症性肠病诊断与治疗的共识意见(2018年·北京)[J]. 中国实用内科杂志, 2018, 38(9): 796-813. [3] KAPLAN G G. The global burden of IBD: from 2015 to 2025[J]. Nat Rev Gastroenterol Hepatol, 2015, 12(12): 720-727. doi: 10.1038/nrgastro.2015.150
[4] BEN-HORIN S, CASTEELE N V, SCHREIBER S, et al. Biosimilars in Inflammatory Bowel Disease: Facts and Fears of Extrapolation[J]. Clinical Gastroenterology and Hepatology, 2016, 14(12): 1685-1696. doi: 10.1016/j.cgh.2016.05.023
[5] ANANTHAKRISHNAN A N. Epidemiology and risk factors for IBD[J]. Nat Rev Gastroenterol Hepatol, 2015, 12(4): 205-217. doi: 10.1038/nrgastro.2015.34
[6] MARTINEZ-MEDINA M, DENIZOT J, DREUX N, et al. Western diet induces dysbiosis with increased E coli in CEABAC10 mice, alters host barrier function favouring AIEC colonisation[J]. Gut, 2014, 63(1): 116-124. doi: 10.1136/gutjnl-2012-304119
[7] SUGIHARA K, MORHARDT T L, KAMADA N. The role of dietary nutrients in inflammatory bowel disease[J]. Front Immunol, 2019, 9: 3183. doi: 10.3389/fimmu.2018.03183
[8] DE VRIES J H M, DIJKHUIZEN M, TAP P, et al. Patient's dietary beliefs and behaviours in inflammatory bowel disease[J]. Dig Dis, 2019, 37(2): 131-139. doi: 10.1159/000494022
[9] CROOKS B, MISRA R, AREBI N, et al. The dietary practices and beliefs of British South Asian people living with inflammatory bowel disease: a multicenter study from the United Kingdom[J]. Intest Res, 2022, 20(1): 53-63. doi: 10.5217/ir.2020.00079
[10] BERGERON F, BOUIN M, D'AOUST L, et al. Food avoidance in patients with inflammatory bowel disease: what, when and who[J]. Clin Nutr, 2018, 37(3): 884-889. doi: 10.1016/j.clnu.2017.03.010
[11] KOCSIS R N. Book review: diagnostic and statistical manual of mental disorders: (DSM-5)[Z]. Sage Publications Sage CA: Los Angeles, 2013: 1-31.
[12] FINK M, SIMONS M, TOMASINO K, et al. When is patient behavior indicative of avoidant restrictive food intake disorder (ARFID) vs reasonable response to digestive disease?[J]. Clin Gastroenterol Hepatol, 2022, 20(6): 1241-1250. doi: 10.1016/j.cgh.2021.07.045
[13] YELENCICH E, TRUONG E, WIDAMAN A M, et al. Avoidant restrictive food intake disorder prevalent among patients with inflammatory bowel disease[J]. Clin Gastroenterol Hepatol, 2022, 20(6): 1282-1289, e1. doi: 10.1016/j.cgh.2021.08.009
[14] HE J B, ZICKGRAF H F, ELLIS J M, et al. Chinese version of the nine item ARFID screen: psychometric properties and cross-cultural measurement invariance[J]. Assessment, 2021, 28(2): 537-550. doi: 10.1177/1073191120936359
[15] ELLIS J, ZICKGRAF H F, WHITED M C, et al. Establishing clinical cutoffs for the screening of avoidant/restrictive food intake disorder; proceedings of the Annals of Behavioral Medicine, F, 2017[C]. SPRINGER 233 SPRING ST, NEW YORK, NY 10013 USA.
[16] GRUNERT K G, DEAN M, RAATS M M, et al. A measure of satisfaction with food-related life[J]. Appetite, 2007, 49(2): 486-493. doi: 10.1016/j.appet.2007.03.010
[17] HE J B, ELLIS J M, ZICKGRAF H F, et al. Translating, modifying, and validating the adult picky eating questionnaire for use in China[J]. Eat Behav, 2019, 33: 78-84. doi: 10.1016/j.eatbeh.2019.04.002
[18] 吴明隆. 问卷统计分析实务: SPSS操作与应用[M]. 重庆: 重庆大学出版社, 2010: 21-54. [19] 吴明隆. 结构方程模型: SIMPLIS的应用[M]. 重庆: 重庆大学出版社, 2012: 25-41. [20] 林崇德. 心理学大辞典[M]. 上海: 上海教育出版社, 2003: 1-31. [21] FLETCHER P C, SCHNEIDER M A. Is there any food I can eat Living with inflammatory bowel disease and/or irritable bowel syndrome[J]. Clin Nurse Spec, 2006, 20(5): 241-247. doi: 10.1097/00002800-200609000-00011
-
期刊类型引用(3)
1. 何岱昆,沈雪婷,王丽娜,潘志刚. 老年急性脑梗死患者卒中相关性肺炎的生存率及其预后的影响因素分析. 老年医学与保健. 2023(01): 25-29 .  百度学术
百度学术
2. 王静,刘仲仲,逯青丽,刘佩,刘燕,常乔乔,张娜,蔺雪梅,王芳,吴松笛. 西安地区中青年与老年急性轻型脑梗死患者的临床特征及1年预后分析. 实用临床医药杂志. 2021(07): 34-38 .  本站查看
本站查看
3. 徐丽华,冀瑞俊,高素颖,于凯,杨红娜,何艳,耿颂. 急性脑梗死患者1年预后不良的相关危险因素分析. 临床荟萃. 2020(10): 895-899 .  百度学术
百度学术
其他类型引用(0)




 下载:
下载:

 苏公网安备 32100302010246号
苏公网安备 32100302010246号
