Influencing factors and predictive model construction of malnutrition in hospitalized elderly patients with comorbidities of chronic diseases
-
摘要:目的
探讨住院老年慢性病共病患者营养不良的影响因素及预测模型构建。
方法采用便利抽样法选取2023年1月—2024年2月在苏州大学附属苏州九院老年医学科住院的老年慢性病共病患者426例为研究对象。以微型营养评定简表(MNA-SF)评分 < 8分且白蛋白 < 34.0 g/L或前白蛋白 < 200 mg/L为营养不良依据,将患者分为营养不良组和无营养不良组。比较2组一般资料、口腔状况[采用口腔健康评估量表(OHAT)评估]、膳食炎症指数(DII, 采用食物频率问卷表评估)、日常活动能力[采用Barthel指数(BI)评估]。采用多因素Logistic回归分析对老年慢性病共病患者营养不良的影响因素进行探讨,并构建模型公式。采用R软件运行梯度提升机(GBM)算法构建GBM预测模型。采用受试者工作特征(ROC)曲线分析2个模型的预测效能,采用Delong检验比较2个模型的曲线下面积(AUC)的差异。
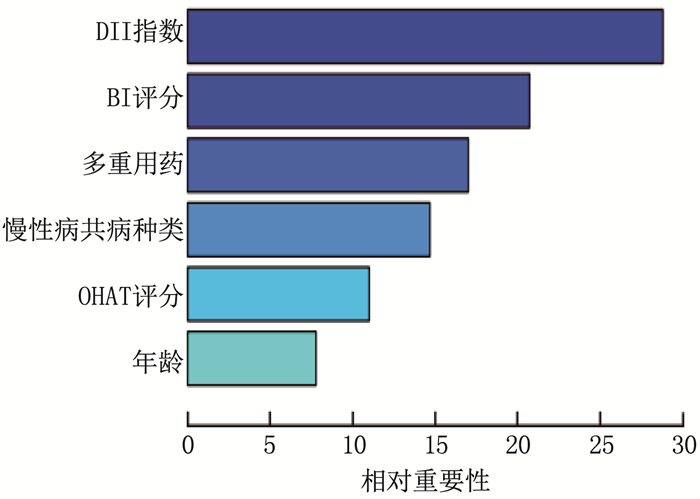
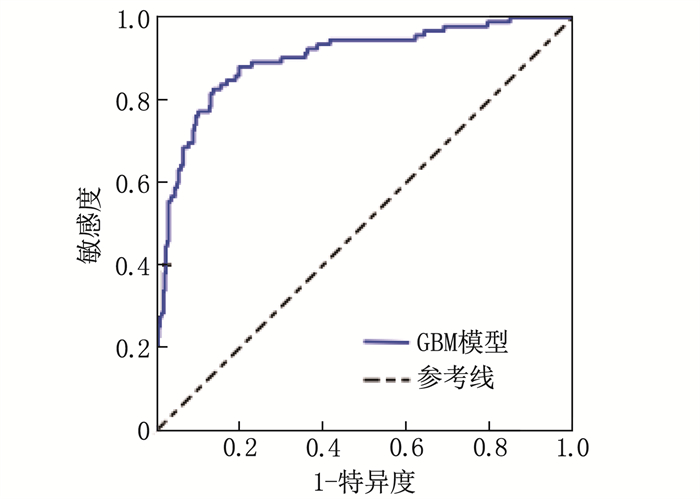
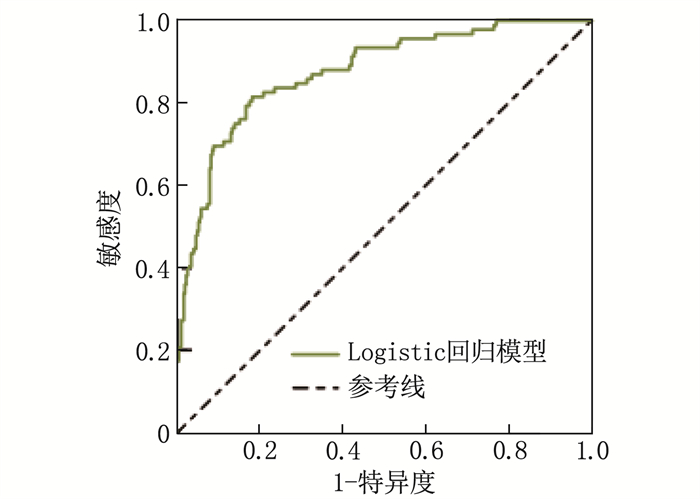
结果92例被诊断为营养不良(营养不良组),334例患者无营养不良(无营养不良组)。营养不良组与无营养不良组年龄、慢性病共病种类、多重用药种类、OHAT评分、DII、BI评分比较,差异有统计学意义(P < 0.05)。年龄大、慢性病共病种类多、多重用药种类多、OHAT评分高、DII高、BI评分低均是老年慢性病共病患者营养不良的影响因素(P < 0.05)。ROC曲线显示,GBM模型的AUC为0.901, Logistic回归模型的AUC为0.874。Delong检验提示, GBM模型的预测效能优于Logistic回归模型(P < 0.05)。
结论住院老年慢性病共病患者营养不良与年龄、慢性病共病种类、多重用药种类、OHAT评分、DII、BI评分有关,以此构建GBM模型可有效评估患者营养不良的发生风险。
Abstract:ObjectiveTo investigate the influencing factors of malnutrition in hospitalized elderly patients with comorbidities of chronic diseases, and to construct a predictive model.
MethodsA convenience sampling method was used to select 426 elderly patients with comorbidities of chronic diseases admitted to the Department of Geriatrics of Suzhou Ninth People's Hospital Affiliated to Soochow University from January 2023 to February 2024. Based on a Mini-nutritional Assessment-Short Form (MNA-SF) score < 8 and either an albumin level < 34.0 g/L or a prealbumin level < 200 mg/L as reference of malnutrition, patients were classified into malnutrition group and non-malnutrition group. General characteristics, oral status[assessed using the Oral Health Assessment Tool (OHAT)], dietary inflammatory index (DII, evaluated through a food frequency questionnaire), and activities of daily living[assessed using the Barthel Index (BI)]were compared between the two groups. Multivariable Logistic regression analysis was employed to explore the influencing factors of malnutrition in elderly patients with comorbidities of chronic diseases and to construct a model formula. A gradient boosting machine (GBM) algorithm was implemented using R software to build a GBM predictive model. Receiver Operating Characteristic (ROC) curves were utilized to analyze the predictive performance of both models, and the Delong test was applied to compare the difference of the area under the curve (AUC).
ResultsNinety-two patients were diagnosed with malnutrition (malnutrition group), while 334 patients had no malnutrition (non-malnutrition group). Statistically significant differences were observed between the malnutrition and non-malnutrition groups in terms of age, the number of chronic comorbidities, the number of medication taken, OHAT scores, DII, and BI scores (P < 0.05). Advanced age, a higher number of chronic comorbidities, a greater number of medication taken, higher OHAT scores, higher DII, and lower BI scores were all influencing factors of malnutrition in elderly patients with comorbidities of chronic diseases (P < 0.05). The ROC curve analysis revealed an AUC of GBM model was 0.901 and 0.874 for the Logistic regression model. The Delong test indicated that the predictive performance of the GBM model was superior to that of the Logistic regression model (P < 0.05).
ConclusionMalnutrition in hospitalized elderly patients with chronic multimorbidity is associated with age, the number of chronic comorbidities, the number of medications taken, OHAT scores, DII, and BI scores. The constructed GBM model can effectively assess the risk of malnutrition in these patients.
-
自身免疫性甲状腺疾病(AITD)属于器官特异性自身免疫性疾病,最常见的2种类型为格雷夫斯病(GD)和桥本氏甲状腺炎(HT)[1]。AITD发病机制尚不清楚,但其发生受遗传和环境因素共同影响,当遗传易感个体暴露于环境调节触发因素如吸烟,病毒/细菌感染,不适当的碘摄入和面临压力应激时,可能会发生AITD [2-3]。已知的AITD易感基因分为3组: 人类白细胞抗原(HLA)基因,非HLA免疫调节基因(如CTLA-4、PTPN22和CD40)和甲状腺特异性基因(如TSHR和Tg)。作者主要阐述基于AITD与HLA基因之间的关系及其对相关疾病发生发展的影响,同时对2者间关联性的研究进展及机制作综述。
1. HLA特定位点与AITD的关联
1.1 与GD有关的HLA基因及单倍体型
GD是一种伴甲状腺素合成异常的器官特异性自身免疫性疾病,约占甲亢患者的85%以上,在40~60岁高发,多见于女性。亚洲人群比高加索人群发病率更高。GD发生与遗传有关,已发现很多GD的HLA易感基因[2], 此前研究多与HLA分型相关,尽管各种研究结果不一致,但都表明HLA基因多态性在GD的发生中起重要作用。
在高加索人群中: 研究[4-5]发现等位基因HLA-DR3、DQB1*02、DQA1*0501和DRB1*03-DQA1*0501-DQB1*02(DR3)单倍体型与GD发生的高风险相关,其中HLA-DR3(HLA-DRB1*03)被认为是GD最主要的易感等位基因[6], 而HLA-DRB1*07可以降低GD发生的风险率。此外, VITA R等[7]发现DR4也与GD的发生有相关性。
有关HLA I类基因与GD间的关联研究: SIMMONDS M J等[8]研究了806例来自英国的GD患者和487例对照受试者中HLA-B和HLA-C位点对GD的影响,发现在HLA-C位点中, HLA-C*07(OR=1.63)具有最强易感性, HLA-C*03(OR=0.54)和HLA-C*16(OR=0.36)对GD具有保护性; 在HLA-B位点中, B*08(OR=1.62)具有强易感性, B*44(OR=0.64)则具有保护作用。此项研究首次为HLA-C与GD的主要关联提供了证据支持。
研究[9-11]报道GD与HLA-DQA1*0501和HLA-DQA1*0301等位基因呈正相关,这与之前得出的DQA1*0501与亚洲人无关的结论相悖。尹凤媛[10]对山东青岛地区194例GD患者研究后证实,携带DQA1*0201(P < 0.01, OR<1)等位基因的个体分布频率显著低于正常对照组,这与赵文娟等[12]对山东沿海地区的研究结果相同。而王长青等[9]对福州地区100例GD患者与100例健康对照研究后发现,HLA-DQA1* 0201的频率与对照组无统计学差异,表明与GD没有相关性。由此可见,在同一种族不同地区间,与GD相关的HLA等位基因也有一定的差异性,可能是因为HLA等位基因的频率分布和研究例数不同所导致。此外, CHEN P L等[13]进行了1项病例对照关联研究,对6个经典的HLA位点(HLA-A、HLA-B、HLA-C、HLA-DPB1、HLA-DQB1和HLA-DRB1)进行全面基因分型发现: HLA-B*4601(PBc=1.17×10-2, OR=1.33)、DPB1*0501(PBC=2.58×10-10, OR=2.34)、DRB1*1501(PBC=1.22×10-2, OR=1.68)和DRB1*1602(PBC=1.46×10-5, OR=2.63)是GD的易感基因; DQB1*0302(PBC=1.97×10-2, OR=0.62)、DRB1*1202(P=5.6×10-4, OR=0.53)是保护基因。WU Y L等[14]通过对所有DRB1等位基因进行基于高分辨率序列分型的病例对照关联研究,并于1个家庭数据集中进行确认,证实了DRB1*0901可能是GD的主要HLA易感基因,而DRB1*1202则是常见保护基因。
一项关于日本人群HLA与GD关联研究[15]显示: HLA-B*4601、HLA-DPB1*0501、HLA-B*3501和HLA-DRB1*1403与GD正相关。可见HLA-B*4601、HLA-DPB1*0501是中国和日本人群对GD的共同易感基因。此项研究还发现其中最具代表性的保护性等位基因HLA-DR13 (HLA-DRB1*1302)是对GD易感的HLA-DP5等位基因的上位基因,即部分保护性HLA等位基因对易感HLA等位基因具有上位效应。在韩国人群中, GD与HLA-DRB1*0803(Pc=0.03, OR=2.27)和DRB1*1602(Pc=0.03, OR=22.34)的相关性已被报道[16], 此外在泰国的GD患者中也观察到HLA-DRB1*1602的频率增加(P=0.006 3, OR=2.91)[17]。HLA-DRB1*1602可能是亚洲人群共有的GD易感基因。
GD的遗传基因在亚洲人群和高加索人群中具有较大差异性。相关研究[18-19]报道白种人中最显著的易感性等位基因DRB1*0301在亚洲人群中频率较低,在中国人中约占4%~9%。HLA-B*46的等位基因频率在亚洲人群中为3.9%~8.6%, 在欧洲人群中几乎为零[20], 可能是HLA基因型在人种、地域的高度异质性及研究样本量的差异所致。其他非HLA基因,如TSH受体基因、细胞因子基因、补体基因等也与GD发病有关[9], 这些因素共同相互作用,也会引起临床表型的显现,最终导致了结果的差异性。
1.2 与桥本氏甲状腺炎有关的HLA基因及单倍体型
桥本氏甲状腺炎(HT)又称慢性淋巴细胞性甲状腺炎,是甲状腺最常见的器官特异性自身免疫性疾病,大约占甲状腺疾病的22.5%[21]。流行病学资料[22]确证了HT有遗传倾向,HT具有多种临床特征,可能有多种基因参与了甲状腺自身免疫的过程,现将常见的发病基因综述如下。
关于高加索人群的研究[23-25]发现, HT与HLA-DRB1*03、DRB1*04、DQB1*0201、DQB1*0301及DQA1*0301易感性密切相关; 而对HT起保护作用的基因位点为HLA-DRB1*07、DQB1*06、DQA1*0102和DQA1*0201。ZEITLIN A A等[23]对英国625例HT患者和619例对照志愿者研究后发现,与HT关联性最强的单倍体型为DR4单倍体型(P=6.79×10-7, OR=1.98), 具有强易感性; 此外, DR3被证实与HT相关,但是检测到DR3单倍体型与HT相关性较低(P=0.050), 这与HEWARD J M等[26]对于GD的研究结果相反, DR3与GD有强相关性,而与DR4的关联性则较弱。这为GD和HT之间的遗传因果关系存在不同的理论提供了一定的依据。
徐春等[27]关于30例汉族HT患者和24名正常对照人群的HLA基因的研究表明, HT的易感基因为HLA-DQA1*0301(P < 0.02, RR=7.00), 而HLA-DQB1*0602(P < 0.01, RR=0.095)为保护性位点。此外,有关中国汉族儿童HT患者的研究报道[28], HLA-B*4601与该病的易感性相关(Pc=9.99×10-5, OR=2.31), 但仍需扩大样本进一步研究以明确HLA-B*4601在HT发展中的作用,这一发现表明HLA-B*46等位基因可能为亚洲特定的HT基因标记。研究[29-30]表明,中国人群的HLA-DR9等位基因也对HT有易感性。HLA-B、HLA-DR、HLA-DQ等位基因与中国人群HT之间密切关联,但具体的致病机制仍有待深入研究。
TAMAI H等[31-32]对日本人群中进行HLA-DQ位点与HT的相关性研究时发现, HLA-DQA1*0102和DQB1*0602与HT呈负相关。相关研究[33]报道,在日本人群中, HLA-DQA1*0301与DR4呈连锁不平衡,同时DQA1*0301基因频率也相应有所升高,提示在日本人中DQA1*0301也与HT的易感性有关,而连锁不平衡是导致位点在不同人种间频率不一致的主要归因。DQA1*0301基因很可能是不同地区人群对HT的一个共同易感基因,而DQB1*0602基因可能是共同保护基因。
UEDA S等[15]对444例HT患者和481例对照受试者的HLA等位基因进行基因分型,分析了易感和保护性HLA等位基因在HT发展过程中的相互作用。研究结果发现,等位基因HLA-A*0207(PC=1.4×10-5, OR=3.42)和HLA-DR4(PC=0.002 2, OR=1.84)与HT的易感性强相关。在有关HLA-B位点的研究[34]中, HLA-B*46(Pc < 0.02, RR=3.66)及HLA-B*51(Pc < 0.002, RR=3.42)基因频率在日本HT患者中相对升高,证明与HT的易感性相关。此外,一项关于DR-DQ单倍体型与HT关联性的研究表明, DRB1*0901-DQB1*0303单倍型赋予日本人群对HT的易感性,这与HASHIMOTO K[35]研究结果相符。
一项有关韩国人群的研究[36]表明,与健康对照人群相比, HT患者的HLA-B*46和HLA-Cw*01等位基因频率较高,提示与HT的易感性相关,而HLA-B*46与HLA-Cw*01的共存可能是韩国人群早发性AITD的基因标记。HLA-B*46位点在中国、日本及韩国人群中均对HT具有易感性,可能为亚洲人群特定易感基因。
HLA等位基因的分布存在种族差异,但是不同种族、地域间也同时具有一定的相似性。了解HLA等位基因与不同人群中AITD的关联性异同,有助于精确指导临床诊疗。
2. GD与HT与HLA基因关联性的异同
在AITD中,有关GD和HT的遗传免疫机制的异同,有诸多研究争论。相关研究[13, 28, 37]发现,携带HLA-B*4601、HLA-DQA1*0301、HLA-DQA1*0501等位基因的个体与GD和HT的易感性相关,而携带DQA1*0201等位基因的个体则与GD和HT的保护性相关。在高加索人群中, DR3与GD和HT的易感性均相关,DR7则与GD和HT的保护性皆相关。同一对等位基因,在不同的人群中,既可以与GD又可以与HT的易感或保护性相关,说明GD和HT在遗传免疫机制上,可能有一定的共同基础[37]。此外, WEETMAN A P[38]对AITD进行家族性研究时发现, GD和HT聚集在同一个家族,而GD在单个患者中可发展为HT, 这表明GD和HT可能具有相同的遗传因素。从抗体层面的研究也证实,有些患者既是GD患者,亦为HT患者。ZEITLIN A A等[23]在对HT发病机制的研究中对该现象进行了阐明,HT患者早期由于机体代偿,反馈回路导致T3和T4的过量产生,引起甲状腺功能短暂亢进,与甲状腺功能减退症的最终结果相反。这种短暂性甲状腺毒症与早期不正确的GD诊断相结合,也可能是一些理论假设GD可以转化为HT的原因。
GD与HT在遗传机制上,既存在一定的共同性,也具有各自的特异性,两者间相关性仍有待于临床表型基础上的分层研究。
3. HLA基因与AITD关联的致病机制
HLA-Ⅱ类分子是AITD的主要易感基因,其α链与β链共同构成一个抗原(肽)结合槽,外来抗原经加工处理形成肽链并与HLA-Ⅱ类分子结合后,才可被T细胞识别,从而产生细胞因子,参与免疫反应调节,此为T细胞激活的必需信号,并可激活B淋巴细胞,促使其产生大量自身抗体,引发AITD[27]。
HLA-DR是T细胞激活的第一信号,其表达程度反映了细胞的抗原提呈能力。LEE H J等[39]假设HLA-DR3中特定序列变体,产生可将致病性甲状腺衍生肽呈递给T细胞的独特口袋结构,导致AITD发生。通过对大量AITD患者和对照组中的HLA-DR基因进行测序,发现HLA-DRβ链(HLA-DRβ1-Arg74)第74位精氨酸的存在对AITD的发展至关重要,而谷氨酰胺在该位置(Gln-74)则具有保护性,该发现与相关研究结论一致[40-41]。分子动力学模拟分析表明,与含有保护性Gln-74等位基因的口袋相比, HLA-DRβ1-Arg74等位基因产生了一个带正电的窄P4口袋[41], 这种结构变化可以影响AITD的发生风险[42]。
研究[23]表明DR4单倍型可能是以细胞破坏为中心的自身免疫疾病。SCHÖNLAND S O等[43]研究发现具有DRB1*04等位基因的个体生命早期表现出CD4+ T细胞和粒细胞中端粒的缩短。在DRB1*04阳性个体中观察到早发性端粒缩短可能导致CD4+ T细胞和粒细胞的复制、衰老加速,导致细胞更新率降低[44]。T细胞群体性质的变化可降低免疫系统应对抗原刺激的功能,且进入衰老状态的T细胞不能有效阻止自身反应细胞扩增。此外,不排除该过程可能为控制刺激反应较小的衰老T细胞主动攻击宿主自身的细胞所造成[45]。HLA-Ⅱ类抗原的等位基因的多态性能够改变HLA分子、抗原、T细胞受体之间的相互作用,并由此控制对外来抗原(或自身抗原)的免疫应答。
HLA-I类抗原在有核细胞表面表达,主要参与内源性抗原向CD8+淋巴细胞的呈递, HLA-I类分子还可以结合与甲状腺抗原交叉反应的细菌/病毒抗原,并通过分子模拟产生甲状腺自身免疫[5, 7, 46]。分子模拟是遗传易感个体暴露于给定微生物以触发AITD的一种重要机制[47], 该机制在亚急性甲状腺炎中更为典型。HLA的致病机制较为复杂,仍需深入研究进一步明确其机制。
4. 结语
自身免疫相关性甲状腺疾病的发生、发展与HLA基因均关联,其直接表现于对疾病的易感性和保护性。分析这些疾病致病因素可能与特异性或非特异性炎症相关,故而对其机制的研究应以此为出发点,进而使HLA基因在疾病的预测和干预中发挥重要作用。目前相关研究结果存在差异,还须进一步进行不同地区、不同人群、不同分层和新技术层面的研究。
-
表 1 老年慢性病共病患者营养不良的单因素分析(x±s)[n(%)][M(P25, P75)]
指标 分类 营养不良组(n=92) 无营养不良组(n=334) t/χ2/U P 年龄/岁 74.54±4.16 72.83±3.59 3.676 0.001 体质量指数/(kg/m2) 21.92±2.98 22.65±3.55 1.805 0.072 性别 男 52(56.52) 161(48.20) 1.996 0.158 女 40(43.48) 173(51.80) 文化程度 高中及以下 58(63.04) 186(55.69) 1.595 0.207 大专及以上 34(36.96) 148(44.31) 日常有无家人照顾 有 62(67.39) 253(75.75) 2.615 0.106 无 30(32.61) 81(24.25) 家庭居住地 农村 55(59.78) 181(54.19) 0.913 0.339 城镇 37(40.22) 153(45.81) 慢性病共病种类 2~5种 71(77.17) 299(89.52) 9.631 0.002 ≥6种 21(22.83) 35(10.48) 多重用药种类 < 5种 74(80.43) 309(92.51) 11.599 0.001 ≥5种 18(19.57) 25(7.49) 血红蛋白/(g/L) 122.85±17.93 126.46±19.63 1.590 0.112 白蛋白/(g/L) 34.97±4.82 36.01±4.73 1.861 0.064 前白蛋白/(mg/L) 229.88±34.98 237.13±38.41 1.633 0.103 总胆固醇/(mmol/L) 4.33±1.05 4.46±1.21 0.938 0.349 甘油三酯/(mmol/L) 1.19±0.37 1.21±0.39 0.440 0.659 空腹血糖/(mmol/L) 5.64±1.82 5.48±1.56 0.839 0.402 口腔健康评估量表评分/分 8.85±1.46 7.69±1.17 7.958 < 0.001 膳食炎症指数 0.78(-0.89, 1.72) 0.13(-1.53, 1.41) 8.874 < 0.001 日常生活活动能力量表评分/分 56.54±7.93 61.73±8.97 5.033 < 0.001 表 2 多因素Logistic回归分析结果
变量 β SE Wald χ2 P OR(95%CI) 年龄 0.895 0.332 2.696 0.007 2.447(1.276~4.693) 慢性病共病种类 0.756 0.285 7.036 0.008 2.129(1.218~3.725) 多重用药种类 1.163 0.404 8.287 0.004 3.199(1.449~7.064) OHAT评分 0.574 0.231 6.174 0.013 1.775(1.128~2.793) DII 1.357 0.439 9.554 0.002 3.885(1.644~9.179) BI评分 -0.875 0.359 5.940 0.015 0.416(0.206~0.843) 常数项 -6.528 1.926 11.488 < 0.001 — -
[1] 徐莉, 葛晶, 于鹏, 等. 中国老年人慢性病及共病模式变化研究: 基于中国健康与养老追踪调查数据[J]. 中国全科医学, 2024, 27(11): 1296-1302. doi: 10.12114/j.issn.1007-9572.2023.0634 [2] 杨直, 高静, 柏丁兮, 等. 老年慢性病共病患者治疗负担体验的质性研究[J]. 中国全科医学, 2022, 25(19): 2336-2341. doi: 10.12114/j.issn.1007-9572.2022.0169 [3] 张莉娜, 黄晓, 魏绍峰, 等. 人体测量指标在老年住院患者营养不良风险评估中的筛查效果[J]. 中国老年学杂志, 2024, 44(4): 984-987. doi: 10.3969/j.issn.1005-9202.2024.04.055 [4] 王劼琼, 朱树贞, 詹艳, 等. 口腔健康评估量表的汉化及信效度检验[J]. 中华现代护理杂志, 2019, 25(28): 3607-3610. doi: 10.3760/cma.j.issn.1674-2907.2019.28.010 [5] 中国疾病预防控制中心营养与健康所. 《中国食物成分表》标准版(第6版) [J]. 营养学报, 2019, 41(5): 426-428. [6] HÉBERT J R, SHIVAPPA N, WIRTH M D, et al. Perspective: the dietary inflammatory index (DII)-lessons learned, improvements made, and future directions[J]. Adv Nutr, 2019, 10(2): 185-195. doi: 10.1093/advances/nmy071
[7] 侯东哲, 张颖, 巫嘉陵, 等. 中文版Barthel指数的信度与效度研究[J]. 临床荟萃, 2012, 27(3): 219-221. [8] KAISER M J, BAUER J M, RAMSCH C, et al. Validation of the Mini Nutritional Assessment short-form (MNA-SF): a practical tool for identification of nutritional status[J]. J Nutr Health Aging, 2009, 13(9): 782-788. doi: 10.1007/s12603-009-0214-7
[9] CRICHTON M, CRAVEN D, MACKAY H, et al. A systematic review, meta-analysis and meta-regression of the prevalence of protein-energy malnutrition: associations with geographical region and sex[J]. Age Ageing, 2019, 48(1): 38-48.
[10] 崔红元, 朱明炜, 陈伟, 等. 中国老年住院患者营养状态的多中心调查研究[J]. 中华老年医学杂志, 2021, 40(3): 364-369. [11] 冉蕾, 向英, 王璋. 老年肠内营养支持期间喂养不耐受发生率及影响因素分析[J]. 实用预防医学, 2024, 31(4): 440-444. [12] 夏银平, 余飞, 杨虹, 等. 住院老年慢性病共病患者营养情况的影响因素分析[J]. 中国医药导报, 2023, 20(4): 108-111. [13] 刘璟, 许文馨, 朱俊东, 等. 养老机构老年人营养不良现状及影响因素分析[J]. 护理学杂志, 2022, 37(3): 97-100. [14] 汤红梅, 许慧琳, 郭琪, 等. 上海市闵行社区老年人营养不良风险评估及其影响因素[J]. 环境与职业医学, 2023, 40(9): 1068-1073. [15] 郁阿翠, 陈喜, 杨萌娜, 等. 老年人营养不良状况及影响因素分析[J]. 实用老年医学, 2022, 36(8): 822-826, 832. [16] DANTAS P P A, COLUSSI P R G, DEZINGRINI K D S, et al. Pairs of natural teeth rather than use of dental prosthesis are associated with nutritional status in older adults: a cross-sectional study[J]. J Dent, 2021, 108: 103656.
[17] ZHU Z, XU J Y, LIN Y, et al. Correlation between nutritional status and oral health quality of life, self-efficacy of older inpatients and the influencing factors[J]. BMC Geriatr, 2022, 22(1): 280.
[18] KIM S, KWON Y S, HONG K H. What is the relationship between the chewing ability and nutritional status of the elderly in Korea[J]. Nutrients, 2023, 15(9): 2042.
[19] 叶晨, 黄晓婕, 苏米亚·艾合买提江, 等. 中国居民膳食炎症指数情况及变化趋势[J]. 中国食物与营养, 2023, 29(2): 85-89. [20] MA T C, ZHOU J, WANG C X, et al. Association between dietary inflammatory index and S-klotho plasma levels in middle-aged and elderly people[J]. Front Nutr, 2022, 9: 853332.
[21] 闫慧慧, 刘鑫, 肖千一, 等. 膳食炎症指数在社区老年人的应用初探[J]. 老年医学与保健, 2021, 27(2): 395-398. [22] 李伟红, 吴新春, 李毅, 等. 老年住院患者膳食摄入与营养状况调查[J]. 中国临床保健杂志, 2021, 24(2): 183-187. [23] 刘金枚, 张坤, 彭杨, 等. 医养结合机构老年人营养不良预测模型的构建及验证[J]. 护理研究, 2023, 37(18): 3254-3260. [24] 中华人民共和国国务院办公厅. 国民营养计划(2017—2030)[EB/OL]. (2017-07-13)[2019-03-02]. http://www.gov.cn/zhengce/content/2017-07/13/content_5210134.hrm. -
期刊类型引用(7)
1. 付政平,董贤明,秦建领,卢奎彬,渠展,王庆丰,汤聪,徐红艳,岳雨倩. 社区获得性肺炎凝血功能异常对治疗和预后的影响. 山西卫生健康职业学院学报. 2024(06): 40-42 .  百度学术
百度学术
2. 叶文,龙尧水,陈咏梅,胡泽玉,白文学. MPV、PCT、PDW、P-LCR、MPR对儿童SCAP的诊断价值. 检验医学与临床. 2023(09): 1325-1329 .  百度学术
百度学术
3. 吴颖,高蔚,翁婷. 血浆FIB-PLT-DD联合检测在慢性肺源性心脏病治疗中的临床意义. 中国医药科学. 2023(19): 177-180+185 .  百度学术
百度学术
4. 史妹,周历安,符叶柳. 床旁肺超声B线计数及外周血嗜酸性粒细胞评估慢性阻塞性肺疾病并发肺炎的价值及其相关因素分析. 海军医学杂志. 2023(12): 1243-1247 .  百度学术
百度学术
5. 雷云飞,宋影,王亚冰. D–二聚体及凝血功能指标对慢性阻塞性肺疾病的检验价值. 深圳中西医结合杂志. 2022(23): 54-56 .  百度学术
百度学术
6. 黄鑫,王卫阳. 阿莫西林克拉维酸钾联合补肺活血胶囊对慢性阻塞性肺疾病患者肺功能及预后影响. 临床军医杂志. 2021(07): 785-786 .  百度学术
百度学术
7. 李刚,孙雨婷,王佳美,李满元. 外周血平均血小板体积在儿童社区获得性肺炎中的价值. 中国医药指南. 2021(31): 87-88+91 .  百度学术
百度学术
其他类型引用(0)




 下载:
下载:
 苏公网安备 32100302010246号
苏公网安备 32100302010246号