Pathogen status, risk factors and prediction model construction for catheter-related infection in patients with maintenance hemodialysis
-
摘要:目的
探讨维持性血液透析(MHD)患者导管相关感染的病原菌情况、危险因素并构建预测模型。
方法采用病例对照研究设计,回顾性收集2022年6月—2024年3月在苏州大学附属苏州九院进行MHD治疗的208例患者的临床资料。分析患者导管相关感染情况,依据导管相关感染发生情况将MHD患者分为感染组和无感染组,并比较2组患者的临床资料。为避免过度拟合,采用最小绝对收缩和选择算子(LASSO)回归分析初步筛选变量,再采用多因素Logistic回归分析探讨MHD患者导管相关感染的危险因素。基于各风险因素构建预测模型,采用受试者工作特征(ROC)曲线的曲线下面积(AUC)评估模型的区分度; 应用K-fold交叉验证法对模型进行深度验证。
结果208例MHD患者导管相关感染率为24.52%(51/208), 其中导管局部感染22例,隧道感染17例,导管相关性血流感染12例; 共分离培养出革兰阳性菌36株,革兰阴性菌28株,真菌1株。感染组与无感染组在合并糖尿病、白蛋白、置管部位、导管留置时间以及导管维护频率方面比较,差异有统计学意义(P < 0.05)。LASSO回归分析和多因素Logistic回归分析表明,合并糖尿病(OR=3.651, 95%CI: 2.056~7.508)、白蛋白低(OR=1.782, 95%CI: 1.129~2.815)、置管部位为股内静脉(OR=2.298,95%CI: 1.269~4.162)、导管留置时间长(OR=2.959, 95%CI: 1.327~6.599)、导管维护频率≤2次/月(OR=2.373, 95%CI: 1.316~4.276)均为MHD患者导管相关感染的独立危险因素(P < 0.05)。基于独立危险因素构建的预测模型的AUC为0.885(95%CI: 0.838~0.931), 灵敏度为0.875, 特异度为0.847;100次K-fold交叉验证表明模型具有较好的泛化能力。
结论MHD患者导管相关感染风险较高,构建预测模型能有效评估MHD患者导管相关感染风险。
Abstract:ObjectiveTo explore the pathogens status and risk factors for catheter-related infection in patients with maintenance hemodialysis (MHD), and to establish a prediction model.
MethodsA case-control study design was adopted, and clinical materials of 208 MHD patients treated in Suzhou Ninth People's Hospital of Suzhou University from June 2022 to March 2024 were retrospectively collected. The catheter-related infection status of the patients was analyzed, and they were divided into infection group and non-infection group based on the occurrence of catheter-related infections. The clinical materials were compared between the two groups. To avoid overfitting, the least absolute shrinkage and selection operator (LASSO) regression analysis was used for initial variable screening, followed by multivariate Logistic regression analysis to explore the risk factors for catheter-related infections in MHD patients. A predictive model was constructed based on the risk factors, and the area under the curve (AUC) of the receiver operating characteristic (ROC) curve was used to assess discrimination of the model. The K-fold cross-validation method was applied for in-depth validation of the model.
ResultsThe incidence rate of catheter-related infection in the 208 MHD patients was 24.52% (51/208), including 22 cases of local catheter infections, 17 cases of tunnel infections, and 12 cases of catheter-related bloodstream infections. A total of 36 Gram-positive bacteria, 28 Gram-negative bacteria, and 1 fungus were isolated and cultured. Significant differences were observed between the infection and non-infection groups in terms of complicating diabetes, albumin level, catheter insertion site, catheter indwelling time, and catheter maintenance frequency (P < 0.05). LASSO regression analysis and multivariate Logistic regression analysis revealed that complicating diabetes (OR=3.651, 95%CI, 2.056 to 7.508), low albumin level (OR=1.782, 95%CI, 1.129 to 2.815), catheter insertion in the internal femoral vein (OR=2.298, 95%CI, 1.269 to 4.162), long catheter indwelling time (OR=2.959, 95%CI, 1.327 to 6.599), and catheter maintenance frequency ≤2 times per month (OR=2.373, 95%CI, 1.316 to 4.276) were independent risk factors for catheter-related infections in MHD patients (P < 0.05). The AUC of the predictive model based on independent risk factors was 0.885 (95%CI, 0.838 to 0.931), with a sensitivity of 0.875 and a specificity of 0.847. A hundred rounds of K-fold cross-validation demonstrated good generalization ability of the model.
ConclusionMHD patients have a high risk of catheter-related infections, and the constructed prediction model can effectively assess the risk of catheter-related infections in MHD patients.
-
Keywords:
- maintenance hemodialysis /
- catheter-related infections /
- pathogens /
- risk factors /
- prediction model
-
维持性血液透析(MHD)是急性肾衰竭的有效干预手段[1], 但长时间置管会增加导管相关感染的发生风险[2]。研究[3-4]表明血液透析患者的导管相关感染发生率为8.9%~41.8%, 可见血液透析患者的导管相关感染风险较高。透析患者的导管相关感染是指导管留置期间出现的原发性感染,其可造成非预期的导管移除,缩短导管使用寿命,并可增加患者住院次数,加重患者医疗负担,甚至会因导管相关感染而导致疾病恶化,危及患者生命安全[5]。本研究分析MHD患者导管相关感染状况及其危险因素,并依据危险因素构建预测模型,现将结果报告如下。
1. 资料与方法
1.1 一般资料
采用病例对照研究设计,回顾性选取2022年6月—2024年3月在本院肾内科进行MHD治疗的208例患者为研究对象。纳入标准: ①年龄≥18岁者; ② MHD≥3个月者; ③长期留置静脉导管者; ④患者的临床资料、干预方式记录完整。排除标准: ①置管前有皮肤感染者; ②长时间使用激素、免疫抑制剂治疗者; ③伴有恶性肿瘤、结核病者; ④合并传染性疾病者,如乙型肝炎、丙型肝炎、梅毒等; ⑤合并其他脏器感染者; ⑥ MHD前1个月内有手术外伤史者。依据患者MHD期间导管相关感染发生情况将其分为感染组和无感染组。本研究已获得本院医学伦理委员会审核批准(批号: SZJY024031)。
1.2 研究方法
1.2.1 资料收集
制作资料收集表,收集MHD患者的年龄、性别、体质量指数(BMI)、是否吸烟、基础疾病(高血压、糖尿病)、首次MHD前空腹状态下静脉血实验室指标(血红蛋白、白蛋白、血钙、血磷、C反应蛋白、尿素)、透析频率、置管部位、是否发生导管功能不良、导管留置时间、导管维护频率等资料。
1.2.2 导管相关感染诊断
参照《血管导管相关感染预防与控制指南(2021版)》[6]进行诊断。①导管局部感染: 导管出口部位2 cm范围内皮肤出现硬结、红肿,且出口部位渗出脓性分泌物,分泌物培养结果呈阳性。②导管相关血流感染: 出现发热(体温>38 ℃)或新发透析前低血压(收缩压 < 90 mmHg, 1 mmHg=0.133 kPa)或出现寒战等临床表现; 血液透析导管或透析系统获取的血液标本,经培养为同一病原菌。③隧道感染: 覆盖导管表面组织和置管处>2 cm的皮肤有红斑、触痛。
1.2.3 病原菌检测
鉴于患者确诊感染, 24 h内取导管分泌物及血液标本进行病原菌鉴定,采用自动微生物检测分析仪进行细菌培养及鉴定。操作严格按照《全国临床检验操作规程》[7]进行。
1.3 统计学分析
采用SPSS 25.0软件和R软件进行数据分析,计数资料采用[n(%)]描述,计量资料采用(x ±s)表示,组间比较分别采用χ2检验、t检验。采用最小绝对收缩和选择算子(LASSO)回归分析法和交叉验证法筛选出相关性指标,随后纳入多因素Logistic回归分析探讨MHD患者导管相关感染的危险因素,基于各危险因素指标的回归系数(β)和常数项构建模型公式。采用拟合优度检验模型拟合状况,采用受试者工作特征(ROC)曲线的曲线下面积(AUC)评价模型效能,采用N次K-fold交叉验证法对模型进行深度验证。P < 0.05为差异有统计学意义。
2. 结果
2.1 MHD患者导管相关感染状况
208例患者MHD期间出现导管相关感染者51例(感染组),发生率为24.52%(51/208), 其余157例未发现导管相关感染(无感染组)。51例导管相关感染患者中,发生导管局部感染22例(43.14%),隧道感染17例(33.33%), 导管相关性血流感染12例(23.53%)。51例导管相关感染患者共分离培养出革兰阳性菌36株,革兰阴性菌28株,真菌1株,共计65株,见表 1。
表 1 MHD患者导管相关感染的病原菌分布情况病原菌 分类 株数/株 构成比/% 革兰阳性菌 金黄色葡萄球菌 11 16.92 耐甲氧西林金黄色葡萄球菌 8 12.31 表皮葡萄球菌 7 10.77 耐甲氧西林表皮葡萄球菌 5 7.69 草绿色链球菌 3 4.62 其他 2 3.08 革兰阴性菌 大肠埃希菌 10 15.38 铜绿假单胞菌 8 12.31 鲍曼不动杆菌 7 10.77 其他 3 4.62 真菌 近平滑假丝酵母 1 1.54 合计 65 100.00 2.2 感染组与无感染组临床资料比较
感染组与无感染组在合并糖尿病、白蛋白、置管部位、导管留置时间以及导管维护频率方面比较,差异有统计学意义(P < 0.05), 见表 2。
表 2 2组临床资料比较(x ±s)[n(%)]指标 分类 感染组(n=51) 无感染组(n=157) t/χ2 P 年龄/岁 59.85±12.29 57.74±11.85 1.095 0.275 体质量指数/(kg/m2) 21.63±2.75 22.35±2.94 1.543 0.124 性别 男 29(56.86) 86(54.78) 0.068 0.795 女 22(43.14) 71(45.22) 吸烟 是 18(35.29) 39(24.84) 2.114 0.146 否 33(64.71) 118(75.16) 合并高血压 是 15(29.41) 42(26.75) 0.137 0.711 否 36(70.59) 115(73.25) 合并糖尿病 是 23(45.10) 36(22.93) 9.310 0.002 否 28(54.90) 121(77.07) 血红蛋白/(g/L) 93.35±17.94 98.63±23.18 1.488 0.138 白蛋白/(g/L) 29.61±3.78 33.78±3.92 6.657 < 0.001 血钙/(mmol/L) 2.21±0.35 2.16±0.31 0.969 0.334 血磷/(mmol/L) 1.67±0.27 1.64±0.23 0.775 0.439 C反应蛋白/(mg/L) 8.59±2.83 8.16±2.75 0.963 0.337 尿素/(mmol/L) 4.54±1.08 4.75±1.12 1.173 0.242 置管部位 股静脉 24(47.06) 48(30.57) 4.662 0.032 颈静脉 27(52.94) 109(69.43) 透析频率 2次/周 14(27.45) 61(38.85) 2.171 0.141 3次/周 37(72.55) 96(61.15) 发生导管功能不良 是 9(17.65) 17(10.83) 1.637 0.201 否 42(82.35) 140(89.17) 导管留置时间/月 6.92±1.48 5.32±1.15 8.017 < 0.001 导管维护频率 >2次/月 17(33.33) 99(63.06) 13.788 < 0.001 ≤2次/月 34(66.67) 58(36.94) 2.3 MHD患者发生导管相关感染的多因素Logistic回归分析
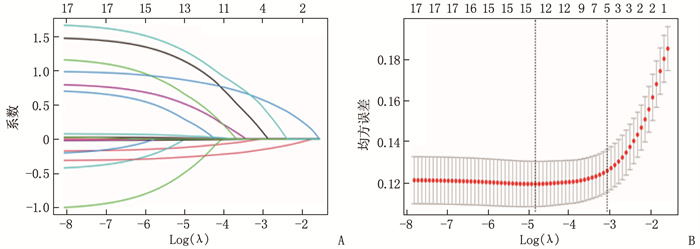
以MHD患者是否发生导管相关感染(0=否, 1=是)为结局变量,采用LASSO算法获取最大相关性指标后,再经交叉验证最终获得5个最佳变量(合并糖尿病、白蛋白、置管部位、导管留置时间、导管维护频率),见图 1。将筛选到的变量纳入多因素Logistic回归分析,结果表明合并糖尿病、白蛋白低、置管部位为股静脉、导管留置时间长、导管维护频率≤2次/月是MHD患者发生导管相关感染的危险因素(P < 0.05), 见表 3。
表 3 多因素Logistic回归分析变量 β SE Wald χ2 P OR(95%CI) 合并糖尿病 1.295 0.293 19.535 < 0.001 3.651(2.056~7.508) 白蛋白低 0.578 0.233 6.154 0.013 1.782(1.129~2.815) 置管部位为股静脉 0.832 0.303 7.539 0.006 2.298(1.269~4.162) 导管留置时间长 1.085 0.409 7.037 0.008 2.959(1.327~6.599) 导管维护频率≤2次/月 0.864 0.301 8.239 0.004 2.373(1.316~4.276) 常数项 -9.681 2.192 19.506 < 0.001 — 2.4 MHD患者导管相关感染风险的预测模型构建
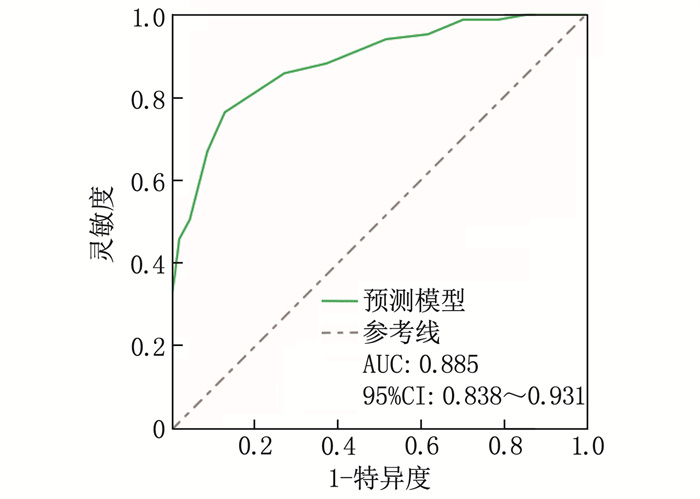
依据表 3回归系数与常数项构建MHD患者导管相关感染的风险预测模型,得出预测模型方程为: Logit(P)=1.295×合并糖尿病(0=否, 1=是)+0.578×白蛋白(实测值)+0.832×置管部位(0=颈静脉, 1=股静脉)+1.085×导管留置时间(实测值)+0.864×导管维护频率(0=>2次/月, 1=≤2次/月)-9.681。拟合优度偏差性检验显示该模型无过拟合现象(χ2=1.854, P=0.537)。该模型的AUC为0.885(95%CI: 0.838~0.931), 灵敏度为0.875, 特异度为0.847, 表明模型具有一定的预测效能,见图 2。
2.5 MHD患者导管相关感染的预测模型的深度验证
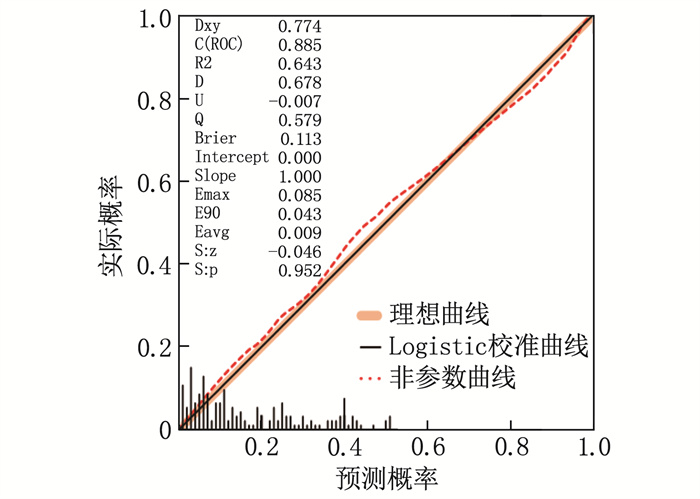
验证指标提取见图 3,即曲线下面积与一致性指数比值(AUC/C-index)>0.7表示优良, R2值越大越好,判别指数(D)≥0.4表示优良, U检验值的P>0.05说明通过校准度检验, Brier分数值越低表示预测校准度越好; 预测模型与理想模型之间的最大偏移量用Emax表示,预测模型与理想模型之间的最小偏移量用Eavg表示,二者偏移量越小说明预测模型与理想模型越接近。将以上指标作为K折交叉验证的评价指标,对多因素Logistic回归模型进行100次K-fold交叉验证法(K=10)的深度验证,交叉验证结果发现,评估原始数据建模的所有数值良好,且变化值较小,证明所构建的预测模型诊断性能良好,具有一定的泛化能力,见表 4。
表 4 预测模型的100次10折交叉验证深度评估结果指标 建模数据值 校正值 变化值 AUC/C-index 0.885 0.880 -0.005 R2 0.643 0.575 -0.068 D 0.678 0.539 -0.139 U检验 -0.007 0.027 0.034 Brier分数 0.113 0.119 0.006 Emax 0.085 0.218 0.133 Eavg 0.009 0.116 0.107 AUC/C-index: 曲线下面积与一致性指数比值;
D: 判别指数; Emax: 最大偏移量; Eavg: 最小偏移量。3. 讨论
导管相关感染是MHD常见的并发症[8]。本研究纳入208例MHD患者资料分析发现,导管相关感染发生率为24.52%, 高于研究[9]报道的16.67%, 原因可能与设置筛选病例的纳入与排除标准不同有关。研究[10]发现MHD患者发生导管相关感染与其高死亡风险相关,因而有必要了解MHD患者导管相关感染的病原菌,以便给予合理的抗生素干预。本研究对MHD患者导管相关感染的病原菌资料进行分析,发现感染最多的菌群是革兰阳性菌,以金黄色葡萄球菌为主,其次是革兰阴性菌,以大肠埃希菌为主,与研究[11]报道相似。其原因可能是这类菌群为人体皮肤的常见细菌,插管过程中皮肤细菌容易被携带进入导管内,因而临床需给予合理的抗生素干预。
糖尿病患者机体高血糖环境有利于细菌定植、繁殖,同时糖代谢紊乱现象可导致细胞因子分泌减少,削弱机体的防御功能[12], 因而合并糖尿病的MHD患者易受细菌侵袭,感染风险较高。本研究发现合并糖尿病是MHD患者发生导管相关感染的危险因素[13]。分析原因可能是伴有糖尿病者体内富含葡萄糖组织,给细菌定植与繁殖提供了有利环境[14],同时糖尿病导致体内代谢紊乱,会减少细胞因子分泌,损害免疫功能[15], 导致机体抵抗力下降,因而易受细菌侵袭。研究[16]显示多糖能够帮助细菌紧密黏附在导管壁,增加导管相关感染的风险。血液中的白蛋白含量可反映患者机体的营养状况,当MHD患者的血清白蛋白含量缺乏,表明营养状况较差[17]。本研究发现白蛋白低是MHD患者发生导管相关感染的危险因素,与GUO H J等[18]Meta分析结论相符。原因可能是部分MHD患者采取低蛋白饮食来减缓自身疾病进展,导致机体营养状况不佳,损害机体免疫力和抵抗力,无法吞噬和杀灭病菌,因而导管相关感染风险高。
SHAHAR S等[19]研究表明,置管部位为股静脉会增加导管相关感染的发生风险,与本研究结果相似。原因可能为股静脉解剖位置靠近会阴、肛门,该区域环境通常以潮湿为特征,有利于细菌生长; 同时,股静脉内血流较为缓慢,此条件也有利于细菌繁殖,增加导管相关感染风险。导管相关感染风险可随导管留置时间延长而增加。李道新等[20]研究发现,导管留置时间长是血液透析患者发生菌血症的危险因素,这提示导管留置时间越长,越可能导致外界细菌经体表或者创口进入血液系统中,诱发菌血症。SAHLI F等[21]研究表明,导管的管腔内细菌定植是引起感染的重要因素。本研究发现导管留置时间长是MHD患者发生导管相关感染的独立危险因素,与MATARRESE A N等[22]研究结论相符。MHD患者通常需每周透析2~3次[23],在此过程中,透析管与患者的静脉留置导管进行多次断开、连接,增加细菌入侵导管腔内的概率[24]; 同时,随着导管留置时间延长,由透析需要导致的反复暴露次数也在增多,促使导管周围生长和繁殖的细菌越来越多,当其超过人体感染阈值时,便可释放至血液中[25], 诱发导管相关感染的严重症状。MHD患者发生导管相关感染的医源性因素也常见且最易被忽略。本研究发现导管维护频率低是MHD患者导管相关感染的风险因素,因此需重视血液透析导管的维护,坚持导管相关感染预防大于治疗的基本原则。
为确保不偏离MHD患者的导管相关感染预防大于治疗的理念[26], 本研究根据筛选出的MHD患者导管相关感染各危险因素的回归系数和常数项构建风险预测模型方程。经ROC曲线分析,该模型预测MHD患者导管相关感染风险的AUC为0.885, 且模型经拟合优度偏差性检验无过拟合现象,表明模型有一定预测能力; 同时,采用交叉验证法对模型进行深度验证发现,模型依旧有较好的诊断效能和泛化能力。因而依据MHD患者导管相关感染各风险因素构建模型,评估导管相关感染风险,将有助于医务人员为高风险人群制订个性化管理措施(如加强对伴有糖尿病患者的血糖管理,将患者血糖水平控制在合理范围,降低导管相关感染风险; 对患者的营养状况进行评估与监测,若存在低蛋白血症或进食困难,可建议患者输注白蛋白以增强抵抗力,降低感染风险; 置管部位应尽量避免使用股静脉,同时动态评估导管留置时间,严格做好预防性抗菌药物封管,定期进行导管维护)。
本研究的不足: 本研究仅回顾性分析了一家医院的MHD患者数据,受样本量所限,未能划分出独立队列验证模型; 尽管本研究进行了交叉验证,但模型的普适性仍需在更广泛的患者群体中进行验证。因此,未来研究者还需进行多中心研究进一步验证模型的稳定性,不断优化模型性能。
综上所述,MHD患者导管相关感染的发生风险与合并糖尿病、白蛋白低、置管部位为股静脉、导管留置时间长、导管维护频率低有关。据此构建风险预测模型,可有效评估MHD患者导管相关感染风险。
-
表 1 MHD患者导管相关感染的病原菌分布情况
病原菌 分类 株数/株 构成比/% 革兰阳性菌 金黄色葡萄球菌 11 16.92 耐甲氧西林金黄色葡萄球菌 8 12.31 表皮葡萄球菌 7 10.77 耐甲氧西林表皮葡萄球菌 5 7.69 草绿色链球菌 3 4.62 其他 2 3.08 革兰阴性菌 大肠埃希菌 10 15.38 铜绿假单胞菌 8 12.31 鲍曼不动杆菌 7 10.77 其他 3 4.62 真菌 近平滑假丝酵母 1 1.54 合计 65 100.00 表 2 2组临床资料比较(x ±s)[n(%)]
指标 分类 感染组(n=51) 无感染组(n=157) t/χ2 P 年龄/岁 59.85±12.29 57.74±11.85 1.095 0.275 体质量指数/(kg/m2) 21.63±2.75 22.35±2.94 1.543 0.124 性别 男 29(56.86) 86(54.78) 0.068 0.795 女 22(43.14) 71(45.22) 吸烟 是 18(35.29) 39(24.84) 2.114 0.146 否 33(64.71) 118(75.16) 合并高血压 是 15(29.41) 42(26.75) 0.137 0.711 否 36(70.59) 115(73.25) 合并糖尿病 是 23(45.10) 36(22.93) 9.310 0.002 否 28(54.90) 121(77.07) 血红蛋白/(g/L) 93.35±17.94 98.63±23.18 1.488 0.138 白蛋白/(g/L) 29.61±3.78 33.78±3.92 6.657 < 0.001 血钙/(mmol/L) 2.21±0.35 2.16±0.31 0.969 0.334 血磷/(mmol/L) 1.67±0.27 1.64±0.23 0.775 0.439 C反应蛋白/(mg/L) 8.59±2.83 8.16±2.75 0.963 0.337 尿素/(mmol/L) 4.54±1.08 4.75±1.12 1.173 0.242 置管部位 股静脉 24(47.06) 48(30.57) 4.662 0.032 颈静脉 27(52.94) 109(69.43) 透析频率 2次/周 14(27.45) 61(38.85) 2.171 0.141 3次/周 37(72.55) 96(61.15) 发生导管功能不良 是 9(17.65) 17(10.83) 1.637 0.201 否 42(82.35) 140(89.17) 导管留置时间/月 6.92±1.48 5.32±1.15 8.017 < 0.001 导管维护频率 >2次/月 17(33.33) 99(63.06) 13.788 < 0.001 ≤2次/月 34(66.67) 58(36.94) 表 3 多因素Logistic回归分析
变量 β SE Wald χ2 P OR(95%CI) 合并糖尿病 1.295 0.293 19.535 < 0.001 3.651(2.056~7.508) 白蛋白低 0.578 0.233 6.154 0.013 1.782(1.129~2.815) 置管部位为股静脉 0.832 0.303 7.539 0.006 2.298(1.269~4.162) 导管留置时间长 1.085 0.409 7.037 0.008 2.959(1.327~6.599) 导管维护频率≤2次/月 0.864 0.301 8.239 0.004 2.373(1.316~4.276) 常数项 -9.681 2.192 19.506 < 0.001 — 表 4 预测模型的100次10折交叉验证深度评估结果
指标 建模数据值 校正值 变化值 AUC/C-index 0.885 0.880 -0.005 R2 0.643 0.575 -0.068 D 0.678 0.539 -0.139 U检验 -0.007 0.027 0.034 Brier分数 0.113 0.119 0.006 Emax 0.085 0.218 0.133 Eavg 0.009 0.116 0.107 AUC/C-index: 曲线下面积与一致性指数比值;
D: 判别指数; Emax: 最大偏移量; Eavg: 最小偏移量。 -
[1] 蔡茜, 张祖隆. 终末期肾脏病行维持性血液透析患者发生肌少症的相关影响因素分析[J]. 实用临床医药杂志, 2023, 27(10): 84-90. doi: 10.7619/jcmp.20230632 [2] ZANONI F, PAVONE L, BINDA V, et al. Catheter-related bloodstream infections in a nephrology unit: analysis of patient- and catheter-associated risk factors[J]. J Vasc Access, 2021, 22(3): 337-343. doi: 10.1177/1129729820939762
[3] 陈彩合, 马淑燕, 黄文辉. 维持性血液透析患者合并导管相关性血流感染预后的危险因素分析[J]. 中华危重病急救医学, 2024, 36(2): 183-188. [4] MENEGUETI M G, BETONI N C, BELLISSIMO-RODRIGUES F, et al. Central venous catheter-related infections in patients receiving short-term hemodialysis therapy: incidence, associated factors, and microbiological aspects[J]. Rev Soc Bras Med Trop, 2017, 50(6): 783-787. doi: 10.1590/0037-8682-0438-2017
[5] 赵明生, 陈远岷, 左晓英, 等. 使用中心静脉导管行血液透析患者导管相关性血流感染的危险因素分析[J]. 中国医学前沿杂志: 电子版, 2021, 13(9): 104-107. [6] 国家卫生健康委办公厅医政医管局. 血管导管相关感染预防与控制指南(2021版)[EB/OL]. (2020-03-30)[2024-09-14]. http://www.nhc.gov.cn/yzygj/s7659/202103/dad04cf7992e472d9de1fe6847797e49.shtml. [7] 尚红, 王毓三, 申子瑜. 全国临床检验操作规程[M]. 4版. 北京: 人民卫生出版社, 2015: 13-17. [8] HERNÁN V G, MUÑOZ G M, MONROY A M, et al. Influence of care on the prevention of bacteremia in hemodialysis: systematic review[J]. Nephrol Nurs J, 2023, 50(4): 333-344. doi: 10.37526/1526-744X.2023.50.4.333
[9] 武燕, 师璟, 陆伟锋, 等. 血液透析患者中心静脉导管相关性感染的危险因素及预测模型构建[J]. 中华医院感染学杂志, 2024, 34(10): 1584-1588. [10] DONATI G, SPAZZOLI A, CROCI CHIOCCHINI A L, et al. Bloodstream infections and patient survival with tunneled-cuffed catheters for hemodialysis: a single-center observational study[J]. Int J Artif Organs, 2020, 43(12): 767-773. doi: 10.1177/0391398820917148
[11] 马曦立, 刘霞, 吴鑫, 等. 慢性肾功能衰竭血液透析导管相关性血流感染病原菌耐药性及其影响因素[J]. 中华医院感染学杂志, 2021, 31(3): 385-389. [12] MENG L F, YANG L M, ZHU X Y, et al. Comparison of clinical features and outcomes in peritoneal dialysis-associated peritonitis patients with and without diabetes: a multicenter retrospective cohort study[J]. World J Diabetes, 2020, 11(10): 435-446. doi: 10.4239/wjd.v11.i10.435
[13] DOU J, WU X B, AO H, et al. Clinical characteristics of catheter-related infection in patients with chronic renal failure End Stage Renal failure undergoing semi-permanent catheter placement during maintenance hemodialysis through tunnelled cuffed hemodialysis catheter[J]. Pak J Med Sci, 2022, 38(6): 1426-1430.
[14] MARTIN K, LORENZO Y S P, LEUNG P Y M, et al. Clinical outcomes and risk factors for tunneled hemodialysis catheter-related bloodstream infections[J]. Open Forum Infect Dis, 2020, 7(6): ofaa117. doi: 10.1093/ofid/ofaa117
[15] 梁涛, 黄艳秋. 血液透析患者中心静脉导管相关性感染的影响因素分析[J]. 广西医科大学学报, 2019, 36(8): 1292-1295. [16] CHEN W, WANG Z J, WANG G P, et al. A meta-analysis of risk factors for a Dacron-cuffed catheter related infection in hemodialysis[J]. BMC Nephrol, 2024, 25(1): 126. doi: 10.1186/s12882-024-03568-0
[17] DA J J, SUN Y, CHEN J C, et al. Effect of hemoperfusion on protein energy wasting and long-term prognosis in patients on maintenance hemodialysis[J]. Zhonghua Yi Xue Za Zhi, 2023, 103(8): 559-565.
[18] GUO H J, ZHANG L, HE H, et al. Risk factors for catheter-associated bloodstream infection in hemodialysis patients: a meta-analysis[J]. PLoS One, 2024, 19(3): e0299715. doi: 10.1371/journal.pone.0299715
[19] SHAHAR S, MUSTAFAR R, KAMARUZAMAN L, et al. Catheter-related bloodstream infections and catheter colonization among haemodialysis patients: prevalence, risk factors, and outcomes[J]. Int J Nephrol, 2021, 2021: 5562690.
[20] 李道新, 熊飞, 李红兵, 等. 血液透析患者导管相关性血流感染的危险因素及其预测模型构建[J]. 中华医院感染学杂志, 2023, 33(3): 368-371. [21] SAHLI F, FEIDJEL R, LAALAOUI R. Hemodialysis catheter-related infection: rates, risk factors and pathogens[J]. J Infect Public Health, 2017, 10(4): 403-408. doi: 10.1016/j.jiph.2016.06.008
[22] MATARRESE A N, IVULICH D I, CESAR G, et al. Epidemiological analysis of catheter-related bloodstream infections in medical-surgical intensive care units[J]. Medicina, 2021, 81(2): 159-165.
[23] BUTT U, DAVENPORT A, SRIDHARAN S, et al. A practical approach to implementing incremental haemodialysis[J]. J Nephrol, 2024: Online ahead of print.
[24] BLANCO-DI MATTEO A, GARCIA-FERNANDEZ N, AGUINAGA PÉREZ A, et al. Pre-emptive antimicrobial locks decrease long-term catheter-related bloodstream infections in hemodialysis patients[J]. Antibiotics, 2022, 11(12): 1692. doi: 10.3390/antibiotics11121692
[25] OPOKU-ASARE B, BOIMA V, GANU V J, et al. Catheter-Related Bloodstream Infections among patients on maintenance haemodialysis: a cross-sectional study at a tertiary hospital in Ghana[J]. BMC Infect Dis, 2023, 23(1): 664. doi: 10.1186/s12879-023-08581-6
[26] LAZARUS B, BONGETTI E, LING J, et al. Multifaceted quality improvement interventions to prevent hemodialysis catheter-related bloodstream infections: a systematic review[J]. Am J Kidney Dis, 2023, 82(4): 429-442, e1. doi: 10.1053/j.ajkd.2023.02.006




 下载:
下载:
 苏公网安备 32100302010246号
苏公网安备 32100302010246号
