Establishment and application of a new method for detecting Mycoplasma pneumoniae
-
摘要:目的
建立成簇的规律间隔的短回文重复序列(CRISPR)-Cas12a技术结合环介导等温扩增(LAMP)单管一步法快速检测肺炎支原体(Mp), 并探讨其在临床诊断中的应用价值。
方法设计并优化Mp LAMP引物,根据LMAP产物靶标设计Cas12a CrRNA。分析CRISPER-LAMP单管一步法检测Mp DNA的灵敏度; 检测Mp、甲流病毒(FluA)、乙流病毒(FluB)、肺炎克雷伯菌(Kp)和肺炎链球菌(Sp)及50例临床样本,评估CRISPER-LAMP单管一步法的特异性。
结果CRISPER-LAMP单管一步法可在1 h内实现Mp DNA的可视化检测,检出限为10 fg/μL, 聚合酶链式反应(PCR)法检出限为100 fg/μL; CRISPER-LAMP单管一步法检测FluA、FluB、Kp和Sp结果均为阴性; 50例临床样本检测结果均与临床诊断结果相符,且CRISPER-LAMP与PCR法一致性较好(Kappa=1)。
结论CRISPER-LAMP单管一步法检测Mp简便、快速、灵敏度高,且特异性强,检测不需任何特殊设备,检测过程中无气溶胶污染,其有望成为快速检测Mp的新方法。
-
关键词:
- 成簇的规律间隔的短回文重复序列 /
- 环介导等温扩增 /
- 肺炎支原体 /
- 可视化检测 /
- 引物
Abstract:ObjectiveTo establish clusters of regularly interspaced short palindromic repeats (CRISPR)-Cas12a technology combined with loop-mediated isothermal amplification (LAMP) single-tube one-step method for rapid detection of Mycoplasma pneumoniae (Mp), and to explore its application value in clinical diagnosis.
MethodsMp LAMP primers were designed and optimized to design Cas12a CrRNA according to LMAP product targets. The sensitivity of CRISPER-LAMP single-tube one-step method for Mp DNA detection was analyzed; the Mp, influenza virus A (FluA), influenza virus B (FluB), Klebsiella pneumoniae (Kp), Streptococcus pneumoniae (Sp) and 50 clinical samples were detected, and the specificity of CRISPER-LAMP single-tube one-step method was evaluated.
ResultsMp DNA could be visualized within 1 hour by CRISPER-LAMP single-tube one-step method, with a detection limit of 10 fg/μL and a detection limit of 100 fg/μL by polymerase chain reaction (PCR); the FluA, FluB, Kp and Sp were all negative detected by CRISPER-LAMP single-tube one-step method; the detection results of 50 clinical samples were consistent with the clinical diagnosis results, and the consistency between CRISPER-LAMP and PCR method was good (Kappa=1).
ConclusionCRISPER-LAMP single-tube one-step method for Mp detection is simple, rapid, sensitive and specific. It does not need any special equipment, and there is no aerosol pollution in the detection process. It is expected to become a new method for rapid detection of Mp.
-
肺炎支原体(Mp)是一种常见的病原微生物,主要通过呼吸道传播,其不仅可引起多种呼吸道疾病,还可导致肺外其他系统的多种并发症[1]。呼吸道病原体引起的感染症状比较相似,很难靠临床症状及常规检测方法进行明确的早期诊断。因此,快速、高灵敏、高特异性的检测方法对诊断、鉴别呼吸道病原体感染至关重要。环介导等温扩增(LAMP)技术实现了恒温条件下的连续快速扩增核酸片段[2], 但该技术也存在缺陷,其没有聚合酶链式反应(PCR)热循环以避免引物之间的结合,因此恒定温度下的反应很难避免部分非特异性扩增[3]。
成簇的规律间隔的短回文重复序列(CRISPR)技术是一种以序列特异性方式修饰内部DNA/RNA编辑基因的技术,具有简单、廉价和高效等优势。为解决LAMP非特异扩增的缺点,研究人员已经开始使用CRISPR结合LAMP来进行核酸的体外检测[4-5], 其已成功应用于农业、治疗和感染因子、食品工业和生物能源等众多领域[6]。本研究拟建立CRISPR-LAMP检测Mp的新方法,以实现Mp快速、精准检测。
1. 材料与方法
1.1 临床样本
选取2021年1月—2021年12月入住苏北人民医院儿科的患儿50例,其中30例为Mp感染, 20例为非Mp感染。采集患儿口咽拭子, -70 ℃储存,集中进行检测。
1.2 材料
Loopamp®DNA扩增试剂盒和LAMP法荧光检测试剂盒购自日本荣研公司, EnGen®Lba Cas12a (Cpf1)购自New England Biolabs公司, MpDNA质控品购自广州健仑生物科技有限公司,甲流病毒(FluA)标准物质及乙流病毒(FluB)标准物质购自上海计量院,肺炎克雷伯氏菌(Kp)、肺炎链球菌(Sp)临床菌株来源于本院医学检验科微生物室。
1.3 引物设计
采用Primer Explorer Version 5软件设计LAMP引物,采用Deskgen软件设计CRISPR/Cas12a crRNA, 委托上海生工生物工程有限公司合成。引物及crRNA序列见表 1。
表 1 Mp LAMP引物及crRNA序列引物名称 序列(5′→3′) F3 CCACCTAGTGATTTGGAAGA B3 GGACAAAGAAGATTTTCGAAGTT FIP GCTGAACATCAACAAAGAAGGTGCATTGTTGATGAATGTACTACCCA BIP ATACCCCACAATTAAGTGGTTGATTCATAGAATATCTGTCCATCTGG LBcrRNA CTGCACGCATAGTAACAAACTGGAAUUUCUACUGUUGUAGAUCGUCCCGUUGCGCCUAACGGGUGU 1.4 CRISPR-LAMP单管一步法检测
LAMP引物配制,使用去离子双蒸水溶解引物至如下工作浓度: F3(5 μmol/L)、B3(5 μmol/L)、FIP(40 μmol/L)、BIP(40 μmol/L)、LB(40 μmol/L)。
LAMP反应液12.5 μL∶2×反应缓冲液(RM), 6.0 μL; F3、B3、FIP、BIP、LB各0.5 μL; Bst DNA聚合酶0.5 μL; 去离子水2.5 μL、DNA 1.0 μL。
Crispr 12a反应液: 2.0 μL 10×NEB buffer, 7.5 μL H2O, 1.0 μL Cas12a, 1.0 μL crRNA, 1.0 μL ssDNA report。
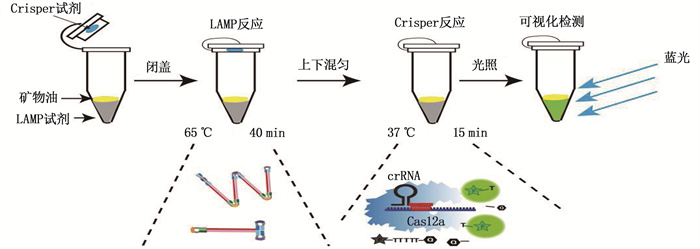
CRISPR-LAMP单管一步法反应体系为25.0 μL, 检测步骤及流程见图 1。将12.5 μL Crispr/Cas12a试剂加在试管盖上, 12.5 μL LAMP反应试剂加在管底,并在LAMP试剂上加1层矿物油; 盖上管盖, 65 ℃反应40 min; 将试管上下颠倒混匀, Cas12a试剂与LAMP反应产物充分混匀后, 37 ℃反应15 min; 470 nm蓝光灯(蓝光透射仪OSE-470-12)照射反应试管,阳性结果呈现绿色荧光。
1.5 Mp PCR方法
Mp检测的引物序列为F: 5′-GGCCGTAACTA TAACGGTCC-3′; R: 5′- AGACCCCGTGAAGCTTT ACT-3。扩增条件: 95 ℃预变性3 min; 30循环,条件为95 ℃ 30 s, 56 ℃ 30 s, 72 ℃ 60 s, 72 ℃ 10 min。使用仪器为天隆科技Genesy 96T基因扩增热循环仪,购自西安天隆科技有限公司。
1.6 灵敏度分析
Mp基因组DNA稀释至10.0 ng/μL, 应用NanoDrop 1000微量紫外可见分光光度计(美国Thermo Scientific), 配置1×106 fg/μL、1×104 fg/μL、1×102 fg/μL、1×10 fg/μL和1 fg/μL的Mp DNA标准品。ddH2O为阴性对照。分别采用CRISPER-LAMP单管一步法和PCR法检测上述标准品,以评估CRISPER-LAMP单管一步法的灵敏度。
1.7 特异性分析
采用AllPrep®DNA Mini Kit试剂盒提Kp、Sp基因组DNA, 每份DNA样本稀释至10 ng/μL与MpDNA质控品、FluA标准物质及FluB标准物质进行CRISPER-LAMP单管一步法检测。
1.8 统计学方法
PCR法结果与CRISPER-LAMP单管一步法结果一致性采用Cohen′s Kappa检验。
2. 结果
2.1 CRISPR-LAMP单管一步法检测Mp灵敏度
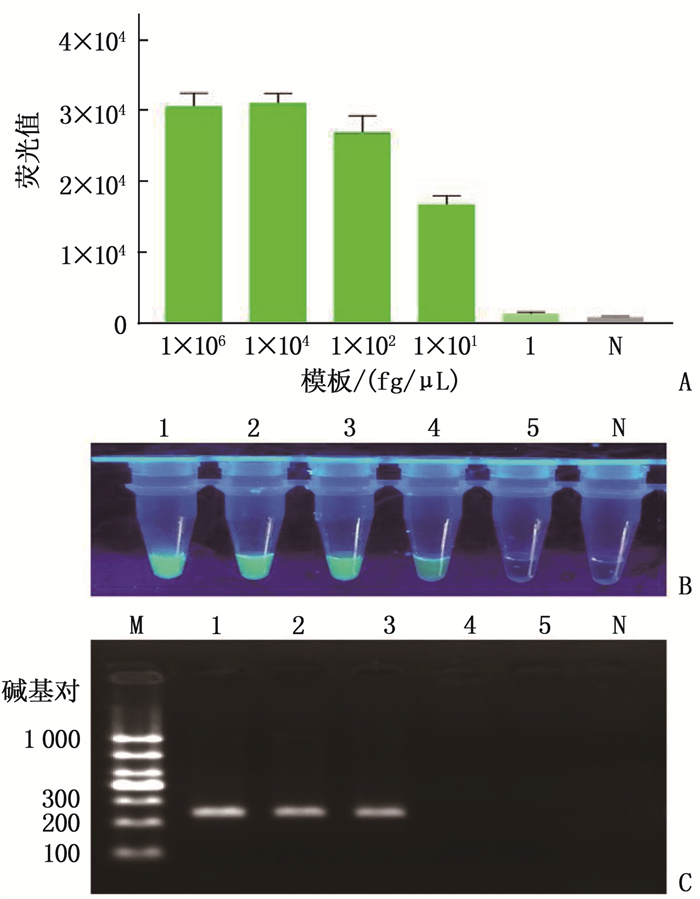
以稀释的Mp DNA标准品为检测模板进行反应, CRISPR-LAMP单管一步法结果见图 2A、2B。A为荧光检测仪(Biotek Synergy)检测反应产物荧光值, B为可视化检测结果。应用琼脂糖凝胶电泳法检测PCR法扩增Mp DNA系列浓度标准品的产物,结果见图 2C。结果显示, CRISPR-LAMP单管一步法检测Mp检出限为10 fg/μL, PCR法检测Mp检出限为100 fg/μL。
2.2 CRISPR-LAMP单管一步法检测Mp的特异性分析
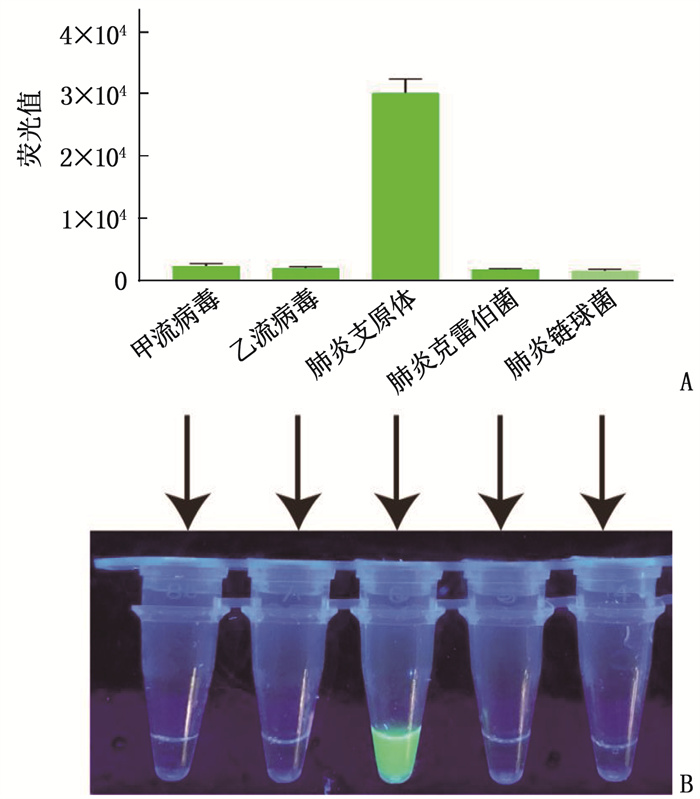
CRISPR-LAMP单管一步法检测FluA, FluB、Kp、Sp反应均为阴性; Mp为阳性,结果见图 3A、3B。结果显示, CRISPR-LAMP单管一步法检测Mp具有高特异性,与咽拭子中可能存在的病原体不存在交叉污染检测。
2.3 CRISPR-LAMP法与PCR法检测临床样本的一致性
CRISPR-LAMP单管一步法检测50例临床标本(30例Mp感染样本; 20例临床非Mp感染标本),其中30例阳性, 20例阴性。CRISPR-LAMP单管一步法与PCR法一致性较好(Kappa值为1), 见表 2。
表 2 CRISPR-LAMP法与PCR法检测临床标本一致性(n=50)CRISPR-LAMP法 PCR法 Kappa值 + - + 30 0 1 - 0 20 “+”表示阳性结果,“-”表示阴性结果。 3. 讨论
实验室病原学检测是Mp感染诊断的关键,检测Mp的传统方法为分离培养和血清学试验。但培养法因周期较长、灵敏度低在临床应用中受到极大限制; 血清学抗体检测也不能实现Mp早期检测,故上述方法限制了其在临床实验室的广泛开展[7]。PCR技术在实验室诊断中起到了关键的作用,目前已成为Mp首推的重要的检测手段之一,但用于临床实验室的PCR技术都需依赖特定场所、设备、仪器及经培训上岗的工作人员,操作复杂、费时、技术要求高,不适合Mp检测的常规开展[8]。血清学、培养法、分子检测在临床实践中各有优缺点,因此亟需研发、转化可灵敏、准确鉴定Mp的新技术方法。
LAMP技术已应用于塞卡病毒、新型冠状病毒(SARS-CoV-2)等多种病原体的检测[9-11]。该技术克服了传统PCR反应需通过反复热变性过程获得单链模板的缺点,并避免了反复降温的耗时过程,可以在15~60 min扩增出109~1010倍靶序列拷贝,具有高灵敏度和扩增效率。CRISPR-Cas系统是原核生物中的一种适应性免疫系统,其在细菌宿主染色体中以病毒DNA的形式存储记忆,以防止噬菌体感染[12]。在CRISPR-Cas效应子家族中, Cas12a系统能在识别靶点后诱导任意单链DNA(ssDNA)的分裂,在分裂位点释放荧光信号[13]。
本研究利用CRISPR可进一步提高LAMP反应的特异性这一优势,建立了CRISPR-LAMP单管一步法检测Mp。因CRISPR-Cas12a系统的高特异性,当特殊设计的crRNA与靶标Mp病原体DNA配对后,与Cas12a蛋白形成复合物,激活该蛋白的切割活性,进而引起荧光信号的释放,从而应用蓝光透射仪实现了荧光可视化的检测。该法可检测到10 fg/μL的Mp DNA, 检测灵敏度高于传统的PCR技术(100 fg/μL)一个数量级,与TAO D G等[14]研究结论相一致。
在核酸检测实验中的主要问题是气溶胶污染导致的假阳性[15]。本方法中虽然LAMP扩增温度为65 ℃, CRISPR体系的反应温度为37 ℃, 但本研究组利用矿物油把2个反应系统分隔放置在一个试管的不同位置。LAMP扩增反应首先在离心管中进行,在进行过程中, CRISPR体系试剂将在管盖内保持相对稳定。当LAMP扩增反应完成后, CRISPR体系试剂通过人为混匀进入LAMP扩增后的体系中,并进行核酸检测,然后对反应混合物进行荧光成像检测,故本方法可以有效减少气溶胶污染。
本研究建立的方法检测了50例经确诊的临床样本,其中有30例为阳性, 20例为阴性,结果均与PCR结果一致, Kappa值为1, 表明2种方法一致性很好。此方法检测FluA、FluB、Kp、Sp反应均为阴性,显示其具有高特异性。但本法存在以下3点不足: ①由于LAMP反应的温度为65 ℃, 此温度对CRISPR体系中的Cas12a、crRNA和ssDNA report 3种试剂产生影响的程度以及是否对最终实验结果产生影响,本研究将会在后续的实验中逐步加以验证。②在此法评价灵敏度时,本研究实验结果为10 fg/μL, 实际的检测限应该小于10 fg/μL, 后续本研究将会评价10 fg/μL至1 fg/μL之间的其他浓度,以期找到此法“真实”的检出限。③在此法评价特异性时,本研究选取了除Mp外4种病原体,仍不够全面,在后续的实验中本研究将会增加引起呼吸道感染的其他病原体,继续探究本检测方法的特异性。此外检测临床样本仅有50例,存在偶然性及片面性。
综上所述,本研究将LAMP的强大病原体扩增优势与CRISPR-Cas12a对Mp DNA特异性检测能力相结合,建立了单管一步法检测Mp的方法,该法简便、快速,检测过程中无需开盖、无气溶胶污染,并可在1 h后可读取结果; 检测灵敏度达到了10 fg/μL, 且特异性强不受其他病原体干扰,不需要高端复杂的设备。CRISPER-LAMP单管一步法有望成为检测Mp的新手段,可为社区及基层医院广泛检测Mp提供新方法。
-
表 1 Mp LAMP引物及crRNA序列
引物名称 序列(5′→3′) F3 CCACCTAGTGATTTGGAAGA B3 GGACAAAGAAGATTTTCGAAGTT FIP GCTGAACATCAACAAAGAAGGTGCATTGTTGATGAATGTACTACCCA BIP ATACCCCACAATTAAGTGGTTGATTCATAGAATATCTGTCCATCTGG LBcrRNA CTGCACGCATAGTAACAAACTGGAAUUUCUACUGUUGUAGAUCGUCCCGUUGCGCCUAACGGGUGU 表 2 CRISPR-LAMP法与PCR法检测临床标本一致性(n=50)
CRISPR-LAMP法 PCR法 Kappa值 + - + 30 0 1 - 0 20 “+”表示阳性结果,“-”表示阴性结果。 -
[1] 吕静. 小儿肺炎支原体肺炎细胞免疫和体液免疫指标检测的临床价值[J]. 实用临床医药杂志, 2019, 23(6): 107-109. https://www.cnki.com.cn/Article/CJFDTOTAL-XYZL201906029.htm [2] NOTOMI T, OKAYAMA H, MASUBUCHI H, et al. Loop-mediated isothermal amplification of DNA[J]. Nucleic Acids Res, 2000, 28(12): E63. doi: 10.1093/nar/28.12.e63
[3] VENKATESAN G, BHANUPRAKASH V, BALAMURUGAN V. Development and comparative evaluation of loop mediated isothermal amplification (LAMP) assay for simple visual detection of orf virus in sheep and goats[J]. Mol Cell Probes, 2015, 29(3): 193-195. doi: 10.1016/j.mcp.2015.03.006
[4] ALI Z, AMAN R, MAHAS A, et al. iSCAN: an RT-LAMP-coupled CRISPR-Cas12 module for rapid, sensitive detection of SARS-CoV-2[J]. Virus Res, 2020, 288: 198129. doi: 10.1016/j.virusres.2020.198129
[5] BROUGHTON J P, DENG X D, YU G X, et al. CRISPR-cas12-based detection of SARS-CoV-2[J]. Nat Biotechnol, 2020, 38(7): 870-874. doi: 10.1038/s41587-020-0513-4
[6] NIDHI S, ANAND U, OLEKSAK P, et al. Novel CRISPR-cas systems: an updated review of the current achievements, applications, and future research perspectives[J]. Int J Mol Sci, 2021, 22(7): 3327. doi: 10.3390/ijms22073327
[7] WAITES K B, XIAO L, LIU Y, et al. Mycoplasma pneumoniae from the respiratory tract and beyond[J]. Clin Microbiol Rev, 2017, 30(3): 747-809. doi: 10.1128/CMR.00114-16
[8] TANG M Y, WANG D, TONG X, et al. Comparison of different detection methods for Mycoplasma pneumoniae infection in children with community-acquired pneumonia[J]. BMC Pediatr, 2021, 21(1): 90. doi: 10.1186/s12887-021-02523-4
[9] WANG X, YIN F G, BI Y H, et al. Rapid and sensitive detection of Zika virus by reverse transcription loop-mediated isothermal amplification[J]. J Virol Methods, 2016, 238: 86-93. doi: 10.1016/j.jviromet.2016.10.010
[10] CURTIS K A, MORRISON D, RUDOLPH D L, et al. A multiplexed RT-LAMP assay for detection of group M HIV-1 in plasma or whole blood[J]. J Virol Methods, 2018, 255: 91-97. doi: 10.1016/j.jviromet.2018.02.012
[11] YAN C, CUI J, HUANG L, et al. Rapid and visual detection of 2019 novel coronavirus (SARS-CoV-2) by a reverse transcription loop-mediated isothermal amplification assay[J]. Clin Microbiol Infect, 2020, 26(6): 773-779. doi: 10.1016/j.cmi.2020.04.001
[12] 栾天. 胸膜肺炎放线杆菌RPA-Cas12a检测方法的建立和初步应用[D]. 北京: 中国农业科学院, 2021. [13] NGUYEN L T, SMITH B M, JAIN P K. Enhancement of trans-cleavage activity of Cas12a with engineered crRNA enables amplified nucleic acid detection[J]. Nat Commun, 2020, 11(1): 4906. doi: 10.1038/s41467-020-18615-1
[14] TAO D G, LIU J J, NIE X W, et al. Application of CRISPR-Cas12a enhanced fluorescence assay coupled with nucleic acid amplification for the sensitive detection of African swine fever virus[J]. ACS Synth Biol, 2020, 9(9): 2339-2350. doi: 10.1021/acssynbio.0c00057
[15] 李云龙, 张健, 魏艳秋, 等. 分子诊断实验室去除核酸污染的方法学研究[J]. 生物工程学报, 2021, 37(2): 673-679. https://www.cnki.com.cn/Article/CJFDTOTAL-SHWU202102028.htm -
期刊类型引用(1)
1. 李利娟,武洁,尚新秀,冯伟勋. 醒脾化浊方对糖尿病前期痰湿体质患者的疗效及对血糖水平和肾功能指标的影响. 实用临床医药杂志. 2025(04): 60-63 .  本站查看
本站查看
其他类型引用(0)




 下载:
下载:
 苏公网安备 32100302010246号
苏公网安备 32100302010246号
