Predictive value of transvaginal ultrasound blood flow parameters combined with serum anti-mullerian hormone for in vitro fertilization embryo transfer pregnancy failure in polycystic ovary syndrome infertility
-
摘要:目的
探讨经阴道超声血流参数联合血清抗苗勒管激素(AMH)对多囊卵巢综合征(PCOS)不孕症体外受精-胚胎移植(IVF-ET)妊娠失败的预测价值。
方法选取行IVF-ET的173例PCOS不孕症患者为研究对象, 其中脱落12例。根据胚胎移植后第28天阴道B超结果将161例患者分为妊娠失败组(n=96)与妊娠成功组(n=65)。比较2组阻力指数(RI)、搏动指数(PI)、收缩与舒张末期最大血流速度比值(S/D)和血清AMH水平。采用多因素Logistic回归分析法分析PCOS不孕症IVF-ET妊娠失败的影响因素。绘制受试者工作特征(ROC)曲线,分析RI、PI、S/D、血清AMH水平单独及联合评估对PCOS不孕症患者IVF-ET妊娠失败的预测价值。
结果妊娠失败组血清AMH水平低于妊娠成功组,血流RI、PI、S/D高于妊娠成功组,差异有统计学意义(P < 0.001)。RI(OR=4.688, 95%CI: 2.878~6.498)、PI(OR=4.332, 95%CI: 2.277~6.387)、S/D(OR=3.773, 95%CI: 1.856~5.691)、月经第3天黄体生成素(LH)/促卵泡生成素(FSH)值(OR=2.998,95%CI: 1.236~4.760)高是PCOS不孕症IVF-ET妊娠失败的危险因素(P < 0.05); 月经第3天FSH水平高(OR=0.579, 95%CI: 0.416~0.806)、血清AMH水平高(OR=0.722, 95%CI: 0.533~0.911)及人绒毛膜促性腺激素(hCG)日子宫内膜厚(OR=0.632, 95%CI: 0.421~0.843)是PCOS不孕症IVF-ET妊娠失败的保护因素(P < 0.05)。RI、PI、S/D联合血清AMH水平预测PCOS不孕症IVF-ET妊娠失败的灵敏度、特异度、曲线下面积(AUC)分别为95.83%、80.00%、0.933。
结论超声血流参数联合AMH对PCOS不孕症IVF-ET妊娠失败具有较好的预测价值。
Abstract:ObjectiveTo explore the predictive value of transvaginal ultrasound blood flow parameters combined with serum anti mullerian hormone (AMH) for in vitro fertilization embryo transfer (IVF-ET) pregnancy failure in infertility with polycystic ovary syndrome (PCOS).
MethodsA total of 173 infertile PCOS patients who underwent IVF-ET were selected as the study objects, of which 12 cases fell off. According to the results of vaginal Bultrasound on the 28th day after embryo transfer, 161 patients were divided into failed pregnancy group (n=96) and successful pregnancy group (n=65). The levels of resistance index (RI), pulsatile index (PI), ratio of maximum systolic to diastolic blood flow velocity (S/D), and serum AMH were compared between the two groups. Multivariate Logistic regression analysis was used to analyze the influencing factors of pregnancy failure in IVF-ET with PCOS infertility. Receiver operating characteristic (ROC) curves were drawn to analyze RI, PI, S/D and serum AMH levels alone and their combination to evaluate the predictive valueof IVF-ET pregnancy failure in PCOS infertility patients.
ResultsThe serum AMH level in the failed pregnancy group was significantly lower than that in the successful pregnancy group, and the blood flow RI, PI and S/D were higher than those in the successful pregnancy group (P < 0.001). RI (OR=4.688, 95%CI, 2.878 to 6.498), PI (OR=4.332, 95%CI, 2.277 to 6.387), S/D (OR=3.773, 95%CI, 1.856 to 5.691) and luteinizing hormone (LH)/follicle stimulating hormone (FSH) values on the third day of menstrual cycle (OR=2.998, 95%CI, 1.236 to 4.760) were the risk factors for pregnancy failure in PCOS infertility IVF-ET (P < 0.05); high FSH level on the third day of menstruation (OR=0.579, 95%CI, 0.416 to 0.806), high serum AMH level (OR=0.722, 95%CI, 0.533 to 0.911) and endometrial thickness on human chorionic gonadotropin (hCG)day (OR=0.632, 95%CI, 0.421 to 0.843) were protective factors for pregnancy failure in IVF-ET in PCOS infertility (P < 0.05). The sensitivity, specificity and area under the curve (AUC) of RI, PI and S/D combined with serum AMH levels in predicting pregnancy failure in IVF-ET of PCOS infertility were 95.83%, 80.00% and 0.933, respectively.
ConclusionThe combination of ultrasonic blood flow parameters and AMH has a good value in predicting pregnancy failure in IVF-ET of PCOS infertility.
-
多囊卵巢综合征(PCOS)是一种内分泌异常和代谢异常的疾病,多发生于育龄期女性,以无排卵或稀发排卵、胰岛素抵抗等为主要临床特征[1]。研究[2]显示,约有15%的育龄期PCOS患者会发生不孕,临床主要通过促排卵并行体外受精-胚胎移植(IVF-ET)等辅助生殖技术进行治疗。但由于PCOS患者内分泌环境紊乱、代谢异常,易引起卵母细胞质量、胚胎发育、子宫内膜容受性异常等问题,从而影响患者妊娠结局[3]。因此,需寻求能够有效预测PCOS不孕症IVF-ET妊娠失败的相关指标,以期为临床及时干预和积极治疗提供参考依据。近年来,经阴道彩色多普勒超声被广泛应用于妇科疾病的诊断预测中,其可靠性强、操作方便快捷、安全性高,能够有效监测卵巢、子宫变化及血流情况[4]。既往研究[5]显示,经阴道三维超声可用于评估子宫内膜容受性,对预测IVF-ET患者妊娠结局具有一定意义。抗苗勒管激素(AMH)水平的高低与卵巢储备功能密切相关,能够有效预测卵巢储备功能[6], 但对PCOS不孕症IVF-ET妊娠结局的预测价值尚未达成一致。鉴于此,本研究对行IVF-ET的PCOS不孕症患者行阴道超声检测和血清AMH水平检测,并分析经阴道超声血流参数联合血清AMH对PCOS不孕症IVF-ET妊娠失败的预测价值,以期为临床改善妊娠结局提供参考。
1. 资料与方法
1.1 一般资料
纳入标准: ①符合PCOS诊断标准[7]且不孕者; ②首次行IVF-ET治疗者; ③配偶精液检查结果正常者; ④年龄20~35岁者; ⑤子宫及卵巢形态正常者; ⑥在IVF-ET治疗前3个月内未服用促排卵药物、激素类药物者; ⑦性生活无异常、无避孕需求者; ⑧知情同意者。排除标准: ①存在宫腔粘连、子宫腺肌症等影响胚胎着床的子宫疾病者; ②合并心、肝、肾等重要脏器病变者; ③输卵管病变者; ④合并自身免疫系统、血液系统、内分泌系统疾病者; ⑤合并子宫恶性肿瘤者; ⑥夫妻任一方染色体异常。脱落标准: ①研究过程中失访者; ②研究过程中发生死亡等不良事件者; ③其他各种原因提前退出研究者。
根据样本量计算公式N=Z2×σ2/d2(其中Z=1.96, σ=0.5, d=78.21%, 得出N≈157)以及上述标准,同时考虑研究过程中样本量的脱落情况等因素影响(脱落率设为10%, 计算总样本量为173例),共选取2021年6月—2022年12月收治的行IVF-ET的173例PCOS不孕症患者为研究对象,并分为妊娠失败组和妊娠成功组。本研究已通过医院伦理委员会审核批准。
1.2 方法
1.2.1 阴道超声检测
所有PCOS不孕症患者于胚胎移植日,采用GE Voluson E8三维彩色多普勒超声诊断仪进行阴道超声检查。受试者检查前排空膀胱,取膀胱截石位,在探头表面涂抹少许润滑剂并套一次性避孕套,将探头经阴道缓慢送至阴道穹窿处,转动探头,对子宫矢状切面内膜与肌层交界处的暗带区域、彩色血流最明亮处进行扫查,获取子宫螺旋动脉血流多普勒频谱,自动检测获得血流动力学参数阻力指数(RI)、搏动指数(PI)、收缩与舒张末期最大血流速度比值(S/D), 测量3次,取平均值。
1.2.2 血清AMH水平检测
所有PCOS不孕症患者于胚胎移植日,抽取清晨空腹状态下静脉血5 mL, 以3 000转/min离心10 min后,取上层清液,置于-80 ℃保存。采用酶联免疫吸附法检测血清AMH水平,相关试剂盒购自CUSABIO公司。
1.2.3 资料收集
收集PCOS不孕症患者的临床资料,包括年龄、体质量指数(BMI)、不孕年限等一般资料。月经第3天检测促卵泡生成素(FSH)、黄体生成素(LH)水平及LH/FSH值。通过阴道B超检查测定窦卵泡数(AFC)、获卵总数、MII卵数、受精卵数、优质胚胎数,促性腺激素(Gn)刺激时间, Gn总剂量,人绒毛膜促性腺激素(hCG)日雌二醇(E2)水平及子宫内膜厚度等资料。
1.2.4 IVF-ET术后妊娠结局判断标准
胚胎移植后第14天检测患者血β人绒毛膜促性腺激素(β-hCG), 初步判断是否妊娠,阴性者为未孕,停止黄体支持; 阳性者继续进行黄体支持,胚胎移植后第28天经阴道B超检查可见妊娠囊、卵黄囊诊断为临床妊娠,纳入妊娠成功组,未见妊娠囊即为生化妊娠,未孕及生化妊娠纳入妊娠失败组。
1.3 观察指标
① 比较妊娠失败组与妊娠成功组一般资料及RI、PI、S/D、血清AMH水平; ②分析PCOS不孕症IVF-ET妊娠失败的影响因素; ③分析RI、PI、S/D对PCOS不孕症IVF-ET妊娠失败的预测价值,其中任1项预测为妊娠失败即认为联合预测为妊娠失败; ④分析阴道RI、PI、S/D、血清AMH水平单独及联合对PCOS不孕症IVF-ET妊娠失败的预测价值,其中任1项预测为妊娠失败即认为联合预测为妊娠失败。
1.4 统计学分析
采用SPSS 23.0软件分析数据。年龄、BMI、不孕年限、月经第3天FSH、LH及LH/FSH值、hCG日E2及子宫内膜厚度、AFC、优质胚胎数、RI、PI、S/D、AMH均为计量资料,经K-S检验均符合正态分布(P>0.05), 采用(x±s)表示,组间比较行独立样本t检验; Gn刺激时间、Gn总剂量、获卵总数、MII卵数、受精卵数均为计数资料,采用[n(%)]表示,行χ2检验; 采用多因素Logistic回归分析法分析PCOS不孕症患者IVF-ET妊娠失败的影响因素,变量筛选方法为逐步后退法; 绘制受试者工作特征(ROC)曲线,分析经阴道超声血流参数联合血清AMH水平对PCOS不孕症IVF-ET妊娠失败的预测价值,将预测妊娠失败约登指数最大时对应的指标值记录为最佳截断点(Cut-off值),以曲线下面积(AUC)评价不同指标预测妊娠失败的效能, AUC的比较采用秩和检验。P < 0.05为差异有统计学意义。
2. 结果
2.1 2组一般资料及RI、PI、S/D及血清AMH水平比较
173例PCOS不孕症患者脱落12例, IVF-ET妊娠失败率为59.63%(96/161)。妊娠失败组(n=96)和妊娠成功组(n=65)的年龄、BMI、月经第3天LH水平、hCG日E2水平、Gn刺激时间、Gn总剂量、MII卵数、受精卵数比较,差异无统计学意义(P>0.05); 妊娠失败组月经第3天FSH水平、AFC、hCG日子宫内膜厚度、优质胚胎数、血清AMH水平均低于或小于妊娠成功组, LH/FSH值、获卵总数 < 5个占比、RI、PI、S/D均高于妊娠成功组,差异有统计学意义(P < 0.05)。见表 1。
表 1 2组临床资料比较(x±s))[n(%)]指标 妊娠失败组(n=96) 妊娠成功组(n=65) t/χ2 P 年龄/岁 28.48±5.07 29.10±4.89 0.772 0.441 BMI/(kg/m2) 22.53±2.89 22.08±2.77 0.986 0.326 不孕年限/年 4.07±0.72 3.95±0.53 1.149 0.252 月经第3天FSH/(U/L) 5.85±1.52 6.35±1.23 2.207 0.029 月经第3天LH/(U/L) 8.17±1.25 7.93±1.67 1.042 0.299 月经第3天LH/FSH值 1.40±0.41 1.25±0.33 2.459 0.015 hCG日E2/(pmol/L) 7 893.26±2 032.88 8 092.75±2 451.27 0.562 0.575 AFC/个 12.35±3.27 13.59±4.22 2.097 0.038 Gn刺激时间 ≥10 d 66(68.75) 49(75.38) 0.836 0.361 < 10 d 30(31.25) 16(24.62) Gn总剂量 ≥2 000 IU 58(60.42) 43(66.15) 0.546 0.460 < 2 000 IU 38(39.58) 22(33.85) 获卵总数 ≥5个 31(32.29) 32(49.23) 4.669 0.031 < 5个 65(67.71) 33(50.77) MII卵数 ≥5个 28(29.17) 28(43.08) 3.306 0.069 < 5个 68(70.83) 37(56.92) hCG日子宫内膜厚度/mm 9.15±1.02 9.89±2.01 3.073 0.002 受精卵数 ≥5个 26(27.08) 27(41.54) 3.667 0.055 < 5个 70(72.92) 38(58.46) 优质胚胎数/个 1.50±0.23 1.57±0.27 2.017 0.045 RI 0.69±0.23 0.55±0.14 4.386 < 0.001 PI 1.48±0.37 1.18±0.28 5.547 < 0.001 S/D 2.99±0.66 2.55±0.44 4.710 < 0.001 AMH/(ng/mL) 3.17±1.01 4.37±0.90 7.724 < 0.001 BMI: 体质量指数; FSH: 促卵泡生成素; LH: 黄体生成素; LH/FSH: 黄体生成素/促卵泡生成素比值;
E2: 雌二醇; AFC: 窦卵泡数; Gn: 促性腺激素; hCG: 绒毛膜促性腺激素; RI: 阻力指数; PI: 搏动指数;
S/D: 收缩与舒张末期最大血流速度比值; AMH: 抗苗勒管激素。2.2 PCOS不孕症IVF-ET妊娠失败的影响因素分析
将一般资料中P < 0.05的因素记为自变量并进行赋值: 血流RI、PI、S/D、血清AMH水平、月经第3天FSH、LH/FSH值、AFC、hCG日子宫内膜厚度、优质胚胎数(实测值)、获卵总数(≥5个=0, < 5个=1), 另将PCOS不孕症患者IVF-ET妊娠结局记为因变量(妊娠成功=0, 妊娠失败=1), 进行多因素Logistic回归分析,排除共线性因素(方差膨胀系数值>10), 结果显示, RI、PI、S/D、月经第3天LH/FSH值高均是PCOS不孕症IVF-ET妊娠失败的危险因素(P < 0.05), 月经第3天FSH水平、血清AMH水平高及hCG日子宫内膜厚是PCOS不孕症IVF-ET妊娠失败的保护因素(P < 0.05)。见表 2。
表 2 PCOS不孕症IVF-ET妊娠失败的影响因素分析影响因素 B SE Wald P OR 95%CI RI 1.545 0.477 10.491 0.001 4.688 2.878~6.498 PI 1.466 0.498 8.666 0.004 4.332 2.277~6.387 S/D 1.328 0.379 12.278 < 0.001 3.773 1.856~5.691 AMH -0.326 0.101 10.418 0.001 0.722 0.533~0.911 月经第3天FSH -0.547 0.169 10.476 0.001 0.579 0.416~0.806 月经第3天LH/FSH值 1.098 0.322 11.628 < 0.001 2.998 1.236~4.760 AFC 0.178 0.107 2.767 0.109 1.195 1.004~1.386 hCG日子宫内膜厚度 -0.459 0.154 8.883 0.004 0.632 0.421~0.843 优质胚胎数 0.053 0.034 2.430 0.119 1.054 1.000~1.309 获卵总数 < 5个 0.212 0.129 2.701 0.111 1.236 1.012~1.560 RI: 阻力指数; PI: 搏动指数; S/D: 收缩与舒张末期最大血流速度比值; AMH: 抗苗勒管激素; FSH: 促卵泡生成素;
LH/FSH: 黄体生成素/促卵泡生成素比值; AFC: 窦卵泡数; hCG: 人绒毛膜促性腺激素。2.3 RI、PI、S/D对PCOS不孕症IVF-ET妊娠失败预测价值分析
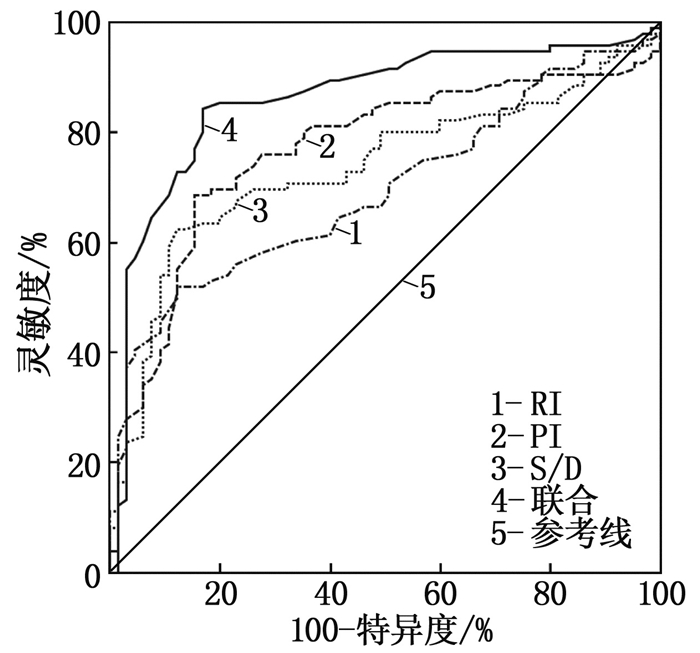
PI、RI、S/D联合预测PCOS不孕症IVF-ET妊娠失败的灵敏度高于各项单独预测, AUC均大于各项单独预测(Z=2.799, P=0.005; Z=2.029, P=0.042; Z=2.502, P=0.012), 特异度均与各项单独预测基本一致。见表 3、图 1。
表 3 RI、PI、S/D对PCOS不孕症IVF-ET妊娠失败的预测价值指标 cut-off值 灵敏度/% 特异度/% AUC 95%CI RI 0.68 52.08 87.69 0.696 0.618~0.766 PI 1.42 68.75 84.62 0.767 0.694~0.830 S/D 2.92 62.50 86.15 0.735 0.660~0.802 联合 — 84.38 83.08 0.861 0.797~0.910 RI: 阻力指数; PI: 搏动指数; S/D: 收缩与舒张末期最大血流速度比值。 2.4 阴道超声血流参数、血清AMH水平单项及联合对PCOS不孕症IVF-ET妊娠失败的预测价值
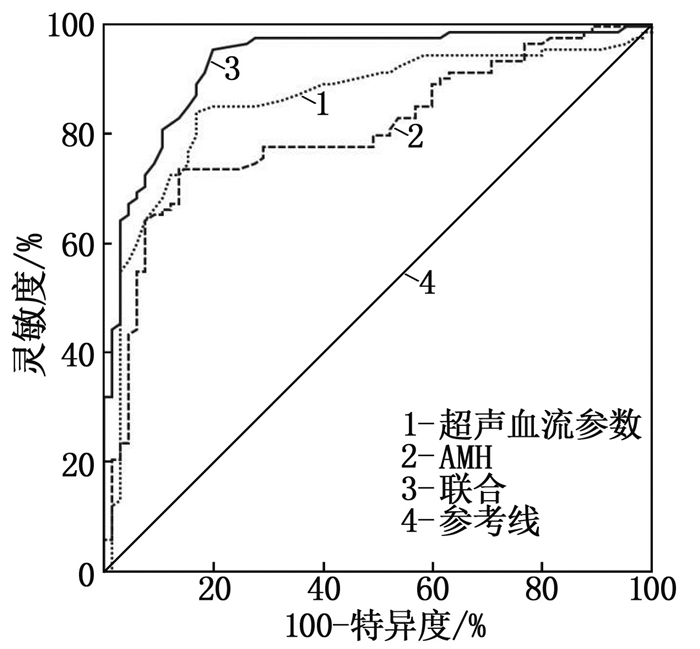
阴道超声血流参数联合血清AMH水平预测PCOS不孕症IVF-ET妊娠失败的灵敏度均高于单独预测, AUC均大于单独预测(Z=1.976, P=0.048; Z=3.174, P=0.002), 特异度均与单独预测比较基本一致。见图 2、表 4。
表 4 阴道超声血流参数、血清AMH水平单项及联合对PCOS不孕症IVF-ET妊娠失败的预测价值指标 cut-off值 灵敏度/% 特异度/% AUC 95%CI 超声血流参数 — 84.38 83.08 0.861 0.797~0.910 抗苗勒管激素 3.78 ng/mL 73.96 86.15 0.808 0.738~0.865 联合 — 95.83 80.00 0.933 0.883~0.966 3. 讨论
PCOS的病因尚不明确,可能与遗传、环境因素有关,卵巢体积增大、卵泡增多等病理变化均会引起排卵障碍而导致不孕[8]。随着医学技术的发展, IVF-ET已成为治疗不孕症的有效手段,但受多种因素的影响,妊娠失败率较高,给患者带来了较大的心理负担和经济压力。本研究中, PCOS不孕症IVF-ET妊娠失败率为59.63%, 与周晓燕等[9]报道的60.58%接近,均提示PCOS不孕症患者IVF-ET后有较高的妊娠失败风险。因此,需寻求可早期预测PCOS不孕症IVF-ET妊娠失败的可靠指标,以指导临床治疗及降低妊娠失败率、改善妊娠结局。
血管状况对胚胎的着床和发育具有重要意义,良好的血流灌注与卵泡的生长发育密切相关。经阴道彩色多普勒超声获得的图像清晰度高,可呈现组织间的结构关系,还能够将感兴趣区域内组织的血管和血流量化[10]。本研究结果显示,妊娠失败组RI、PI、S/D均显著高于妊娠成功组,且多因素Logistic回归分析显示,以上指标均为PCOS不孕症IVF-ET妊娠失败的影响因素。PCOS不孕症患者体内激素水平缺乏周期性变化,子宫内膜血流速度缓慢,血供不足,血流阻力增大,血流RI、PI、S/D水平升高会造成血流灌注差,从而出现血供障碍,而血供障碍的存在会造成子宫内膜增殖缓慢,子宫容受性下降,无法为胚胎着床提供有力条件,故RI、PI、S/D过高表明子宫血流灌注状况较差,不利于妊娠和胚胎着床,增加了妊娠失败风险[11-12]。刘耘利等[13]通过阴道三维超声血流参数RI、PI、S/D预测IVF-ET移植患者的妊娠结局,与二维超声参数相比预测价值更高,为不孕患者的IVF-ET治疗提供指导。本研究采用阴道三维超声血流参数RI、PI、S/D预测PCOS不孕症IVF-ET妊娠失败,结果显示联合预测的灵敏度、特异度、AUC分别为84.38%、83.08%、0.861, 提示RI、PI、S/D对PCOS不孕症IVF-ET妊娠失败具有一定的预测价值,可为临床早期预测妊娠结局提供重要信息。
本研究结果显示,妊娠失败组血清AMH水平低于妊娠成功组,且多因素Logistic回归分析显示,高水平的AMH为PCOS不孕症IVF-ET妊娠失败的保护因素。AMH是转化生长因子β超家族成员,由原始卵泡颗粒细胞产生,并通过卵泡液进入体循环,能够反映卵巢中AFC的储备量,是判断卵巢储备功能的可靠指标[14]。正常情况下,女性青春期后血清AMH水平达到高峰,随着年龄增长,血清AMH水平逐渐下降,而PCOS不孕症患者由于窦前卵泡数目多,血清AMH水平异常升高。相关研究[15]表明,血清AMH水平与IVF-ET临床妊娠成功率呈正相关,血清AMH水平低会对窦前卵泡和小窦卵泡产生抑制作用,从而抑制优势卵泡的发育,严重影响卵子和胚胎质量,导致妊娠失败。相关研究[16]发现,血清AMH水平对PCOS患者性激素具有调节作用,能够促进患者卵泡发育和成熟,影响胚胎质量,本研究在此基础上进一步对血清AMH水平对PCOS不孕症患者IVF-ET妊娠失败的预测价值进行分析,结果显示,血清AMH对PCOS不孕症IVF-ET妊娠失败的灵敏度、特异度、AUC分别为73.96%、86.15%、0.808, 提示血清AMH对PCOS不孕症IVF-ET妊娠失败具有一定的预测价值。因血清AMH水平受年龄影响,其预测PCOS不孕症IVF-ET妊娠失败的灵敏度较低,因此需与2种或多种指标相结合进行预测,以发挥各自优势,提高预测效能。
本研究绘制ROC曲线分析阴道超声血流参数联合血清AMH水平对PCOS不孕症IVF-ET妊娠失败的预测价值,结果发现,联合预测的灵敏度、特异度、AUC分别为95.83%、80.00%、0.933, 其中灵敏度、AUC均高于单独预测,特异度均与单独预测较为接近,提示阴道超声血流参数、血清AMH水平对PCOS不孕症IVF-ET妊娠失败均具有预测价值,但两者联合预测价值更高。这主要是由于阴道超声血流参数从子宫内膜血流变化方面进行预测, AMH从血清生物指标方面对妊娠结局进行预测,两者通过优劣互补,共同提高预测效能。此外,本研究还发现月经第3天LH/FSH值高为PCOS不孕症IVF-ET妊娠失败的危险因素,月经第3天FSH水平高、hCG日子宫内膜厚为保护因素。但既往研究[17-18]中, FSH、LH/FSH预测IVF-ET妊娠结局的灵敏度、特异度均较低, AUC分别为0.672、0.793, 子宫内膜厚度预测IVF-ET妊娠结局的特异度较低,不超过10%, AUC为0.700, 提示FSH、LH/FSH、子宫内膜厚度对IVF-ET妊娠结局的预测价值不甚理想。女性内分泌水平主要通过下丘脑-垂体-卵巢轴进行调节,其中下丘脑能够分泌促性腺激素释放激素来调节LH及FSH水平, PCOS不孕症患者高雄激素血症常表现为FSH水平降低, LH/FSH值升高,从而导致患者排卵障碍,卵母细胞受影响,卵子质量下降,最终导致妊娠失败; hCG日子宫内膜厚,容积大,营养供给充足,子宫容受性升高,适合孕卵着床,有利于妊娠。
综上所述, RI、PI、S/D、血清AMH水平均为PCOS不孕症IVF-ET妊娠失败的影响因素,能够预测PCOS不孕症IVF-ET妊娠结局,二者联用能够提高预测效能。
-
表 1 2组临床资料比较(x±s))[n(%)]
指标 妊娠失败组(n=96) 妊娠成功组(n=65) t/χ2 P 年龄/岁 28.48±5.07 29.10±4.89 0.772 0.441 BMI/(kg/m2) 22.53±2.89 22.08±2.77 0.986 0.326 不孕年限/年 4.07±0.72 3.95±0.53 1.149 0.252 月经第3天FSH/(U/L) 5.85±1.52 6.35±1.23 2.207 0.029 月经第3天LH/(U/L) 8.17±1.25 7.93±1.67 1.042 0.299 月经第3天LH/FSH值 1.40±0.41 1.25±0.33 2.459 0.015 hCG日E2/(pmol/L) 7 893.26±2 032.88 8 092.75±2 451.27 0.562 0.575 AFC/个 12.35±3.27 13.59±4.22 2.097 0.038 Gn刺激时间 ≥10 d 66(68.75) 49(75.38) 0.836 0.361 < 10 d 30(31.25) 16(24.62) Gn总剂量 ≥2 000 IU 58(60.42) 43(66.15) 0.546 0.460 < 2 000 IU 38(39.58) 22(33.85) 获卵总数 ≥5个 31(32.29) 32(49.23) 4.669 0.031 < 5个 65(67.71) 33(50.77) MII卵数 ≥5个 28(29.17) 28(43.08) 3.306 0.069 < 5个 68(70.83) 37(56.92) hCG日子宫内膜厚度/mm 9.15±1.02 9.89±2.01 3.073 0.002 受精卵数 ≥5个 26(27.08) 27(41.54) 3.667 0.055 < 5个 70(72.92) 38(58.46) 优质胚胎数/个 1.50±0.23 1.57±0.27 2.017 0.045 RI 0.69±0.23 0.55±0.14 4.386 < 0.001 PI 1.48±0.37 1.18±0.28 5.547 < 0.001 S/D 2.99±0.66 2.55±0.44 4.710 < 0.001 AMH/(ng/mL) 3.17±1.01 4.37±0.90 7.724 < 0.001 BMI: 体质量指数; FSH: 促卵泡生成素; LH: 黄体生成素; LH/FSH: 黄体生成素/促卵泡生成素比值;
E2: 雌二醇; AFC: 窦卵泡数; Gn: 促性腺激素; hCG: 绒毛膜促性腺激素; RI: 阻力指数; PI: 搏动指数;
S/D: 收缩与舒张末期最大血流速度比值; AMH: 抗苗勒管激素。表 2 PCOS不孕症IVF-ET妊娠失败的影响因素分析
影响因素 B SE Wald P OR 95%CI RI 1.545 0.477 10.491 0.001 4.688 2.878~6.498 PI 1.466 0.498 8.666 0.004 4.332 2.277~6.387 S/D 1.328 0.379 12.278 < 0.001 3.773 1.856~5.691 AMH -0.326 0.101 10.418 0.001 0.722 0.533~0.911 月经第3天FSH -0.547 0.169 10.476 0.001 0.579 0.416~0.806 月经第3天LH/FSH值 1.098 0.322 11.628 < 0.001 2.998 1.236~4.760 AFC 0.178 0.107 2.767 0.109 1.195 1.004~1.386 hCG日子宫内膜厚度 -0.459 0.154 8.883 0.004 0.632 0.421~0.843 优质胚胎数 0.053 0.034 2.430 0.119 1.054 1.000~1.309 获卵总数 < 5个 0.212 0.129 2.701 0.111 1.236 1.012~1.560 RI: 阻力指数; PI: 搏动指数; S/D: 收缩与舒张末期最大血流速度比值; AMH: 抗苗勒管激素; FSH: 促卵泡生成素;
LH/FSH: 黄体生成素/促卵泡生成素比值; AFC: 窦卵泡数; hCG: 人绒毛膜促性腺激素。表 3 RI、PI、S/D对PCOS不孕症IVF-ET妊娠失败的预测价值
指标 cut-off值 灵敏度/% 特异度/% AUC 95%CI RI 0.68 52.08 87.69 0.696 0.618~0.766 PI 1.42 68.75 84.62 0.767 0.694~0.830 S/D 2.92 62.50 86.15 0.735 0.660~0.802 联合 — 84.38 83.08 0.861 0.797~0.910 RI: 阻力指数; PI: 搏动指数; S/D: 收缩与舒张末期最大血流速度比值。 表 4 阴道超声血流参数、血清AMH水平单项及联合对PCOS不孕症IVF-ET妊娠失败的预测价值
指标 cut-off值 灵敏度/% 特异度/% AUC 95%CI 超声血流参数 — 84.38 83.08 0.861 0.797~0.910 抗苗勒管激素 3.78 ng/mL 73.96 86.15 0.808 0.738~0.865 联合 — 95.83 80.00 0.933 0.883~0.966 -
[1] SIDDIQUI S, MATEEN S, AHMAD R, et al. A brief insight into the etiology, genetics, and immunology of polycystic ovarian syndrome (PCOS)[J]. J Assist Reprod Genet, 2022, 39(11): 2439-2473. doi: 10.1007/s10815-022-02625-7
[2] COLLÉE J, MAWET M, TEBACHE L, et al. Polycystic ovarian syndrome and infertility: overview and insights of the putative treatments[J]. Gynecol Endocrinol, 2021, 37(10): 869-874. doi: 10.1080/09513590.2021.1958310
[3] FARLAND L V, STERN J E, LIU C L, et al. Polycystic ovary syndrome and risk of adverse pregnancy outcomes: a registry linkage study from Massachusetts[J]. Hum Reprod, 2022, 37(11): 2690-2699. doi: 10.1093/humrep/deac210
[4] SANTOS ROCA A J, MEJÍAS RAMOS J L, LYNCH L, et al. Prenatal diagnosis of Vasa previa by routine transvaginal color Doppler[J]. P R Health Sci J, 2021, 40(2): 90-92.
[5] 王英华, 鲁海鸥, 李芷舒, 等. 胚胎移植日经阴道三维超声评估子宫内膜容受性对体外受精/卵泡质内单精子显微注射-胚胎移植患者妊娠结局预测价值研究[J]. 临床军医杂志, 2020, 48(2): 191-192. https://www.cnki.com.cn/Article/CJFDTOTAL-JYGZ202002023.htm [6] MOOLHUIJSEN L M E, VISSER J A. Anti-müllerian hormone and ovarian reserve: update on assessing ovarian function[J]. J Clin Endocrinol Metab, 2020, 105(11): 3361-3373. doi: 10.1210/clinem/dgaa513
[7] TEEDE H J, MISSO M L, COSTELLO M F, et al. Recommendations from the international evidence-based guideline for the assessment and management of polycystic ovary syndrome[J]. Hum Reprod, 2018, 33(9): 1602-1618. doi: 10.1093/humrep/dey256
[8] 栗凤霞, 王艳硕, 史艳想, 等. 维生素E联合二甲双胍治疗对多囊卵巢综合征不孕症患者的影响[J]. 实用临床医药杂志, 2022, 26(14): 97-100, 104. doi: 10.7619/jcmp.20220640 [9] 周晓燕, 汤美玲, 马娟, 等. 多囊卵巢综合征患者体外受精-胚胎移植妊娠结局的影响因素及预测[J]. 中国妇产科临床杂志, 2020, 21(4): 370-373. https://www.cnki.com.cn/Article/CJFDTOTAL-FKLC202004009.htm [10] SHI L Y, HUANG L J, LIU L, et al. Diagnostic value of transvaginal three-dimensional ultrasound combined with color Doppler ultrasound for early cesarean scar pregnancy[J]. Ann Palliat Med, 2021, 10(10): 10486-10494. doi: 10.21037/apm-21-2208
[11] 张敏, 阮加里, Frempong, 等. 孕早期子宫动脉血流动力学参数对反复妊娠丢失患者妊娠结局的预测价值[J]. 中华生殖与避孕杂志, 2021, 41(7): 624-630. [12] 陶沙, 吕莎, 曾贞. 经阴道超声检测参数对PCOS不孕症患者子宫内膜容受性的评估研究[J]. 中国性科学, 2020, 29(8): 75-78. https://www.cnki.com.cn/Article/CJFDTOTAL-XKXZ202008025.htm [13] 刘耘利, 许伟标, 刘琼珠, 等. 经阴道三维超声对体外受精-胚胎移植患者子宫内膜容受性的评估及对妊娠结局的预测价值[J]. 中国临床医学影像杂志, 2021, 32(6): 426-431. https://www.cnki.com.cn/Article/CJFDTOTAL-LYYX202106014.htm [14] BEDENK J, VRTAĈNIK-BOKAL E, VIRANT-KLUN I. The role of anti-Müllerian hormone (AMH) in ovarian disease and infertility[J]. J Assist Reprod Genet, 2020, 37(1): 89-100.
[15] BUTLER W J, PICO A, HAWKINS K C, et al. Discordance between day-3 follicle stimulating hormone & anti-Müllerian hormone is predictive of clinical pregnancy during fertility treatment[J]. Gynecol Endocrinol, 2021, 37(9): 798-801. doi: 10.1080/09513590.2020.1862788
[16] 派尔旦木·那斯尔, 努尔比亚·阿布拉. 血清抗苗勒管激素及性激素水平对多囊卵巢综合征不孕患者促排卵治疗后排卵结局的影响[J]. 中国性科学, 2022, 31(8): 33-37. https://www.cnki.com.cn/Article/CJFDTOTAL-XKXZ202208010.htm [17] 曹阳阳, 常旺燕. 年龄、LH/FSH、AMH对体外受精-胚胎移植临床结局的预测价值[J]. 医学临床研究, 2022, 39(1): 63-66. [18] 邓小艳, 刘莉, 李金丽, 等. Glycodelin-A与IVF-ET的子宫内膜容受性及妊娠结局的关系[J]. 中国妇产科临床杂志, 2021, 22(1): 33-35. https://www.cnki.com.cn/Article/CJFDTOTAL-FKLC202101012.htm -
期刊类型引用(2)
1. 王晗,孙晓娜,王丽元. 多囊卵巢综合征不孕患者血清CMKLR1 P15INK4b与炎症 氧化应激 胰岛素抵抗的关系. 安徽医学. 2024(09): 1124-1128 .  百度学术
百度学术
2. 陈丹,包杰,曹丽幸. 血清AMH联合性激素检验在多囊卵巢综合征致不孕症辅助诊断中的应用. 临床医学. 2024(10): 79-81 .  百度学术
百度学术
其他类型引用(0)




 下载:
下载:
 苏公网安备 32100302010246号
苏公网安备 32100302010246号
