Causal relationship between serum uric acid level and cerebrovascular disease: a two-sample bidirectional Mendelian randomization study
-
摘要:目的
采用两样本双向孟德尔随机化(MR)研究评估血清尿酸(SUA)水平与脑血管病(CVD)的因果关联。
方法从全基因组关联研究(GWAS)中获取两样本的单核苷酸多态性(SNPs)作为工具变量。以逆方差加权法(IVW)为主要方法, 以加权中位数法、加权模式方法和MR-Egger回归作为补充,进行敏感性分析以验证结果的稳健性。
结果正向IVW分析结果显示, SUA升高是中风(OR=1.183, 95% CI: 1.081~1.295, P=2.51×10-4)、缺血性卒中(OR=1.196, 95% CI: 1.084~1.320, P=3.81×10-4)、大动脉粥样硬化性卒中(OR=1.466, 95% CI: 1.134~1.897, P=0.004)的危险因素, 是血管性痴呆(OR=0.451, 95% CI: 0.273~0.745, P=0.002)、多发梗死性痴呆(OR=0.372, 95% CI: 0.144~0.959, P=0.041)的保护因素。反向IVW分析结果则不支持基因预测的CVD风险对SUA水平存在因果影响。所有显著性结果均经Bonferroni校正P < 0.005。敏感性分析进一步证实了本研究结果的可靠性。
结论MR分析显示, SUA水平升高与中风、缺血性卒中、大动脉粥样硬化性卒中的发病风险呈正相关,与血管性痴呆、多发梗死性痴呆的发病风险呈负相关。
Abstract:ObjectiveTo evaluate the causal relationship between serum uric acid (SUA) level and cerebrovascular disease (CVD) by a two-sample bidirectional Mendelian randomization (MR) study.
MethodsSingle nucleotide polymorphisms (SNPs) from Genome-Wide Association Studies (GWAS) were obtained as instrumental variables for both samples. Inverse-variance weighted (IVW) method was primarily adopted, with weighted median method, weighted mode method, and MR-Egger regression serving as supplementary approaches for sensitivity analyses to verify the robustness of the results.
ResultsThe forward IVW analysis results showed that increased SUA was a risk factor for stroke (OR=1.183, 95% CI, 1.081 to 1.295, P=2.51×10-4), ischemic stroke (OR=1.196, 95% CI, 1.084 to 1.320, P=3.81×10-4), and large artery atherosclerotic stroke (OR=1.466, 95% CI, 1.134 to 1.897, P=0.004), and also a protective factor for vascular dementia (OR=0.451, 95% CI, 0.273 to 0.745, P=0.002) and multi-infarct dementia (OR=0.372, 95% CI, 0.144 to 0.959, P=0.041). The reverse IVW analysis results did not support a causal effect of genetically predicted CVD risk on SUA level. All significant results were corrected by Bonferroni with P value less than 0.005. Sensitivity analyses further confirmed the reliability of the study findings.
ConclusionThe MR analysis reveals positive correlations between increased SUA level and the risk of stroke, ischemic stroke and large artery atherosclerotic stroke, and negative correlations of SUA level with the risk of vascular dementia and multi-infarct dementia.
-
脑血管病(CVD)是由多种脑血液循环障碍引起的脑部疾病的总称,具有高发病率、高病死率等特点[1]。全球疾病负担工作组(GBDWG)报告[2]显示,中国居民终生罹患CVD的风险高达39.3%, 远高于全球平均水平(24.9%)。尿酸(UA)是嘌呤代谢的终产物,具有抗氧化和清除氧自由基的作用[3]。研究[4]发现,血清尿酸(SUA)水平升高与CVD的发病率及病死率有关。荟萃分析[5-6]表明, SUA水平升高与中风、缺血性卒中(IS)发病风险增加有关; 但也有研究[7]提出高SUA水平可能对IS具有保护作用。目前, SUA在认知功能障碍方面的病理生理作用和临床意义仍存在争议[8]。一项长期队列研究[9]提出SUA水平升高可能显著增加罹患血管性痴呆(VaD)的风险; 但也有研究[10]发现SUA与VaD风险无相关性。
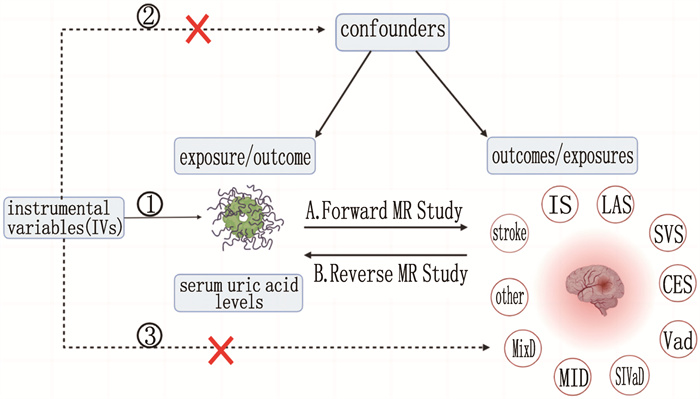
孟德尔随机化(MR)分析通过使用与暴露因素强相关性的单核苷酸多态性(SNPs)作为工具变量(IVs), 来推断暴露与结局的因果关系[11-12]。MR分析的优势在于能克服传统研究中混杂因素和反向因果关系的影响,从而得到更为可靠的结论[13-14]。本研究基于全基因组关联研究(GWAS)的汇总数据,应用MR分析探讨SUA与多种CVD的关联性[15], 包括中风, IS及其亚型如大动脉粥样硬化性卒中(LAS)、小血管性卒中(SVS)、心源性栓塞性卒中(CES), 以及VaD及其亚型如皮质下血管性痴呆(SIVaD)、多发梗死性痴呆(MID)、混合性痴呆(MixD)和其他原因性痴呆,以揭示SUA与这些疾病的双向因果关系,为CVD的预防和治疗提供新的科学依据。
1. 材料与方法
1.1 研究设计
本研究遵循孟德尔随机化研究报告规范(STROBE-MR)[14], 为了评估SUA与CVD的双向因果关系,分别进行了20次两样本MR分析。研究设计严格遵循MR研究的3个主要假设[16-18]: ①关联性假设,作为IVs的SNPs必须与暴露因素显著相关; ②独立性假设, IVs和混杂因素之间不存在相关性; ③排他性假设, IVs只能通过暴露与结局相关。本研究使用的数据均可公开获取,无需伦理批准和知情同意。研究设计见图 1。
1.2 数据来源
本研究暴露和结局GWAS数据均来自于GWAS数据库(https://gwas.mrcieu.ac.uk/), 在该数据库检索框中分别输入“serum uric acid levels”“stroke”“ischemic stroke”“vascular dementia”等术语。所有研究对象均限定为欧洲血统,以尽量减少与种族因素相关的偏差。最终确定暴露因素SUA的GWAS数据由SAKAUE S等[19](PMID: 34594039)发表。结局中风、IS及其亚型相关的GWAS数据由MALIK R等[20](PMID: 29531354)发表。VaD及其亚型的GWAS数据来自FinnGen。见表 1。
表 1 本研究使用GWAS数据集的详细信息表型 数据来源 研究人群 样本量/例 单核苷酸多态性/个 PMID 血清尿酸水平 SAKAUE S等 欧洲人群 343 836 19 041 286 34594039 中风 MALIK R等 欧洲人群 446 696 8 211 693 29531354 缺血性卒中 MALIK R等 欧洲人群 440 328 8 296 492 29531354 大动脉粥样硬化性卒中 MALIK R等 欧洲人群 410 484 8 418 349 29531354 小血管性卒中 MALIK R等 欧洲人群 198 048 8 280 845 29531354 心源性栓塞性卒中 MALIK R等 欧洲人群 413 304 7 954 834 29531354 血管性痴呆 FinnGen 欧洲人群 212 389 16 380 457 — 皮质下血管性痴呆 FinnGen 欧洲人群 211 554 16 380 455 — 多发梗死性痴呆 FinnGen 欧洲人群 211 494 16 380 454 — 混合性痴呆 FinnGen 欧洲人群 211 398 16 380 453 — 其他原因性痴呆 FinnGen 欧洲人群 211 687 16 380 454 — 1.3 工具变量筛选
根据STROBE-MR[17], 本研究的SNPs采取以下步骤进行筛选: ①以P<5×10-8为阈值筛选出与暴露强相关的SNPs作为IVs。②设置连锁不平衡系数r2=0.001、区域宽度为10 000 kb以确保所选的SNPs位点相互独立[21]。③提取与结局相关的SNPs, 整合暴露和结局数据集,并删除回文序列。④通过PhenoScanner数据库(http://www.phenoscanner.medschl.cam.ac.uk/)排除混杂因素。⑤计算每个IVs的R2和F统计量。剔除F值< 10的弱IVs, 确保所选IVs的有效性[22]。⑥采用MR-PRESSO识别异常值和校正水平多效性。反向MR分析,从不同CVD的GWAS数据中筛选出独立的SNPs作为IVs(P < 5×10-6), 其他筛选标准与正向MR分析一致。
1.4 统计学分析
本研究主要采用逆方差加权法(IVW), 以加权中位数法(weighted median)、加权模式方法(weighted mode)和MR-Egger回归法作为补充,评估SUA与CVD的因果关联[23], 以森林图呈现分析结果。采用Cochran′s Q检验判断SNPs间的异质性[24-25]。为了识别和减少潜在的水平多效性引起的偏差,本研究采用MR-PRESSO[26]和MR-Egger[27]截距法进行检测。通过“留一法”敏感性分析,依次剔除单个SNP, 以评估其是否对整体结果有影响。通过观察散点图和漏斗图的对称性来检查结果是否稳定。所有分析均在R软件(4.3.2版)中进行,使用“TwoSampleMR(0.5.9版)”和“MR-PRESSO(1.0版)”[28]这2个R包。统计学显著性通过Bonferroni校正后确定, P < 0.005被认为具有显著性, P≥0.005~0.05表示潜在的因果关联, P>0.05为差异无统计学意义。
2. 结果
2.1 SUA水平与不同CVD因果关联的正向MR分析结果
2.1.1 IVs的选择结果
根据上述IVs的筛选标准及步骤,本研究选择了不同数量的SNPs作为评估SUA水平与不同CVD因果关联的IVs, 筛选出163、164、169、168、170、165、171、179、180和181个SNPs分别作为中风、IS、LAS、SVS、CES、VaD、SIVaD、MID、MixD和其他原因性痴呆的IVs。
2.1.2 SUA水平与中风、IS及其亚型之间的因果关联
IVW分析结果显示,基因预测的SUA水平与中风(OR=1.183, 95% CI: 1.081~1.295, P=2.51×10-4)、IS(OR=1.196, 95% CI: 1.084~1.320, P=3.81×10-4)和LAS(OR=1.466, 95% CI: 1.134~1.897, P=0.004)的发病风险呈正相关。上述结果经Bonferroni校正P < 0.005后,差异仍有统计学意义。基因预测的SUA水平与SVS(OR=1.159, 95% CI: 0.917~1.467, P=0.218)、CES (OR=0.878, 95% CI: 0.743~1.037, P=0.126)之间不存在因果关联。
2.1.3 SUA水平与VaD及其亚型之间的因果关联
IVW分析结果显示,基因预测的SUA水平与VaD(OR=0.451, 95% CI: 0.273~0.745, P=0.002)和MID(OR=0.372, 95% CI: 0.144~0.959, P=0.041)的发病风险呈负相关。上述结果经Bonferroni校正P < 0.005后,提示SUA与MID存在潜在的因果关联。基因预测的SUA水平与SIVaD(OR=0.859, 95% CI: 0.371~1.986, P=0.722)、MixD(OR=1.693, 95% CI: 0.444~6.462, P=0.441)和其他原因性痴呆(OR=1.104, 95% CI: 0.545~2.237, P=0.784)之间不存在因果关联。
2.1.4 敏感性分析
Cochran′s Q检验结果显示,上述结果均不存在异质性(P中风=0.845, PIS=0.965, PLAS=0.189, PSVS=0.984, PCES=0.957, PVaD=0.855, PSIVaD=0.930, PMID=0.538, PMixD=0.999,P其他原因性痴呆=0.194)。MR-Egger截距检测结果也显示均不存在水平多效性(P中风=0.360, PIS=0.354, PLAS=0.786, PSVS=0.858, PCES=0.331, PVaD=0.772, PSIVaD=0.659, PMID=0.421, PMixD=0.775, P其他原因性痴呆=0.279)。此外, MR-PRESSO分析在SUA水平与LAS风险的因果关联中识别出4个异常SNPs(rs146787580、rs7696556、rs34868798、rs9807214), 在对这些SNPs进行校正后, SUA水平对LAS风险的因果效应依然显著,其余均未检测出异常SNPs。留一法分析表明消除任何一个SNP均不会对整体结果有影响。最后, SUA水平对不同CVD风险预测的散点图和漏斗图显示了因果效应的分布是对称的,这进一步验证了结果的稳定性和可靠性。SUA水平与不同CVD因果关联的正向MR分析结果见图 2。
2.2 SUA水平与不同CVD因果关联的反向MR分析结果
2.2.1 IVs的选择结果
本研究选择了不同数量的SNPs作为评估不同CVD与SUA水平因果关联的IVs, 筛选出中风(35个)、IS(34个)、LAS(25个)、SVS(23个)、CES(18个)、VaD(6个)、SIVaD(12个)、MID(7个)、MixD(3个)、其他原因性痴呆(4个)分别作为SUA的IVs。
2.2.2 不同CVD与SUA水平之间的因果关联
IVW分析结果显示,基因预测的中风(OR=1.007, 95% CI: 0.994~1.021, P=0.262)、IS(OR=1.004, 95% CI: 0.991~1.016, P=0.572)、LAS(OR=1.005, 95% CI: 0.999~1.010, P=0.086)、SVS(OR=0.995, 95% CI: 0.988~1.001, P=0.101)、CES(OR=1.011, 95% CI: 1.000~1.023, P=0.058)、VaD(OR=1.002, 95% CI: 0.999~1.005, P=0.278)、SIVaD(OR=1.001, 95% CI: 0.999~1.003, P=0.273)、MID(OR=1.003, 95% CI: 0.999~1.006, P=0.103)、MixD(OR=1.003, 95% CI: 0.999~1.008, P=0.157)、其他原因性痴呆(OR=1.004, 95% CI: 0.999~1.010, P=0.135)与SUA水平之间均不存在因果关联。
2.2.3 敏感性分析
Cochran′s Q检验结果显示均不存在异质性(P中风=0.384, PIS=0.265, PLAS=0.611, PSVS=0.971, PCES=0.087, PVaD=0.727, PSIVaD=0.329, PMID=0.299, PMixD=0.165, P其他原因性痴呆=0.240)。MR-Egger截距检测结果也显示均不存在水平多效性(P中风=0.813, PIS=0.661, PLAS=0.224, PSVS=0.439, PCES=0.919, PVaD=0.218, PSIVaD=0.060, PMID=0.654, PMixD=0.363, P其他原因性痴呆=0.220)。此外, MR-PRESSO对异常值进行检测,在中风与SUA的因果关联中识别出2个异常SNPs(rs147076266、rs10774624), 在IS与SUA的因果关联中识别出2个异常SNPs(rs7099238、rs60102266), 在LAS与SUA的因果关联中识别出1个异常SNP(rs142532801), 在SVS与SUA的因果关联中识别出1个异常SNP(rs75501811), 在CES与SUA的因果关联中识别出1个异常SNP(rs13143308), 但对异常值进行校正后,所有因果效应依然显著,其余均未检测出异常SNPs。留一法分析结果表明MR分析结果稳健。最后,不同CVD风险对SUA水平预测的散点图和漏斗图显示了因果效应的分布是对称的,提示了结果的可靠性。SUA水平与不同CVD因果关联的反向MR分析结果见图 3。
3. 讨论
本研究通过双样本双向MR分析,深入探讨了SUA水平与不同CVD之间的因果关联。正向MR分析结果显示, SUA水平升高会增加中风、IS和LAS的发病风险,但也会降低VaD、MID的发病风险。然而, MR分析并未发现SUA与SVS、CES、SIVaD、MixD和其他原因性痴呆之间存在因果关系。此外,反向MR分析结果并不支持基因预测的CVD风险对SUA水平存在因果影响。这些发现为了解SUA在CVD中的作用提供了新的视角,有助于开发针对性的预防和治疗措施,以降低特定患者群体的疾病风险。
既往大量观察性研究分析了SUA与CVD的相关性。LI M等[29]进行了一项回顾性分析发现,高SUA水平与中风发病风险增加相关(RR=1.22, 95% CI: 1.02~1.46), 即使在调整了年龄、高血压、糖尿病和胆固醇等已知风险因素后,该相关性依然显著。WANG C Q等[30]通过中介MR研究也发现, SUA水平升高与中风、IS、LAS风险增加呈正相关。本研究使用不同来源的GWAS数据进行MR分析,得出了类似的结论,即SUA每增加1个单位,中风、IS、LAS的发病风险分别增加18.3%、19.6%、46.6%。考虑到本研究MR分析提取了更多符合条件的IVs,并且仅使用了来自欧洲血统的GWAS汇总数据,这使得本研究结果更加准确。
作为一个严重的公共健康问题, VaD的发病率呈上升趋势[31]。多个观察性研究探讨了SUA水平与VaD风险之间的相关性。一项基于人群的队列研究[32]发现,SUA水平升高与VaD风险降低有关,并指出其具有神经保护作用。XU Y Z等[33]研究也指出,较低的SUA水平与认知功能下降有关。然而,一项前瞻性队列研究[34]显示,当人体SUA水平升高>400 μmol/L时, VaD的风险可能会增加50%(HR=1.50, 95% CI: 1.28~1.77)。本研究结果与部分既往研究结果并不完全一致,其原因可能为: ①既往研究主要是观察性研究,结果可能受到混杂因素和反向因果关系的影响。②部分研究可能因样本量不足而限制了结论的普遍性和准确性。
SUA对CVD的作用机制可能涉及多种生物化学过程和炎症反应。有研究[35]提出SUA可能通过抑制一氧化氮(NO)合酶的活性,间接促进高血脂和高血压的发展,这可能导致动脉壁上脂质的积累而形成动脉粥样硬化斑块,从而加剧CVD的发生。有研究[36]指出在由低密度脂蛋白(LDL)引发的炎症反应中,SUA可能作为助氧化剂,降低NO水平,导致血管损伤。此外, SUA还可能通过增强炎症因子的活性,加剧血管内皮的炎症反应,促进血管内皮损伤,增加动脉粥样硬化的风险,这也是CVD的一个主要病因[37-38]。上述研究表明,SUA可能通过激活炎症途径和促进氧化应激参与机体的炎症损伤过程,破坏血管内皮细胞,促进动脉粥样硬化的发展。同时,炎症因子可通过影响黄嘌呤氧化酶的活性,不仅增加UA的生成,还可能导致细胞损伤或凋亡[39],形成UA与炎症之间的恶性循环,从而可能增加CVD的风险。临床上对于SUA水平较高的患者,应积极采取预防措施以降低CVD的发病风险。
本研究的反向MR分析结果未发现CVD风险与SUA水平之间存在因果关联,这一发现与部分观察性研究结果不同。既往研究[40]指出,随着IS发作后时间的推移,SUA水平呈上升趋势,且与患者长期不良预后相关。然而,也有研究[41]显示在脑血管事件发生后SUA的水平显著下降,这意味着SUA可能参与了疾病的进展过程。UA具有抗氧化性质,在大脑缺血、缺氧的情况下,脑内脂质过氧化物增加以及组织抗氧化水平降低都是氧化应激增加的间接证据。
本研究的优势: ①利用遗传学方法证明SUA水平与CVD风险之间的双向因果关联,有效避免了传统观察性研究中的混杂因素和反向因果关系的影响。②通过使用大规模GWAS的汇总数据并结合敏感性分析,进一步证实了本研究结果的可靠性。本研究的局限性: ①研究依赖于GWAS的汇总数据,缺乏个体层面的数据,这限制了进行年龄、性别等特定亚组分析的能力,以及评估不同亚组间因果效应差异的可能性。②所使用的GWAS数据主要来源于欧洲人群,因此研究结果在其他种族或人群的普适性需要进一步验证。
综上所述,本研究MR分析表明SUA水平升高与中风、IS、LAS发病风险呈正相关,与VaD、MID发病风险呈负相关,为临床上采取严格控制SUA水平的干预措施来降低CVD的发病风险提供科学依据。未来可通过扩大样本量范围,涵盖多样化人群,以探讨特定的亚组或不同人群中可能存在的因果关联,进一步开发更为精准的预防和治疗策略。
-
表 1 本研究使用GWAS数据集的详细信息
表型 数据来源 研究人群 样本量/例 单核苷酸多态性/个 PMID 血清尿酸水平 SAKAUE S等 欧洲人群 343 836 19 041 286 34594039 中风 MALIK R等 欧洲人群 446 696 8 211 693 29531354 缺血性卒中 MALIK R等 欧洲人群 440 328 8 296 492 29531354 大动脉粥样硬化性卒中 MALIK R等 欧洲人群 410 484 8 418 349 29531354 小血管性卒中 MALIK R等 欧洲人群 198 048 8 280 845 29531354 心源性栓塞性卒中 MALIK R等 欧洲人群 413 304 7 954 834 29531354 血管性痴呆 FinnGen 欧洲人群 212 389 16 380 457 — 皮质下血管性痴呆 FinnGen 欧洲人群 211 554 16 380 455 — 多发梗死性痴呆 FinnGen 欧洲人群 211 494 16 380 454 — 混合性痴呆 FinnGen 欧洲人群 211 398 16 380 453 — 其他原因性痴呆 FinnGen 欧洲人群 211 687 16 380 454 — -
[1] GOLDSTEIN L B. Introduction for focused updates in cerebrovascular disease[J]. Stroke, 2020, 51(3): 708-710. doi: 10.1161/STROKEAHA.119.024159
[2] GBD Lifetime Risk of Stroke Collaborators, FEIGIN V L, NGUYEN G, et al. Global, regional, and country-specific lifetime risks of stroke, 1990 and 2016[J]. N Engl J Med, 2018, 379(25): 2429-2437. doi: 10.1056/NEJMoa1804492
[3] WANG Q W, WEN X, KONG J M. Recent progress on uric acid detection: a review[J]. Crit Rev Anal Chem, 2020, 50(4): 359-375. doi: 10.1080/10408347.2019.1637711
[4] CORTESE F, SCICCHITANO P, CORTESE A M, et al. Uric acid in metabolic and cerebrovascular disorders: a review[J]. Curr Vasc Pharmacol, 2020, 18(6): 610-618. doi: 10.2174/1570161118666191217123930
[5] DU L, MA J H, ZHANG X N. Higher serum uric acid may contribute to cerebral infarction in patients with type 2 diabetes mellitus: a meta-analysis[J]. J Mol Neurosci, 2017, 61(1): 25-31. doi: 10.1007/s12031-016-0848-y
[6] ZHONG C K, ZHONG X Y, XU T, et al. Sex-specific relationship between serum uric acid and risk of stroke: a dose-response meta-analysis of prospective studies[J]. J Am Heart Assoc, 2017, 6(4): e005042. doi: 10.1161/JAHA.116.005042
[7] ZHANG P, WANG R, QU Y, et al. Serum uric acid levels and outcome of acute ischemic stroke: a dose-response meta-analysis[J]. Mol Neurobiol, 2024, 61(3): 1704-1713. doi: 10.1007/s12035-023-03634-y
[8] TANA C, TICINESI A, PRATI B, et al. Uric acid and cognitive function in older individuals[J]. Nutrients, 2018, 10(8): 975. doi: 10.3390/nu10080975
[9] LATOURTE A, SOUMARÉ A, BARDIN T, et al. Uric acid and incident dementia over 12 years of follow-up: a population-based cohort study[J]. Ann Rheum Dis, 2018, 77(3): 328-335. doi: 10.1136/annrheumdis-2016-210767
[10] LI Q, CEN K W, CUI Y, et al. Uric acid levels and their association with vascular dementia and Parkinson's disease dementia: a meta-analysis[J]. Neurol Sci, 2023, 44(6): 2017-2024. doi: 10.1007/s10072-023-06620-3
[11] NAZARZADEH M, PINHO-GOMES A C, BIDEL Z, et al. Plasma lipids and risk of aortic valve stenosis: a Mendelian randomization study[J]. Eur Heart J, 2020, 41(40): 3913-3920. doi: 10.1093/eurheartj/ehaa070
[12] LAWLOR D A, HARBORD R M, STERNE J A C, et al. Mendelian randomization: using genes as instruments for making causal inferences in epidemiology[J]. Stat Med, 2008, 27(8): 1133-1163. doi: 10.1002/sim.3034
[13] CLAYTON G L, GONÇALVES A, SOARES, et al. A framework for assessing selection and misclassification bias in Mendelian randomisation studies: an illustrative example between body mass index and covid-19[J]. BMJ, 2023, 381: e072148. http://www.semanticscholar.org/paper/0f8c69006e263a539eaca48de55c0325fc24e210
[14] SKRIVANKOVA V W, RICHMOND R C, WOOLF B A R, et al. Strengthening the reporting of observational studies in epidemiology using Mendelian randomisation (STROBE-MR): explanation and elaboration[J]. BMJ, 2021, 375: n2233. http://www.xueshufan.com/publication/3210406414
[15] LU N, DUBREUIL M, ZHANG Y Q, et al. Gout and the risk of Alzheimer's disease: a population-based, BMI-matched cohort study[J]. Ann Rheum Dis, 2016, 75(3): 547-551. doi: 10.1136/annrheumdis-2014-206917
[16] SEKULA P, FABIOLA GRECO M, PATTARO C, et al. Mendelian randomization as an approach to assess causality using observational data[J]. J Am Soc Nephrol, 2016, 27(11): 3253-3265. doi: 10.1681/ASN.2016010098
[17] SKRIVANKOVA V W, RICHMOND R C, WOOLF B A R, et al. Strengthening the reporting of observational studies in epidemiology using Mendelian randomization: the STROBE-MR statement[J]. JAMA, 2021, 326(16): 1614-1621. doi: 10.1001/jama.2021.18236
[18] 刘波, 游俊杰, 郑思琳, 等. 基于孟德尔随机化分析胃食管反流病与慢性阻塞性肺疾病的因果关系研究[J]. 实用临床医药杂志, 2024, 28(1): 113-117. [19] SAKAUE S, KANAI M, TANIGAWA Y, et al. A cross-population atlas of genetic associations for 220 human phenotypes[J]. Nat Genet, 2021, 53(10): 1415-1424. doi: 10.1038/s41588-021-00931-x
[20] MALIK R, CHAUHAN G, TRAYLOR M, et al. Multiancestry genome-wide association study of 520, 000 subjects identifies 32 loci associated with stroke and stroke subtypes[J]. Nat Genet, 2018, 50(4): 524-537. doi: 10.1038/s41588-018-0058-3
[21] 张卫娜, 郑丽, 刘德平. 尿酸与心房颤动、冠心病和充血性心力衰竭因果关联的两样本孟德尔随机化研究[J]. 中国心血管杂志, 2023, 28(5): 423-429. doi: 10.3969/j.issn.1007-5410.2023.05.004 [22] BURGESS S, THOMPSON S G, CRP CHD GENETICS COLLABORATION. Avoiding bias from weak instruments in Mendelian randomization studies[J]. Int J Epidemiol, 2011, 40(3): 755-764. doi: 10.1093/ije/dyr036
[23] 李威, 柴金莲, 贾海峰, 等. 微量营养素与骨坏死的因果关系: 来自双向孟德尔随机试验的证据[J]. 中国组织工程研究, 2024, 33(33): 5308-5314. doi: 10.12307/2024.686 [24] HEMANI G, TILLING K, DAVEY SMITH G. Orienting the causal relationship between imprecisely measured traits using GWAS summary data[J]. PLoS Genet, 2017, 13(11): e1007081. doi: 10.1371/journal.pgen.1007081
[25] SUI X H, LIU T T, LIANG Y, et al. Psychiatric disorders and cardiovascular diseases: a Mendelian randomization study[J]. Heliyon, 2023, 9(10): e20754. doi: 10.1016/j.heliyon.2023.e20754
[26] VERBANCK M, CHEN C Y, NEALE B, et al. Detection of widespread horizontal pleiotropy in causal relationships inferred from Mendelian randomization between complex traits and diseases[J]. Nat Genet, 2018, 50(5): 693-698. doi: 10.1038/s41588-018-0099-7
[27] BOWDEN J, DAVEY SMITH G, BURGESS S. Mendelian randomization with invalid instruments: effect estimation and bias detection through Egger regression[J]. Int J Epidemiol, 2015, 44(2): 512-525. doi: 10.1093/ije/dyv080
[28] HEMANI G, ZHENG J, ELSWORTH B, et al. The MR-Base platform supports systematic causal inference across the human phenome[J]. Elife, 2018, 7: e34408. doi: 10.7554/eLife.34408
[29] LI M, HOU W S, ZHANG X W, et al. Hyperuricemia and risk of stroke: a systematic review and meta-analysis of prospective studies[J]. Atherosclerosis, 2014, 232(2): 265-270. doi: 10.1016/j.atherosclerosis.2013.11.051
[30] WANG C Q, GAO Y K, SMERIN D, et al. Genetically predicted type 2 diabetes mellitus mediates the causal association between plasma uric acid and ischemic stroke[J]. Int Immunopharmacol, 2024, 134: 112267. doi: 10.1016/j.intimp.2024.112267
[31] 黎启娇, 萨仁, 林智鹏, 等. 补髓通窍益脑汤联合靳三针治疗血管性痴呆患者的效果观察[J]. 实用临床医药杂志, 2022, 26(14): 46-49, 54. doi: 10.7619/jcmp.20214795 [32] HONG J Y, LAN T Y, TANG G J, et al. Gout and the risk of dementia: a nationwide population-based cohort study[J]. Arthritis Res Ther, 2015, 17(1): 139. doi: 10.1186/s13075-015-0642-1
[33] XU Y Z, WANG Q, CUI R T, et al. Uric acid is associated with vascular dementia in Chinese population[J]. Brain Behav, 2017, 7(2): e00617. doi: 10.1002/brb3.617
[34] CHEN T S, MI N N, LAO H Y, et al. Investigating the nexus of metabolic syndrome, serum uric acid, and dementia risk: a prospective cohort study[J]. BMC Med, 2024, 22(1): 115. doi: 10.1186/s12916-024-03302-5
[35] SÁNCHEZ-LOZADA L G, TAPIA E, SANTAMARÍA J, et al. Mild hyperuricemia induces vasoconstriction and maintains glomerular hypertension in normal and remnant kidney rats[J]. Kidney Int, 2005, 67(1): 237-247. doi: 10.1111/j.1523-1755.2005.00074.x
[36] SO A, THORENS B. Uric acid transport and disease[J]. J Clin Invest, 2010, 120(6): 1791-1799. doi: 10.1172/JCI42344
[37] CRIŞAN T O, CLEOPHAS M C, OOSTING M, et al. Soluble uric acid primes TLR-induced proinflammatory cytokine production by human primary cells via inhibition of IL-1Ra[J]. Ann Rheum Dis, 2016, 75(4): 755-762. doi: 10.1136/annrheumdis-2014-206564
[38] CRIŞAN T O, CLEOPHAS M C P, NOVAKOVIC B, et al. Uric acid priming in human monocytes is driven by the AKT-PRAS40 autophagy pathway[J]. Proc Natl Acad Sci U S A, 2017, 114(21): 5485-5490. doi: 10.1073/pnas.1620910114
[39] KOMAKI Y, SUGIURA H, KOARAI A, et al. Cytokine-mediated xanthine oxidase upregulation in chronic obstructive pulmonary disease's airways[J]. Pulm Pharmacol Ther, 2005, 18(4): 297-302. doi: 10.1016/j.pupt.2005.01.002
[40] CHERUBINI A, POLIDORI M C, BREGNOCCHI M, et al. Antioxidant profile and early outcome in stroke patients[J]. Stroke, 2000, 31(10): 2295-2300. doi: 10.1161/01.STR.31.10.2295
[41] BROUNS R, WAUTERS A, VAN DE VIJVER G, et al. Decrease in uric acid in acute ischemic stroke correlates with stroke severity, evolution and outcome[J]. Clin Chem Lab Med, 2010, 48(3): 383-390. doi: 10.1515/CCLM.2010.065




 下载:
下载:


 苏公网安备 32100302010246号
苏公网安备 32100302010246号
