Correlations of frailty and nutritional risk with postoperative pulmonary infection in elderly patients with gastric cancer
-
摘要:目的
探讨老年胃癌患者术前衰弱和营养风险与术后肺部感染的相关性。
方法选取2021年8月—2022年9月滨州医学院附属医院胃肠外科行限期手术的老年胃癌患者为研究对象,采用Fried衰弱表型量表和营养风险筛查(NRS2002)评估量表评估患者的衰弱和营养风险状况。观察和记录住院期间术后肺部感染的发生情况,分析衰弱和营养风险对老年胃癌患者术后肺部感染的预测效果。
结果共纳入患者217例,其中存在营养风险者106例(48.85%), 衰弱者72例(33.18%)。在同等营养风险(NRS2002评分≥3分)情况下,衰弱患者术后肺部感染的发生率高于非衰弱患者,差异有统计学意义(P < 0.01)。Logistic回归分析显示,在校正了相关因素后,衰弱是术后肺部感染发生的独立危险因素(OR=3.628, 95%CI: 1.528~8.611)。衰弱联合营养风险预测老年胃癌患者术后肺部感染的受试者工作特征(ROC)曲线的曲线下面积(AUC)为0.834(95%CI: 0.769~0.899), 高于单独应用衰弱、营养风险评估的0.763(95%CI: 0.685~0.841)、0.737(95%CI: 0.656~0.818), 差异有统计学意义(P < 0.01)。
结论当患者同时存在衰弱和营养风险时,术后肺部感染的发生风险最高; 衰弱联合营养风险评估可增强对老年胃癌患者术后肺部感染的预测效能。
Abstract:ObjectiveTo explore the correlations of preoperative frailty and nutritional risk with postoperative pulmonary infection in elderly patients with gastric cancer.
MethodsElderly patients with confine operation for gastric cancer in the Department of Gastrointestinal Surgery in the Affiliated Hospital of Binzhou Medical University from August 2021 to September 2022 were selected as the research objects, and the Fried Frailty Phenotype Scale and the Nutritional Risk Screening (NRS2002) Assessment Scale were used to evaluate the patient′s frailty and nutritional risk status. Occurrence of postoperative pulmonary infection during hospitalization was observed and recorded, and the effects of frailty and nutritional risk in predicting postoperative pulmonary infection in elderly patients with gastric cancer were analyzed.
ResultsA total of 217 patients were recruited, including 106 cases (48.85%) with nutritional risk and 72 cases (33.18%) with frailty. Under the same condition of nutritional risk (NRS2002 score ≥ 3), the incidence of postoperative pulmonary infection in patients with frailty was significantly higher than that in patients without frailty (P < 0.01). Logistic regression analysis showed that frailty was an independent risk factor for postoperative pulmonary infection (OR=3.628; 95%CI, 1.528 to 8.611) after correction of relevant factors. The area under the curve (AUC) of the receiver operating characteristic (ROC) curve for predicting postoperative pulmonary infection in elderly patients with gastric cancer by frailty combined with nutritional risk was 0.834 (95%CI, 0.769 to 0.899), which was significantly higher than 0.763 (95%CI, 0.685 to 0.841) by frailty and 0.737 (95%CI, 0.656 to 0.818) by nutritional risk (P < 0.01).
ConclusionWhen patients have both frailty and nutritional risk, the risk of postoperative pulmonary infection is the highest; frailty combined with nutritional risk assessment can enhance the predictive efficiency of postoperative pulmonary infection in elderly patients with gastric cancer.
-
Keywords:
- frailty /
- nutritional risk /
- elderly people /
- gastric cancer /
- pulmonary infection /
- prediction
-
随着外科手术技术的进步,胃癌根治术的有效性及安全性大大提高,越来越多的老年胃癌患者能够接受手术治疗[1-2]。老年患者生理功能减退,加之手术损伤、应激等因素导致患者机体免疫力降低,术后更易发生肺部感染[3-4]。若能在术前准确识别高危患者并及时给予干预,则对改善老年胃癌患者预后具有重要的意义。研究[5-6]表明,老年胃癌患者常伴有高营养风险。研究[7]显示,老年手术患者衰弱的发生率高,而衰弱和高营养风险均可增加机体的易损性和不良结局的易感性[8]。本研究拟在老年胃癌患者限期手术前评估其衰弱和营养风险状况,探讨衰弱联合营养风险评估对老年胃癌患者术后肺部感染的预测价值,现将结果报告如下。
1. 资料与方法
1.1 一般资料
选取2021年8月—2022年9月滨州医学院附属医院胃肠外科行限期手术的老年胃癌患者217例。纳入标准: ①年龄≥60岁者; ②有病理学诊断依据且确诊为胃癌者; ③自愿签署知情同意书参加本研究者。排除标准: ①晚期胃癌者(腹腔广泛转移、远处器官转移); ②存在认知功能障碍者; ③合并严重心、肝、肾功能障碍而不能配合评估的患者; ④伴有甲状腺功能低下、帕金森病及脑卒中患者,或因服用药物产生衰弱症状者。本研究已获得医院伦理委员会审核批准(KYLL-2022-98)。
1.2 研究方法
1.2.1 一般资料及临床特征:
通过临床信息管理系统(Cis)收集患者的一般资料及临床特征,包括性别、年龄、经济收入、吸烟史、体质量指数(BMI)、有无基础疾病(高血压、糖尿病、冠心病、脑血管疾病)、日常生活活动能力(ADL)评定量表、合并疾病种类、术前白蛋白及球蛋白和血红蛋白水平、术前心功能、手术类型、美国麻醉医师协会(ASA)分级、肿瘤TNM分期等。
1.2.2 衰弱评估:
在患者入院24 h内采用Fried衰弱表型量表[9]对纳入的胃癌患者进行衰弱评估。①不明原因的体质量下降。过去1年内非有意的体质量减轻≥4.54 kg或体质量下降≥5%。②活动减少。采用明达休闲时间活动问卷(MLTA)收集患者过去1周的活动量,男性 < 383 kcal/周(约散步2.5 h/周)、女性 < 270 kcal/周(约散步2 h/周)为体力活动减少。③自述疲乏。采用流调用抑郁自评量表(CES-D)中“我感到做什么事都很吃力”“我提不起劲来做事”这2个条目,根据过去1周内出现的频次进行评定。④握力下降。采用握力器测量3次患者双手的握力,取平均值,结合性别和BMI进行判断。⑤行走速度慢。根据患者的身高以平时速度行走4.57 m所用时间进行判定。取值区间为0~5分,每项异常为1分, 0分为正常, 1~2分为衰弱前期, ≥3分为衰弱。本研究将正常及衰弱前期统一为非衰弱患者[10]。
1.2.3 营养风险评估:
在患者入院24 h内采用营养风险筛查(NRS 2002)评估工具[11]对纳入的胃癌患者进行营养风险评估。①营养状况评分(0~3分); ②疾病状态评分(0~3分); ③患者年龄≥70岁,总分再加1分。取值区间为0~7分,总评分 < 3分为无营养风险,总评分≥3分为存在营养风险。
1.2.4 结局指标:
在患者术后住院期间追踪观察并记录术后肺部感染发生情况。肺部感染的诊断标准参照卫生部颁发的《医院感染诊断标准(试行)》[12], 指患者术后出现体温≥38.0 ℃并持续24 h以上,伴咳嗽、咳痰、肺部出现湿啰音,胸部影像学检查出现片状影或浸润影。
1.3 统计学方法
采用SPSS 26.0统计软件进行数据分析。计量资料以(x±s)或[M(Q1, Q3)]表示,组间比较采用独立样本t检验; 计数资料以[n(%)]描述,组间比较采用卡方或Fisher精确检验。采用Logistic回归模型分析衰弱和营养风险对术后肺部感染的影响。采用受试者工作特征(ROC)曲线的曲线下面积(AUC)评价衰弱和营养风险对老年胃癌患者术后肺部感染的预测价值,采用Medcalc软件Z检验比较不同评估工具的预测作用, P < 0.05为差异有统计学意义。
2. 结果
2.1 研究对象的一般特征
本研究共纳入217例患者,其中男165例,女52例,年龄(67.33±5.80)岁, BMI为(23.07±3.24) kg/m2; 腹腔镜手术182例,开腹手术35例; NRS 2002评分 < 3分者111例(51.15%), ≥3分者106例(48.85%); 无衰弱者145例(66.82%), 衰弱者72例(33.18%)。根据术后肺部感染发生情况分为感染组42例和非感染组175例, 2组患者一般资料见表 1。
表 1 2组患者一般资料比较(n=217)一般资料 分类 感染组(n=42) 非感染组(n=175) χ2/t P 性别 男 30(71.4) 135(77.1) 0.607 0.436 女 12(28.6) 40(22.9) 年龄/岁 70.6±5.8 66.5±5.5 -4.256 < 0.001 经济收入 < 3 000元人民币 27(64.3) 93(53.1) 4.123 0.127 3 000~5 000元人民币 6(14.3) 52(29.7) >5 000元人民币 9(21.4) 30(17.2) 吸烟 是 17(40.5) 65(37.1) 0.160 0.689 否 25(59.5) 110(62.9) 心功能分级 Ⅰ级 16(38.1) 61(34.9) 0.264 0.876 Ⅱ级 25(59.5) 111(63.4) Ⅲ级 1(2.4) 3(1.7) 手术类型 开腹手术 9(21.4) 26(14.9) 1.081 0.298 腹腔镜手术 33(78.6) 149(85.1) ASA分级 Ⅰ~Ⅱ级 25(59.5) 134(76.5) 5.915 0.116 Ⅲ~Ⅳ级 17(40.5) 41(23.5) 高血压 是 16(38.1) 64(36.6) 0.034 0.854 否 26(61.9) 111(63.4) 糖尿病 是 6(14.3) 29(16.6) 0.131 0.718 否 36(85.7) 146(83.4) BMI/(kg/m2) 22.6±3.6 23.2±3.1 1.135 0.258 TNM分期 Ⅰ期 7(16.7) 47(26.9) 3.354 0.340 Ⅱ期 17(40.5) 66(37.7) Ⅲ期 18(42.8) 62(35.4) ADL评分/分 16.4±7.5 14.5±2.4 -1.657 0.004 白蛋白/(g/L) 35.4±4.0 36.7±4.7 1.669 0.097 球蛋白/(g/L) 24.6±5.4 24.5±4.0 -0.114 0.910 血红蛋白/(g/L) 116.6±21.4 122.5±23.5 1.496 0.136 衰弱 衰弱(≥3分) 28(66.7) 44(25.1) 26.342 < 0.001 非衰弱(< 3分) 14(33.3) 131(74.9) 营养风险 营养风险(≥3分) 33(78.6) 73(41.7) 18.415 < 0.001 无营养风险(< 3分) 9(21.4) 102(58.3) ASA: 美国麻醉医师协会; BMI: 体质量指数; ADL: 日常生活活动能力。 2.2 衰弱和营养风险与术后肺部感染的关系
在纳入的217例老年胃癌患者中,有42例发生了肺部感染,在同等营养风险(NRS 2002评分≥3分)情况下,衰弱患者术后肺部感染的发生率高于非衰弱患者,差异有统计学意义(P < 0.01)。见表 2。
表 2 不同营养风险评分及衰弱患者术后肺部感染发生情况比较(n=217)NRS 2002 衰弱状况 例数/例 感染 χ2 P < 3分 衰弱 12 2(16.7) 1.323 0.250 非衰弱 99 7(7.1) ≥3分 衰弱 60 26(43.3) 9.600 0.002 非衰弱 46 7(15.2) 2.3 老年胃癌患者术后肺部感染影响因素的Logistic回归分析
分析衰弱、营养与并发症的关系,以衰弱(非衰弱=0, 衰弱=1)、营养(无营养风险=0, 有营养风险=1)为自变量,以术后并发症(否=0, 是=1)为因变量,进行Logistic回归分析。结果显示,衰弱[OR=3.782, 95%CI: 1.687~8.476, P=0.001]和营养[OR=2.785, 95%CI: 1.142~6.791, P=0.024]均与肺部感染发生风险相关。在校正年龄、手术类型、ADL、白蛋白等混杂因素后,营养对术后肺部感染的影响无统计学意义(P>0.05), 而衰弱仍是老年胃癌术后肺部感染的独立影响因素[OR=3.628, 95%CI: 1.528~8.611, P=0.003]。见表 3。
表 3 老年胃癌患者术后发生肺部感染的Logistic回归分析(n=217)模型类别 回归系数 标准误 Wald P OR 95%CI 模型1衰弱 1.330 0.412 10.433 0.001 3.782 1.687~8.476 NRS 2002 1.024 0.455 5.075 0.024 2.785 1.142~6.791 模型2衰弱 1.289 0.441 8.534 0.003 3.628 1.528~8.611 NRS 2002 0.610 0.509 1.435 0.231 1.840 0.679~4.989 模型2校正了年龄、手术类型、ADL、白蛋白。 2.4 衰弱评估、营养风险评分以及二者联合应用对老年胃癌患者术后肺部感染的预测价值
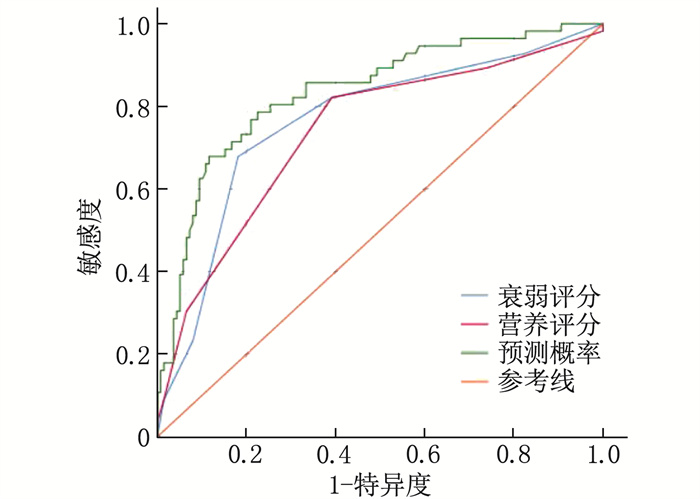
绘制衰弱、营养风险及二者联合预测老年胃癌患者术后肺部感染的ROC曲线,结果显示,衰弱联合营养风险预测术后肺部感染的AUC为0.834(95%CI: 0.769~0.899), 当约登指数最大为0.563时,其灵敏度为67.9%, 特异度为88.4%; 衰弱预测术后肺部感染的AUC为0.763(95%CI: 0.685~0.841), 当约登指数最大为0.497时,其灵敏度为67.9%, 特异度为81.9%; 营养风险预测术后肺部感染的AUC为0.737(95%CI: 0.656~0.818), 当约登指数最大为0.430时,其灵敏度为82.1%, 特异度为60.9%。二者联合应用与单独应用衰弱的AUC差值为0.071, 差异有统计学意义(Z=3.144, P=0.001 7); 二者联合应用与单应用营养风险评分的AUC差值为0.097, 差异有统计学意义(Z=3.233, P=0.001 2)。见图 1。
3. 讨论
老年胃癌患者术前受长期的肿瘤消耗、营养摄入和吸收不足、术后禁食、手术创伤等应激因素影响,导致营养风险的发生率高达40%~80%[13-14]。衰弱是因老年人生理储备功能减退和多系统失调,机体应激耐受力下降,对不良结局易感性增强的临床综合征[15]。相关研究[16-17]证实,术前衰弱或存在营养风险的老年人,其术后并发症发生风险增高,死亡率增加。本研究共纳入217例胃癌患者,衰弱和高营养风险发生率分别为33.18%(72/217)和48.85%(106/217), 与既往研究[18-19]结果相似,证实老年胃癌患者常存在衰弱和营养不良状况。本研究结果显示,在同等营养风险下,评估为衰弱(≥3分)的老年胃癌患者术后肺部感染的发生率高于非衰弱患者,差异有统计学意义(P < 0.01); 当存在营养风险(NRS 2002≥3分)合并衰弱(≥3分)时,术后发生肺部感染的风险显著增高(P < 0.01)。WILSON J M等[20]在一项回顾性队列研究中发现,术前衰弱合并营养不良的老年髋关节术后患者,其并发症发生风险高于单独衰弱或营养不良者,短期并发症发生率为70%,死亡率达25%。SCHWARTZ A M等[21]研究显示,膝关节置换术后并发症发生率和30 d内死亡率在衰弱/营养不良队列中最高。本研究还发现,在校正年龄、手术类型、ADL、白蛋白等混杂因素后,营养风险(NRS 2002评分≥3)不再与术后肺部感染相关(P>0.05), 而衰弱仍是老年胃癌患者术后肺部感染的独立影响因素(P < 0.05), 术前评估衰弱的老年胃癌患者术后发生肺部感染的风险是非衰弱患者的3.628倍。CHEN F F等[22]在一项关于预测胃癌术后并发症的前瞻性队列研究中发现,在不考虑衰弱的情况下,营养风险是胃癌术后并发症的影响因素,但在校正衰弱等因素后,营养风险未保留在预测模型中,而衰弱仍然是术后并发症的重要预测指标,表明与营养风险相比,衰弱与术后肺部感染发生的相关性更大,原因可能为衰弱是反映老年人整体状况的评价指标,而营养是导致衰弱的影响因素之一,与衰弱的发生率密切相关,二者存在一定的协同关联。衰弱增加了老年患者术后并发症的发生风险[23], 早期常规衰弱和营养风险筛查结合多学科协同策略优化围手术期医疗和护理管理,可有效改善术后不良结局。
NRS 2002是欧洲临床营养和代谢学会(ESPEN)[24]及中华医学会肠外肠内营养学分会在《中国老年患者肠外肠内营养应用指南(2020)》中推荐的腹部手术患者术前营养筛查工具[25], 是目前临床上判断手术手风险和预测术后并发症的常用方法。然而,术后肺部感染的发生除了受营养因素影响外,还受年龄、机体生理功能状况、应激耐受能力及激素、心理水平等综合因素的影响,因此营养风险对老年术后肺部感染的预测仍有一定的局限性[26]。SCHWARTZ A M等[21]指出,衰弱与其他评分系统协同使用可增加其预测效能。本研究结果显示,衰弱评估、营养风险评分及二者联合预测老年胃癌患者术后肺部感染的AUC分别为0.763(95%CI: 0.685~0.841)、0.737(95%CI: 0.656~0.818)、0.834(95%CI: 0.769~0.899); 采用Z检验比较联合应用与单独应用衰弱、营养风险评估工具发现,预测效能的差异也有统计学意义(P < 0.01)。由此可见,衰弱联合营养风险评分对老年胃癌患者术后肺部感染的预测效能优于单独应用。PHEN H M等[27]在一项回顾性队列研究中证实,采用改良衰弱指数(mFI)和营养不良共同预测下肢骨折患者术后并发症发生风险高于单独应用衰弱或营养不良。WILSON J M等[20]研究也得出衰弱和低蛋白血症结合可增加对全髋关节置换术后并发症和死亡率的预测效能。由此可见,衰弱和营养风险同时存在时增加了术后并发症的发生风险。
本研究的局限性: ①本研究仅将住院期间发生的短期并发症作为结局指标,未对出院后长期不良健康结局进行随访研究,研究结果可能低估了一些并发症的发生率; ②本研究为单中心研究,可能存在选择偏倚,有待于后续研究中逐步完善。
综上所述,衰弱是老年胃癌患者术后肺部感染的独立危险因素,衰弱评估对老年胃癌患者术后肺部感染预测效能优于营养风险评分。在营养风险评估的基础上,联合衰弱评估可显著提高对老年胃癌患者术后并发症的预测效能。
-
表 1 2组患者一般资料比较(n=217)
一般资料 分类 感染组(n=42) 非感染组(n=175) χ2/t P 性别 男 30(71.4) 135(77.1) 0.607 0.436 女 12(28.6) 40(22.9) 年龄/岁 70.6±5.8 66.5±5.5 -4.256 < 0.001 经济收入 < 3 000元人民币 27(64.3) 93(53.1) 4.123 0.127 3 000~5 000元人民币 6(14.3) 52(29.7) >5 000元人民币 9(21.4) 30(17.2) 吸烟 是 17(40.5) 65(37.1) 0.160 0.689 否 25(59.5) 110(62.9) 心功能分级 Ⅰ级 16(38.1) 61(34.9) 0.264 0.876 Ⅱ级 25(59.5) 111(63.4) Ⅲ级 1(2.4) 3(1.7) 手术类型 开腹手术 9(21.4) 26(14.9) 1.081 0.298 腹腔镜手术 33(78.6) 149(85.1) ASA分级 Ⅰ~Ⅱ级 25(59.5) 134(76.5) 5.915 0.116 Ⅲ~Ⅳ级 17(40.5) 41(23.5) 高血压 是 16(38.1) 64(36.6) 0.034 0.854 否 26(61.9) 111(63.4) 糖尿病 是 6(14.3) 29(16.6) 0.131 0.718 否 36(85.7) 146(83.4) BMI/(kg/m2) 22.6±3.6 23.2±3.1 1.135 0.258 TNM分期 Ⅰ期 7(16.7) 47(26.9) 3.354 0.340 Ⅱ期 17(40.5) 66(37.7) Ⅲ期 18(42.8) 62(35.4) ADL评分/分 16.4±7.5 14.5±2.4 -1.657 0.004 白蛋白/(g/L) 35.4±4.0 36.7±4.7 1.669 0.097 球蛋白/(g/L) 24.6±5.4 24.5±4.0 -0.114 0.910 血红蛋白/(g/L) 116.6±21.4 122.5±23.5 1.496 0.136 衰弱 衰弱(≥3分) 28(66.7) 44(25.1) 26.342 < 0.001 非衰弱(< 3分) 14(33.3) 131(74.9) 营养风险 营养风险(≥3分) 33(78.6) 73(41.7) 18.415 < 0.001 无营养风险(< 3分) 9(21.4) 102(58.3) ASA: 美国麻醉医师协会; BMI: 体质量指数; ADL: 日常生活活动能力。 表 2 不同营养风险评分及衰弱患者术后肺部感染发生情况比较(n=217)
NRS 2002 衰弱状况 例数/例 感染 χ2 P < 3分 衰弱 12 2(16.7) 1.323 0.250 非衰弱 99 7(7.1) ≥3分 衰弱 60 26(43.3) 9.600 0.002 非衰弱 46 7(15.2) 表 3 老年胃癌患者术后发生肺部感染的Logistic回归分析(n=217)
模型类别 回归系数 标准误 Wald P OR 95%CI 模型1衰弱 1.330 0.412 10.433 0.001 3.782 1.687~8.476 NRS 2002 1.024 0.455 5.075 0.024 2.785 1.142~6.791 模型2衰弱 1.289 0.441 8.534 0.003 3.628 1.528~8.611 NRS 2002 0.610 0.509 1.435 0.231 1.840 0.679~4.989 模型2校正了年龄、手术类型、ADL、白蛋白。 -
[1] THRIFT A P, EL-SERAG H B. Burden of gastric cancer[J]. Clin Gastroenterol Hepatol, 2020, 18(3): 534-542. doi: 10.1016/j.cgh.2019.07.045
[2] ILSON D H. Advances in the treatment of gastric cancer: 2020-2021[J]. Curr Opin Gastroenterol, 2021, 37(6): 615-618. doi: 10.1097/MOG.0000000000000776
[3] 赵金辉, 谷顺通, 田丽, 等. 腹腔镜胃癌根治术患者术后肺部感染与影响因素分析[J]. 中华医院感染学杂志, 2019, 29(3): 403-406. https://www.cnki.com.cn/Article/CJFDTOTAL-ZHYY201903021.htm [4] 姚震旦, 杨宏, 崔明, 等. 胃癌根治术后60岁以上患者肺部感染危险因素分析[J]. 中华胃肠外科杂志, 2019, 22(2): 164-171. [5] 吴寒寒, 蒋建华, 程靖, 等. 老年营养风险指数与老年胃癌患者围手术期康复的关系[J]. 安徽医科大学学报, 2022, 57(11): 1816-1820. https://www.cnki.com.cn/Article/CJFDTOTAL-YIKE202211023.htm [6] 张莹, 陈丽娟, 白海燕, 等. 术前营养风险筛查对胃癌患者术后并发症、生活质量及预后的影响研究[J]. 临床和实验医学杂志, 2021, 20(10): 1094-1097. doi: 10.3969/j.issn.1671-4695.2021.10.024 [7] 丁昆, 李锐. 老年患者胃肠肿瘤根治手术术前衰弱与术后并发症的相关性[J]. 临床麻醉学杂志, 2021, 37(12): 1246-1249. doi: 10.12089/jca.2021.12.003 [8] 李秋萍, 韩斌如. 老年外科患者衰弱状态与术后并发症的相关研究[J]. 中国实用护理杂志, 2019, 35(6): 426-429. doi: 10.3760/cma.j.issn.1672-7088.2019.06.006 [9] FRIED L P, TANGEN C M, WALSTON J, et al. Frailty in older adults: evidence for a phenotype[J]. J Gerontol A Biol Sci Med Sci, 2001, 56(3): M146-M156. doi: 10.1093/gerona/56.3.M146
[10] 李秋萍, 韩斌如. 衰弱评估联合麻醉分级对老年患者术后并发症的预测研究[J]. 中华护理杂志, 2019, 54(5): 645-648. doi: 10.3761/j.issn.0254-1769.2019.05.001 [11] KONDRUP J, RASMUSSEN H H, HAMBERG O, et al. Nutritional risk screening (NRS 2002): a new method based on an analysis of controlled clinical trials[J]. Clin Nutr, 2003, 22(3): 321-336. doi: 10.1016/S0261-5614(02)00214-5
[12] 中华人民共和国卫生部. 医院感染诊断标准(试行)摘登(1)[J]. 新医学, 2005, 36(8): 495-495. https://www.cnki.com.cn/Article/CJFDTOTAL-XYXX200508040.htm [13] ZHANG X, TANG M, ZHANG Q, et al. The GLIM criteria as an effective tool for nutrition assessment and survival prediction in older adult cancer patients[J]. Clin Nutr, 2021, 40(3): 1224-1232. doi: 10.1016/j.clnu.2020.08.004
[14] 白静, 巴楠, 张小娟, 等. 胃癌根治术后肺部感染病原菌及危险因素[J]. 中华医院感染学杂志, 2020, 30(21): 3316-3320. https://www.cnki.com.cn/Article/CJFDTOTAL-ZHYY202021025.htm [15] 吴薇, 王青, 王鹏, 等. 老年住院患者步速和握力对全因死亡预测价值的比较[J]. 中华老年医学杂志, 2022, 41(4): 401-405. https://www.cnki.com.cn/Article/CJFDTOTAL-QKYX202232006.htm [16] DOGRUL R T, DOGRUL A B, KONAN A, et al. Does preoperative comprehensive geriatric assessment and frailty predict postoperative complications[J]. World J Surg, 2020, 44(11): 3729-3736. doi: 10.1007/s00268-020-05715-8
[17] VENIANAKI M, ANDREOU A, NIKOLOUZAKIS T K, et al. Factors associated with malnutrition and its impact on postoperative outcomes in older patients[J]. J Clin Med, 2021, 10(12): 2550. doi: 10.3390/jcm10122550
[18] 顾佳慧, 张浩, 孙敏莉, 等. 衰弱对老年手术患者预后影响的研究进展[J]. 中华麻醉学杂志, 2021, 41(1): 116-121. https://cdmd.cnki.com.cn/Article/CDMD-10403-1020972505.htm [19] ZHAO Y L, LIN T P, HOU L S, et al. Association between geriatric nutritional risk index and frailty in older hospitalized patients[J]. Clin Interv Aging, 2021, 16: 1241-1249. http://www.xueshufan.com/publication/3173513325
[20] WILSON J M, BOISSONNEAULT A R, SCHWARTZ A M, et al. Frailty and malnutrition are associated with inpatient postoperative complications and mortality in hip fracture patients[J]. J Orthop Trauma, 2019, 33(3): 143-148. http://pubmed.ncbi.nlm.nih.gov/30570618/
[21] SCHWARTZ A M, WILSON J M, FARLEY K X, et al. Concomitant malnutrition and frailty are uncommon, but significant risk factors for mortality and complication following primary total knee arthroplasty[J]. J Arthroplasty, 2020, 35(10): 2878-2885. http://www.nstl.gov.cn/paper_detail.html?id=ec602b2e6b2765c68941d4a9d1337f43
[22] CHEN F F, ZHANG F Y, ZHOU X Y, et al. Role of frailty and nutritional status in predicting complications following total gastrectomy with D2 lymphadenectomy in patients with gastric cancer: a prospective study[J]. Langenbecks Arch Surg, 2016, 401(6): 813-822. http://pubmed.ncbi.nlm.nih.gov/27485549/
[23] LI C M, LIN C H, LI C I, et al. Frailty status changes are associated with healthcare utilization and subsequent mortality in the elderly population[J]. BMC Public Health, 2021, 21(1): 645. http://www.socolar.com/Article/Index?aid=200260599855&jid=200000025496
[24] 袁凯涛, 石汉平. 《欧洲临床营养和代谢学会指南: 外科临床营养》解读[J]. 中国实用外科杂志, 2017, 37(10): 1132-1134. https://www.cnki.com.cn/Article/CJFDTOTAL-ZGWK201710018.htm [25] 中华医学会肠外肠内营养学分会老年营养支持学组. 中国老年患者肠外肠内营养应用指南(2020)[J]. 中华老年医学杂志, 2020, 39(2): 119-132. [26] 谢建忠, 李林, 黄彬, 等. 胃癌腔镜手术后肺部感染危险因素[J]. 中国感染控制杂志, 2020, 19(7): 653-656. https://www.cnki.com.cn/Article/CJFDTOTAL-GRKZ202007013.htm [27] PHEN H M, JONES C, KRAVETS V G, et al. Impact of frailty and malnutrition on outcomes after surgical fixation of lower extremity fractures in young patients[J]. J Orthop Trauma, 2021, 35(4): e126-e133. http://pubmed.ncbi.nlm.nih.gov/32910628/
-
期刊类型引用(5)
1. 任文文,王海燕,刘爱芳,易红,潘春燕. 胃癌术后病人衰弱变化轨迹的纵向研究. 循证护理. 2025(05): 924-930 .  百度学术
百度学术
2. 冯彩团,符仕康,王宁,郭殿华. 胃癌患者血清微小RNA-506和微小RNA-874的表达及其与幽门螺杆菌感染、病情严重程度的相关性. 实用临床医药杂志. 2024(07): 16-20 .  本站查看
本站查看
3. 万颖,罗俊峰,曾文兴,巢玲. 白细胞介素-6、白细胞介素-8、γ干扰素、肿瘤坏死因子-α联合检测对腹腔镜下胃癌根治术后并发肺炎的预测价值. 癌症进展. 2024(04): 392-394 .  百度学术
百度学术
4. 周晓梅,陈赛华,王鼎,肖婷,刘雷. 营养支持链式管理在胃癌围术期患者中的应用. 实用临床医药杂志. 2024(12): 61-65 .  本站查看
本站查看
5. 杨丽红,姚建琴,杨雪芳,丁欢,谷斌,顾晓莲. 1例晚期胃癌患者3级免疫相关性肺炎合并急性肺水肿的护理. 护士进修杂志. 2024(22): 2454-2457+2461 .  百度学术
百度学术
其他类型引用(0)




 下载:
下载:
 苏公网安备 32100302010246号
苏公网安备 32100302010246号